水
  |
水(みず)とは、次のいずれかの物質を表す用語である。
- 化学式 H2O で表される、水素と酸素の化合物[1]。
- 湯と対比して用いられている語[1]。温度が低く、かつ凝固して氷にはなっていない水。
- 液状のもの全般[1][注 1]。
- 元素としての水(18世紀までの文献に現れる用法)。
この項目では、H2Oの意味での水を中心としながら、幅広い意味の水について解説する。
呼称
水の概念を自然科学的に拡張して、化学式で H2O と表現できるものをすべて広義の「水」とすれば、固体は氷、液体は水、気体は水蒸気、ということになる。加熱してできた水蒸気を凝結した蒸留水など不純物をほとんど含まない水を、純水(及び超純水)と呼ぶ。
重水
水の化学式 H2O の水素が二つとも同位体の重水素である水を重水と呼び、化学式 D2O で表す。水素の一つが重水素であり、もう一つが軽水素である水は、半重水と呼び、DHO で表す。水素の一つが三重水素(トリチウム)である水は、トリチウム水(または三重水素水)と呼び、HTO で表す。重水・半重水とトリチウム水を併せ、さらに酸素の同位体と水素の化合物である水も含めて、単に重水と呼ぶこともある。この広義の重水に対して、普通の水は、軽水と呼ばれる。
軽水と重水は電子状態が同じなので、化学的性質は等しい。しかし、質量が2倍、3倍となる水素の同位体の化合物である水では、結合や解離反応の速度などの物性に顕著な差が表れる(速度論的同位体効果参照)。
日本語での呼称
日常的な日本語では、同じ液体の水でも温度によって名称を変えて呼び分ける。低温や常温では水と呼ぶが、温度が高くなると湯(ゆ)という[注 2]。しかし、英語 (water) やフランス語 (eau) などでは、液体であれば温度によらず名称は不変である[注 3]。
日本語では、低温の液体である水であっても、(湯などから立ち上った)水蒸気が凝結して空気中に細かな粒として存在する水は、湯気という。気象に関する用語では、粒の大きさによって、霧や靄(もや)と呼ぶ(これらを総称した一般用語として霞もある)。それらが上空にある状態では、雲と呼ぶ。雲から凝縮して大きめの水滴となって地上に落ちてくる水は雨と呼ぶ。上空で水蒸気が凝固して結晶となった氷は雪と呼ばれ、一体の結晶になっていない粒は、大きさによって霰(あられ)や雹(ひょう)と呼ぶ。それらが水と混合した状態になっていれば、霙(みぞれ)と呼ばれる。
用途、性質、存在する場所などによる呼び分けも行われている。例えば、水の中でも、特に飲用に供するものを飲料水という。海にある塩分などを多く含む水は海水、地下に存在する水は地下水と呼び、地下水を汲みボトルに詰めたものをミネラルウォーターと呼ぶ。また、用途によって、農業用水、工業用水などの呼称もある。機能と水質に基づく、上水、下水という呼称もある。
概説
水は人類にとって最もありふれた液体であり、基本的な物質である。また、人が生命を維持するには必要不可欠であり、さまざまな産業活動にも不可欠の物質である。
古代ギリシャではタレスが「万物のアルケーは水」とし、エンペドクレスは四大元素のひとつで基本的な元素として水を挙げた。古代インドでも五大のひとつとされ、中国の五行説でも基本要素のひとつと見なされている。18世紀の後半まで、洋の東西を問わず人々はそうした理解をしていた。それが変わったのは、わずか200年ほど前のことであり、19世紀前半に、ドルトン、ゲイリュサック、フンボルトらの実験が行われ、アボガドロによって分子説が唱えられたことによって、H2Oで表すことができる水素と酸素の化合物と理解されるようになった。(→#水の知識の歴史概略)
常温常圧では液体で、透明ではあるが、ごくわずかに青緑色を呈している(ただし、重水は無色である)。また無臭である。日常生活で人が用いるコップ1杯や風呂桶程度の量の水にはほとんど色がないので、水の色は「無色透明」と形容される。詩的な表現では、何かの色に染まっていないことの象徴として水が用いられることがある[注 4]。しかし、海、湖、ダム、大きな川など、厚い層を成して存在する大量の水の色は青色に見える。このような状態で見える水の色を、日本語ではそのまま水色と呼んでいる。(→水の色)
化学が発展してからは化学式 H2O で表され、水素原子と酸素原子は共有結合で結びついている、と理解されている。(→#化学的性質)
また水は、かつて1kgや1calの単位の基準として用いられた。(→#物理的性質)
すべての既知の生命体にとって、水は不可欠な物質である。生物体を構成する物質で、最も多くを占めるのが水である。核や細胞質で最も多い物質でもあり、細胞内の物質代謝の媒体としても利用されている。通常、質量にして生物体の70〜80%が水によって占められている。人体も60〜70%程度が水である。(→#生物と水)
地球表面、特に海洋に豊富に存在する。水は人類にとって身近であって、生物の生存に必要な物質であるが、宇宙全体では液体の状態で存在している量は少ない。(→#水の分布)
現代の人類の水の使用量の約7割が農業用水である。現代の東京の家庭での水の使用量を多い順に並べると、トイレ、風呂、炊事である。(→#水の使用)
下記では、水に関する人類の知識の歴史概略を解説し、続いて現代物理学での水の理解などを解説する。
水の知識の歴史概略
古代から18世紀まで
古代ギリシアの哲学者、一般に最初の哲学者とされる、紀元前6世紀ころの人物ミレトスのタレスは、万物の根源アルケーを探求する中で、アルケーは水であると述べたと伝えられている[2][注 5]。
同じく古代ギリシアのエンペドクレスは、水、空気、土、火を4つのリゾーマタ(元素)とし、それの集合や離散によって自然界のできごとを説明する、いわゆる四元素説を唱えた[2]。これはアリストテレスに継承された。
古代インドでも、地、水、火、風 およびこれに空を加えた五大の思想が唱えられていた[2]。また中国においても、万物は木・火・土・金・水の5種類の元素から成るとする五行説が唱えられた。
つまり、洋の東西を問わず、水は、基本的な4・5種の元素のひとつだと考えられていたのであり、こうした水の理解は、2,000年以上にわたって人々の間で一般的であった。18世紀後半の時点でも、ごく一般的であった。
こうした理解に変化が生じはじめたのは18世紀末のことであり[2]、人類の歴史の中に位置づけると、ごく最近のことである。18世紀末に、キャベンディッシュが、金属と酸とが反応を起こすときに、軽い謎の気体(現在では水素と呼ばれているもの)が発生し、それは簡単に燃えて水になることを発見した[2]。また,ラボアジエが、この燃焼で化合する相手が空気中の酸素であることを確かめた[2]。これによって、(実は)水は元素ではない、という考え方が登場した。ただし、ラボアジエの実験があっても、人々の考え方がすぐに変わったわけではなく、人々は以前どおり四元素の考え方をしていた、学者らもおおむね四元素の考え方をそれまでどおり用いていた、と科学史家らから指摘されている。18世紀までの文献に現れる「aqua」、「water」、「水」などは、基本元素としての水だと理解するのが適切である。
19世紀
その後19世紀初頭、イギリスのドルトンが実験の結果、水素と酸素が重量比で1:7で化合するとし(後に正しくは1:8と判明)、1805年にはゲイ・リュサックやフンボルトなどがそれぞれ、体積比で2:1で化合することを見出した[2]。さらに1811年に、アボガドロが分子説を唱え、その枠組みの中で水の分子がH2Oと定められた。このころ(19世紀の初頭)に西欧の学者たちの水の理解が変わったと科学史家らによって指摘されており、同世紀を通して一般の人々の理解も変化していったと考えてよい[注 6]。
分子説の成立とともにあったという点などで、水は近代化学の発展のきっかけを作ったものである[2]。この時期は、おおむねphilosophia(哲学)を母胎としてscientia(科学)が生まれつつあった時期と一致している。こうした新しい独特の哲学を行う人の数が徐々に増え、彼らが自分たちのことを他の哲学者から区別するためにscientist(科学者)という用語がヒューウェルによって1833年に造語され その使用が提唱された。
水と氷の近代以降の主要な研究の年譜
- 17世紀初頭 ベルギーのファン・ヘルモントは植物成長に関する実験により、水を元素と結論づけた。あらかじめ重量を測定した鉢植えに水だけを与え、4年後に重量を測定すると重量が増加していた。すなわち水元素が木元素に変換したことになる。ヘルモントはガスという用語を作り出している。ビールの発酵、石炭の燃焼、炭酸塩から発生するガスが全て同じものであり、命名もしていたが、彼自身の実験と彼のガスの関係には気づいていなかった。
- 1765年 イギリスのキャベンディッシュ、水を材料に熱の研究を行ない、蒸発熱や潜熱を測定している。
- 1766年 キャベンディッシュ、「人工空気の実験を含む三論文」を発表。第一論文で「可燃性空気」すなわち水素の発見を発表。ただし、水素の燃焼物が何であるかを理解していなかった。
- 1781年 酸素の発見者の一人イギリスのプリーストリーは水素の燃焼物が水であることを見いだし、キャベンディッシュに確認を求める。
- 1784年 キャベンディッシュが「空気に関する諸実験」を発表。水の組成を確認する実験について記述されている。実験には2年を要した。水素と酸素を電気火花によって反応させると大量の反応熱を出すため、生成物にどうしても窒素の酸化物である硝酸が混入してしまうためであった。彼の論文では水素と酸素を可燃性空気と脱フロギストン空気としているものの、水素2容積と酸素1容積から水が生成することを確認している。フロギストンによらない説明を最初に与えたのは酸素という名を命名したラボアジェであった。
- 1785年 ラボアジェが赤熱した鉄管に水を通すと水素が発生することを示し、水素、酸素こそが元素であって、水は化合物であることを最終的に確認した。
- 1791年 イタリアのボルタが酸素と水素が一定の比率で化合する性質を利用し、逆にこれらの気体の分量を測定するユージオメーターを開発した。
- 1800年 ボルタ、化学反応による電流の発生に成功。「ボルタの電堆」と呼ばれる(電池)。
- 1801年 イギリスのウィリアム・ニコルソン、「ボルタの電堆」を用いて、初めて水を電気分解した。陰極に水素が2容積、陽極に酸素が1容積発生することを示した。
- 1920年 この頃までに水素結合の概念が提唱される。
- 1933年 バナールが、水のX線構造解析を行う。
- 1935年 ポーリング、氷の残余エントロピーの理論。
- 1936年 中谷宇吉郎、雪の結晶を人工的に世界で初めて作成する。
- 1958年 アイゲン、水中のプロトン移動に関するモデルを提唱する。
- 1971年 ラーマンにより、水の分子動力学法によるシミュレーションが行われる。
- 1971年 ペイジが、水の中性子による構造解析を行う。
- 1994年 三島修が、2 つのアモルファス氷の間(低密度⇔高密度)の一次相転移を発見。
- 2005年 R. J. D. Miller らにより、水にレーザーパルス照射で生じさせた構造変化は 50 フェムト秒以内に失われることが報告された[3]。
物理的性質
Vienna標準平均海水
水の物理的性質は、その構成要素である水素と酸素の同位体の構成割合によって顕著に異なる。したがって、同位体の構成割合が厳密に定められた水についての測定が必要であり、これによって得られた測定結果でなければ、現代の科学においては意味がない。
水の厳密な測定に用いられる国際的標準物質となっている水は、「Vienna標準平均海水(en:VSMOW)」[注 7][注 8][4]であり、以下の物理的性質は、このVSMOWについてのものである[注 9][5][6]。

| 水 (H2O) | |
|---|---|
|

|
水、オキシダン(系統名) | |
別称 | |
| 識別情報 | |
| CAS登録番号 | 7732-18-5 |
| PubChem | 962 |
| 日化辞番号 | J43.587B |
| KEGG | C00001 |
| ChEBI | |
| RTECS番号 | ZC0110000 |
| 特性 | |
| 化学式 | H2O or HOH |
| モル質量 | 18.01528(33) g/mol |
| 外観 | 常温でわずかに青緑色を呈す透明の液体(ただし重水は無色) |
| 密度 | 999.974 95 kg·m−3, 液体 (3.984 °C) 916.8 kg·m−3, 固体 (0 °C) |
| 融点 | |
| 沸点 |
約99.9743 °C,(373.1243 K)[7] |
| 酸解離定数 pKa | 15.74 pKa2~35-36 |
| 塩基解離定数 pKb | 15.74 |
| 粘度 | 0.001 Pa·s at 20 °C |
| 構造 | |
| 結晶構造 | 六方晶系 |
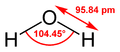
| 分子の形 | 曲線状 |
| 双極子モーメント | 1.85 D |
| 熱化学 | |
| 標準生成熱 ΔfH |
-285.830 kJ mol−1(l) -241.818 kJ mol−1(g) |
| 標準モルエントロピー S |
69.91 J mol−1K−1(l) 188.825 J mol−1K−1(g) |
| 標準定圧モル比熱, Cp |
75.291 J mol−1K−1(l) 33.577 J mol−1K−1(g) |
| 危険性 | |
| 主な危険性 | 水中毒, 水死 |
| NFPA 704 | |
| 関連する物質 | |
| 関連する溶媒 | アセトン メタノール |
| 関連物質 | 水蒸気 氷 重水 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
同位体の割合
天然の水には、約 0.031 146% の重水が含まれている[8]。その大部分である 0.031 069% が HDO(正確には HD16O)分子である。
水の色
水の色は一般に無色透明といわれることが多いが、実際には水分子の赤外吸収スペクトルが可視領域に裾野を引き、赤色光をわずかに吸収するので、ごくわずかな青緑色を呈する。海などの厚い層を成す水および巨大な氷が青いのはこれによる。ただし、重水(D2O)は無色である(水の青#重水の色)[9]。
融点
融点は 273.152 519 K、すなわち 0.002 519°C である[注 10][10]。しかし、過冷却状態になる環境下では、99.9743°C 以下の水蒸気も、0.002 519°C 以下の水も存在する。
沸点
標準気圧(101 325 Pa)での沸点は、約99.9743°C[注 11][注 12][11]である。
密度
3.984°C のとき最大密度 999.974 95 kg·m−3である。固体は液体より密度が小さい[注 13](異常液体)。したがって、固体である氷は液体の水に浮き、氷に圧力をかけると融ける。これは多くの他の分子とは異なる水の特性であり、氷の結晶構造が水分子間での水素結合によってかさ高いことによる。氷が融解して水になると、その体積は約11分の1減少する。詳細については氷の項も参照。
亜臨界水・超臨界水
水の臨界点は圧力22.12MPa、温度374.15°C (647.30K) である。水は臨界点まで蒸気圧曲線に従い、ある温度である圧力以上をかけると液体の状態を保つ。この状態の水(下限は大気圧、100°C)を亜臨界水という。さらに、臨界点以上の圧力・温度条件の水を超臨界水という。亜臨界水ではイオン積が常温常圧の水より高く、オキソニウムイオンおよび水酸化物イオンの濃度が高くなる。一方、超臨界水ではイオン積が常温常圧の水より低くなる。また、超臨界水は比誘電率が低くトルエンと同程度までになるため、常温常圧水と異なり、油との混合が可能となる。亜臨界水および超臨界水はそれぞれが持つ性質を利用した技術の研究が行われている。
過冷却水
凝固点(1気圧では0 °C)以下でも凍っていない、過冷却状態の液体の水のこと。不安定であり、振動などの物理的ショックにより結晶化を開始して氷に転移する。過冷却水の入っている容器にビー玉などを落とすと、物体が底に着く前に着水点から凍結が広がり、全体がシャーベット状に凍りつく。特別な実験装置などは必要なく、家庭の冷凍庫でも実験可能。ペットボトル等の容器に水(不純物のないものが望ましい)を入れ、−5–−10 °Cほどの温度を維持して冷却する。急激に冷やさず時間をかけること、振動を与えずに水全体が均一に冷やされる状況を作り出す(保冷剤やタオル等で包むなど)ことが成功のカギ。
アモルファス氷
非結晶の氷のこと。通常の氷は結晶であるが、液体からの急冷、結晶氷を加圧、あるいは気相からの蒸着などの方法により、非結晶の氷が生成される。密度の違う2つの状態が存在し、それぞれ、高密度アモルファス氷、低密度アモルファス氷という[12]。
その他
水は比熱容量が非常に大きい。
反磁性の性質を示す代表的な物質でもあり、強力な磁石を近づけると水が反発して逃れるように動く現象は、旧約聖書の逸話にちなみ「モーゼ効果」と呼ばれている(俗称ではなく正式な学術用語)。
また、水分子の回転のエネルギー準位がマイクロ波のエネルギーに対応するので、水はマイクロ波を吸収しやすく、電子レンジはそれを利用して加熱をしている。
液体の状態では 10−7 (mol/dm3) (25°C) が電離し、水素イオン(正確にはオキソニウムイオン)と水酸化物イオンとなっている。 一般的に水は電気絶縁性が低いといわれるが、これはイオンなどの不純物が含まれる場合の水の性質である。純粋な水は電気(電流)をほとんど通さない絶縁体である[注 14]。これを利用して、超純水の純度測定に電気伝導度を用いることがある。
化学的性質
水は化学的には化学式 H2O で表される、水素と酸素の化合物である。水分子の酸素原子と水素原子は共有結合で結びついており、その結合は水素原子と酸素原子から価電子を1つずつ供給されてできている。さらに酸素原子の最外殻には共有結合に使われていない孤立電子対が2つ存在する。水素と酸素の電気陰性度の違いから、O-H 結合においては酸素原子側が電気的に負、水素原子側が正となり、局所的に電気双極子を作っている。分子全体でも H-O-H 結合角が曲がっていることから極性を持つ。以上の理由から水の比誘電率は 79.87 (20℃) と高い。このためイオン間の静電気力を弱め塩化ナトリウムなどのイオン結晶の結合格子を破壊して溶解させる、すぐれた溶媒として働く。複数の水分子の間では水素原子と酸素原子の間に水素結合を作る。水に限らず、最外殻に孤立電子対を持つ窒素や酸素やフッ素などの原子やイオン、あるいは電気陰性度が高い原子に結合している水素原子は水分子と水素結合を作ることができる。したがって水は、糖などイオン性ではない分子に対する溶解性も示す。一方、シクロヘキサンなどの炭化水素はイオン性でなく、水素結合も形成しないため、水には溶解せずに寄り集まって油滴を作る。このように水に溶けない疎水性の化合物同士が水の中で見かけ上親和性を示す現象を疎水効果と呼ぶ。
複数の水分子の間に水素結合が働くことで、クラスター状の高次構造(水クラスター)が生じる。水の高次構造は寿命がピコ秒からフェムト秒オーダーと非常に短く、一度形成してもすぐ別の高次構造に移り変わる。
水分子は水素イオン (H+) の供給源として酸としての性質を示す。水分子の酸素原子上に孤立電子対があることから、水は塩基、配位子としてもはたらく。水分子を配位子とする錯体は水和物、もしくはアクア錯体と呼ばれる。酸と塩基の定義のうち、アレニウスによる定義は水溶液中を前提にしたものである。
水は、使い捨てカイロでの鉄粉の酸化、6-ナイロンの合成など、化学反応の触媒としても用いられることがある。また、酸や塩基などを触媒としてエステルやアミドなどの加水分解や、アルケンへの付加反応(水和反応)の基質となる。
生化学反応でも水は頻繁に現れる。光合成では水が4電子酸化を受けて酸素となる。
不均一モデル
水分子が液体中では水素結合でつながっているが、詳しいつながり方ははっきりとは分かっていない。ケンブリッジ大学の教授が1930年代「連続体モデル」を提唱、氷の時と同じように4個の分子が正四面体を作って固まっており、それが若干のゆがみがあっても同じ構造が続く連続体であるという考え方である。
「ミクロ不均一モデル」は、つながった状態とつながりが切れた状態の2つが入り交じっているという考え方である。水が4℃で最も比重が大きくなる理由を説明するために、1892年にヴィルヘルム・レントゲンによって提唱され、考えられた。
2013年、理化学研究所原田慈久氏(現東京大学准教授)、丹羽秀治 特任研究員、德島高 技師などのチームがSpring-8を使った実験で不均一モデルを示す軟X線測定での2つのピークを観察した。連続体モデルではピークは一つである[13][14]氷によく似た秩序構造が水の中に存在していることが判明した。[15][16][17]。
標準としての水
水は生活において大変手頃で重要な存在だったので、かつては単位の基準として重要な役割を果たしていた。日常生活においては高い精度は問題にされないので、(温度や純度をあまり気にせず)水1cm3が1gとして便利に使われたり、「比重が1よりも大きい物質は水に沈む」と言われるなど、生活に密着した基準として水は依然として重要な存在である。
温度の標準
水の融点が0°C(精密には、0.002 519°C)、沸点が100°C(精密には、約99.9743°C)という切りのよい値であったのは、水の融点と沸点を基準としてセルシウス度の目盛りを定義したからである。
現在では、水の三重点の熱力学温度の1/273.16 が K(ケルビン)と定められている。しかし、新しいSIの定義では、ケルビンはボルツマン定数によって定義することが提案されている。
質量
1g(グラム)の元々の定義は4°Cのときの1cm3の水の質量であった。 しかし、水に質量の基準として高い精度を要求するとなると、必然的に高純度の水、高精度の体積、圧力、温度が要求されることになり、これらはいずれも技術的に困難である[注 15]。このため現在の質量の定義は1870年代に製作された国際キログラム原器を1キログラムとしている(キログラムを参照)。現在では、水が最大密度となる3.984°Cのときの1cm3の水の質量は、0.999 974 95gである[注 16]。また、従来は密度 (g/cm3) と比重が完全に一致していたが、この定義を境に一致しなくなった。
なお、新しいSIの定義では、キログラムはプランク定数によって定義することが提案されている。
熱量
1cal(カロリー)の元々の定義は、1gの水を1°C(1K の温度差)上げるのに必要な熱量であった。しかし、現在では、カロリーはJ(ジュール)によって定義されている(日本の計量法体系では、1 cal = (正確に)4.184 J である)。
水の分布
   |
地球上の水
地球上には多くの水が存在しており、生物の生育や熱の循環に重要な役割を持っている。気象学や海洋学などの地球科学、生態学における大きな要因の一つである。水蒸気は最大の温室効果ガスでもある[18]。
地球の水の総量は約14億 km3(= 1.4×1018 m3)と言われ、その97%が海水として存在し、淡水は残り3%にすぎない。そのほとんどが氷河や氷山として存在している。氷の状態の淡水の大部分は南極大陸とグリーンランドが占めている[19]。
| 位置 | 淡水湖 | 河川水 | 地下水浅 | 地下水深 | 土壌水 | 氷河 | 大気 | 塩水湖 | 海洋 |
|---|---|---|---|---|---|---|---|---|---|
| 存在比 (%) | 0.009 | 0.0001 | 0.31 | 0.31 | 0.005 | 2.15 | 0.001 | 0.008 | 97.2 |
このなかで、淡水湖・河川水・地下水浅が、人間が直接に利用可能な水で、総量の1%未満である。飲料水として利用できるものはさらに少ない。海水は天然および人工の全ての汚れを合わせ高濃度に汚染されているため、資源としての利用価値はほとんどない[19]。
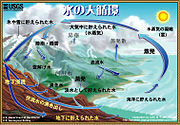
地球における継続的な水の循環は水循環と呼ばれている。太陽エネルギーを主因として、固相・液相・気相間で相互に状態を変化させながら、蒸発・降水・地表流・土壌への浸透などを経て、地球上を絶えず循環している。また、この循環の過程で地球表面の熱の移動や浸食・運搬・堆積などの地形を形成する作用が行われる。
太陽系の水
太陽系の惑星および衛星の表面に存在する水のほとんどは氷または水蒸気であり、地球以外で液体の水が存在する場所は少ない。相図からわかるように、液体の水が存在できる温度範囲は高圧ほど広くなる。逆に、火星のように気圧の低い環境では、液体の水は安定に存在することはできない。
火星の表面にはかつて液体の水があったことが判明している。
木星の衛星エウロパは、内部に液体の水からなる海があるのではないかと言われている。
太陽系外の水
太陽系外惑星には、大量の液体の水を保持している可能性のある惑星がいくつか見つかっている。例えばケプラー22bやグリーゼ581d、HD 85512 bといった惑星は、地球と同じような環境で水の海を持つと推定されている。しかし、GJ 1214 bやかに座55番星eといった惑星は、地球とは異なり、高温高圧の超臨界水の海を持つとされている。
2012年、ハッブル宇宙望遠鏡の観測により、GJ 1214 bが高温の水蒸気の大気を持つ事が確認された。大気の下には超臨界水の海が存在する可能性がある[20]。
2011年、クエーサーAPM 08279+5255の降着円盤に、地球の水の140兆倍という膨大な量の水が発見された。APM 08279+5255は、宇宙誕生から16億年後の時代に存在する天体であり、このことは、既にこの時代に大量の水が存在していた事を示している[21]。
生物と水
   |
生物体を構成する物質で、最も多くを占めるのが水である。核や細胞質で最も多い物質でもあり、細胞内の物質代謝の媒体としても使用されている。通常、質量にして生物体の70% - 80%が水によって占められており、そのうちわずか数%でも不足するとのどの渇きや熱中症など生命活動に不都合があらわれる。
生きている細胞には(理想的な溶媒である)水が多く含まれており、生命現象を司る化学反応の場を提供し、また水そのものが種々の化学反応の基質となっている。体液として、体内の物質輸送や分泌物、粘膜に用いられる。また高分子鎖とゲル化することで体を支える構造体やレンズにも利用されている。クマムシのように厳しい環境にも耐えられる生物は、体内の水分を放出し、不活性な状態をつくり出すことができる。
なお、「生物は太古の海で誕生した」とされることがある。生物の化学組成と海水の組成が似ていることもその説の根拠の一つである。地上の生物もその先祖をたどれば水中生活をおくっていた、とされる。
陸上のように、常に水につかっていない環境では、生物にとって最も重要な問題の一つが水の確保である。陸上の無脊椎動物では、周囲が湿っていなければ活動できないものも多い。陸上生物に見られる進化的形態の多くが水の確保や自由水のない環境への適応である。クマムシの場合も、頻繁に乾燥にさらされる環境への適応として、休眠の能力が発達したと考えられている。
人間と水
人体と水
人体における水分量は年齢・性別によって異なり、新生児で約80%、成人で60%前後、高齢者は50%台となる。また女性は男性に比べて体内の脂肪分が多い関係で水分量は同年代の男性に比べてやや少ない[22]。そして「その人体の水のうち45%までが、細胞内に封じ込められた水[要出典]で、残り15%が血液・リンパ液など細胞の外にある水」と言われている[誰?]。この細胞内液、細胞外液をあわせたものを体液と呼び、この体液が生命の維持、活動に重要な役割を果たす。
なおニッスイによると一日に排出される水の量は体重60kgの成人男性で2,500mLであり、内訳としては尿1,400mL、糞100mL、汗500mL、肺からの呼気500mLである。1日に必要な水の量は当然2,500mLで、一般に飲料水から1,200mL、食物1,000mL、代謝物300mLとして摂取される[22]。
汗は非常に効率よく体温を下げる機能をもつ。水の蒸発潜熱が大きいのは水素結合が強いことに起因している。
- 脱水症
体内の水分量が不足した状態を医学的には脱水と呼ぶ。水分喪失量に対して水分摂取量が不足することによって起こる。水分摂取不足、あるいは水分喪失過剰、あるいは水分摂取不足と水分喪失過剰の同時進行によって起きる。具体的には、高温の環境、重作業、激しい運動、発熱、下痢、嘔吐などが原因となって起きる。
- 水中毒
人体が過剰な水分を投与された場合、細胞外液の浸透圧が異常に下がり、低ナトリウム血症によって悪心、頭痛、間代性痙攣、意識障害等の症状を引き起こす。これを水中毒と言い、輸液ミス、心因性多飲、SIADHなどの結果としてみられる。なお致死量は体重65kgの人で10 - 30リットル/日である。
人間の健康と水
安全な水を飲めるかどうか、ということは人間の健康に大きな影響を及ぼしている。 汚物などに触れた不衛生な水を飲むと、コレラ・腸チフス・赤痢などで命を落とす人が出る。そしてこれらの病気は感染する。体力の弱い乳幼児は、不衛生な水と摂ると、しばしばひどい下痢を起こし脱水症状で死亡する。老人も免疫力が弱く、不衛生な水で命を落としやすい。また、不衛生な水は寄生虫の問題も引き起こす。
古代でも中世でも、人類のほとんどは水道無しで生きていたと考えてよい。都市で暮らすにしても上水道がなかったのである。 安全な水を飲む方法として古代から行われているひとつの方法は煮沸(しゃふつ)してから口に入れるということである。
水道

ローマ帝国(古代ローマ)は、土木技術に秀でており、ローマに水を引くべく水道を建設した。これのおかげでローマの住むローマ市民は公衆浴場を利用することができた。公共の水洗トイレもあった。石でできたベンチ状のものの下を水が流れており、ベンチには穴があいており、そこにこしかけて用をすれば、排泄物が流れてゆくのである。ローマのように水がふんだんにある都市生活は世界的に見て例外的であり、他に類をみない状態であった。 ローマ帝国の時代、ローマという都市に住む人たちは風呂に頻繁に入っていたわけだが、その後、彼ら(かつてのローマ帝国の中核的市民。今のローマ市民やイタリア人)は頻繁に風呂に入る習慣は失った[注 17]。
都市では、都市で生活する者に安全な飲料水をいかにして届けるかということは、都市を治める者、政治を行うものにとって大きな問題である。
日本の江戸では、水不足の状態を改善するために、1652年に玉川上水の建設が計画され、翌1653年、まずは本線が建設された。難工事で幕府の用意した資金は底をついてしまい、玉川兄弟は自宅を売って建設を続行したという。承応3年(1654年)6月から、江戸市中への通水が開始された。玉川上水は江戸っ子の自慢となった。江戸の上水道は世界的に見て質が高かったと指摘されることは多い。

ヨーロッパではどんな状態だったかというと、ヨーロッパでは中世、各都市は外敵を防ぐべく壁をつくり(城塞都市)、自治が行われ、独立性が高く、小さな国のような様相を呈するものが多かった。ヨーロッパの都市では、街の広場などに、都市の近くの山などから水道で水を引き[注 18]、その水を出す fonte フォンテ (イタリア語、ポルトガル語。フランス語では fontaine フォンテーヌ、日本語では「泉」)を設置して、飲料水を市民に提供しているものが多かった。市民は桶を持って広場にやってきて、この「泉」で水を汲んで、水が入った重い桶を持って家まで運び、各家でそれを使うのである。つまり「水道」があるといってもそういう程度のことであったのであり、基本的に各家まで引かれていたわけではない。
ヨーロッパの水事情を理解するための一例として、フランスの首都のパリの水事情について説明すると、パリの水事情はひどいものであった。16世紀・17世紀・18世紀と、パリ市民は安全な飲料水をたっぷりと確保できていたわけではない。基本的に、風呂に入る、などということは考えられない状態であった。やることと言えば、布に水や湯をふくませて、身体を拭くということだったり、せいぜいやるとしても、身体があまりに臭くなったら、桶やたらい(金たらい)を用意して、服を脱いでその中で立って、桶にくんだ水をチョロチョロと身体にかけて流し、数分後にはそそくさと身体を拭く、という程度のことであった。(日本人のように熱い風呂に全身をどっぷりと沈めて身体を温めるなどという発想はフランス人にはまったく無かった。) 汚水の扱いもひどいもので、パリに下水道が整備されていなかったものだから、市民は、汚物を家(アパルトマン)の前の街路に捨てていた。当時、パリの街路は道の端や真ん中に水が集まるようにしてあり、雨になるとそこを雨水が流れるのだが、そこに汚物が大量に流れ、街全体に悪臭が漂っていたのである。そんな状態が常態化すると、しまいには、建物の3階・4階などに住み、いちいち1階まで歩いて降りる手間を面倒に感じる者などでは桶に入った汚物を窓から直接放り投げるような不届き者すらもいた。パリの街を歩くには、足元の汚水にも気を付けなければならないし、同時に、頭上にも注意を払って汚物をかけられないように気を付ける必要すらあったのである。この状況が変わったのは19世紀のことで、オスマンが行ったパリ改造(オスマニザシオン)のおかげであり、オスマンは、パリ市民のために安全な水を豊富に確保するために、パリから100kmも離れた水源からパリに水を引くという決断(大英断)を行い、それが成功し、各家庭に十分に水を届けることが可能になり、その結果、当時、パリの各家庭でバスタブを置き風呂に入るということがちょっとした流行になった。だが、今でもフランス人はあまり風呂に入らない。少なくとも日本人のように毎日風呂に入ったりするような習慣は全然無く、本当にたまにしか入らない[23]。なお、フランス人は、日本人のようには風呂に入らないかわりに、(風呂に入らない身体のひどい体臭をごまかすために)香水を用いるという文化が発達した。
途上国などでは現代でも水道が無い国が多く、毎日自力で長距離を歩いて重い水をバケツ等で家まで運ばなければならず、その労働のために学校へ行くことすらままならないという子供たちが多数存在している。
産業利用を目的とした水利は、用水路と呼ばれる(農業用水・工業用水)。

世界の水の使用量
世界の水の使用量は1995年の段階で年間約35,700億m3で、内訳としては、農業用水が約25,030億m3/年で約7割を占め最大、工業用水が約7,150億m3/年、生活用水が約3,540億m3/年だった、とも推定されている。水使用量は1950年から1995年までで2.6倍になっているともされ、2025年には30億人以上が水の量と質の限界(水ストレス)に直面する、とも予想されている[24]。仮想水という指標で水の使用量が計算されている。
家庭での水の使用状況と用途
家庭での水の使用量は、国ごとに著しく異なる。途上国の中には「一日一人あたり数リットル」という国がある。その一方で、先進国では「一日一人あたり数百リットル」という国が多く、途上国と先進国の間には大きな差がある。日本の家庭の使用量も他の先進諸国と同様、最も高い部類に属する[注 19]。
日本での使用状況の一例として東京の家庭でのそれを挙げると、1日で1人あたり242Lの水を使っている(2005年現在、東京都水道局調べ)。家庭での水の使用量のうち、28%がトイレ、24%が風呂、23%が炊事、17%が洗濯となっている(2002年、東京都水道局調べ)[25]。
水の利用
  |
農業
世界のそれぞれの地域における水の状況は、地域による差、気候の差の影響を大きく受ける。その水の状況が、農業に影響を与え、社会構造にも影響を与えている。
水と芸術

水は人類にとって最も身近で重要な物質であり、かつ様々な態様を見せることから、水をモチーフとした数々の芸術作品が生み出されている。 水そのものを取り入れたものに庭園における池や噴水がある。
別称
- IUPAC系統名はオキシダン (oxidane) であるがほとんど用いられない。(→記事「水素化物」参照)。ほか、「一酸化二水素」「酸化水素」「水酸」「水酸化水素」といった呼び方をすることも可能である。
- ラテン語ではAquaアクウァ(アクワ)。
- 水をネタに、感情的な環境保護論を揶揄するジョークがある。記事「DHMO」(Dihydrogen Monoxide) 「一酸化二水素」を参照。
代表的な慣用句
- 水掛け論 - 田に水がほしい双方が水を掛け合ってまで争うところからきているといわれる。
- 湯水のように(ごとく) - 大量に使うことを指し、通常は無駄遣いや乱費の表現として用いられる。日本ではかつて「水と安全はタダ」など言われ、水は非常に安価または無料の代名詞であった。茶道の点前で茶道具を清めるために大量の湯水を使うことに由来する。
- 水商売(またはその略称「お水」) - 飲食業または風俗業の別称。一日の客数が安定しない(水物である)から。一説に、酒の水割り用の水道水に値段を付ける(金を取る)ことから。
- 水に流す - 過去の因縁を忘れること。汚れ物は水に溶かして流れ去るに任せるのが古来の流儀である。実際に、多くの汚物は水中における自然の浄化作用とその人工的応用である汚水処理によって処理される。
他にも、世間や市場に普遍的なもの(貨幣や情報など)を水にたとえて、洪水のような」、「氾濫する」などと表現されることがある。
注釈
- ^ エンジンの「冷却水」など水以外の物質が多く含まれているものも水と呼ばれる場合がある。日本語以外でも、しばしば液体全般を指している。例えば、フランス語ではeau de vie(オー・ドゥ・ヴィ=命の水)がブランデー類を指すなど、eau(水)はしばしば液体全般を指している。そうした用法は、様々な言語でかなり一般的である。
- ^ 特に温度の高いものは熱湯(ねっとう)という(理・工学的な分野では熱水(ねっすい)という語も用いられる)技術用語では高い温度の湯に相当するものも水と呼ぶ(例:冷却水)。アイヌ語では、低温の水のことをワッカ、高温の水(湯)のことをウセイという。
- ^ 英語では、温度が高い場合でも名詞 (water) は変わらず、形容詞を付加する (hot water)。
- ^ ただし、これはメタファーであって、物理学的な言葉の使い方とは異なる。
- ^ これを伝えているのは、アリストテレスの書などである。
- ^ 「共通に支持されている理論体系と矛盾する断片的な発見がいくつあっても人々の考え方の体系(理論体系)は基本的に変化せず、それが変わるのは、あくまで別の理論体系が現れた時だけである」とする考え方は、20世紀の科学哲学者クーンがパラダイムシフトという用語を用いて提唱した。
- ^ 「ウィーン標準平均海洋水」とも訳される。「海水」(Ocean Water)の文字が使われているが、純水であることに注意。
- ^ 測定に実際に用いるVSMOWは同位体比が次のように規定されている。2H/1H = 155.76 ± 0.1 ppm、3H/1H = (1.85 ± 0.36)×10-11 ppm、18O/16O = 2005.20 ± 0.43 ppm、17O/16O = 379.9 ± 1.6 ppm
- ^ 例えば、「水の三重点」はケルビンの定義に用いられているが、この「水」は、VSMOWである
- ^ 国際温度目盛(ITS-90)による、Vienna標準平均海水(en:VSMOW)についてのものである。
- ^ 国際温度目盛(ITS-90)による、Vienna標準平均海水(en:VSMOW)についてのものである。
- ^ 理科年表では、約99.974°Cとしている(理科年表、平成26年版、p.397注、丸善出版、2013年11月30日発行 )
- ^ 通常気圧において、氷の密度は0.9168g/cm3 である。
- ^ 自己解離によりわずかに電気を通す。6.40×10−8Ω−1 cm−1 (25°C)。
- ^ 特定の物質を出発点にして質量の基準を定めようとすると、純度、体積(=寸法3)、圧力、温度、同位体の割合が関わってくるので、これらを同時に高精度に維持しつつ質量を決定することは、水に限らずどのような物質であろうが容易ではない。なお、ケイ素は不純物が非常に少ない単結晶を作りやすいので、次世代の質量の基準となる物質として候補にあげられているが、やはり体積、温度の精度も上げる必要があり、アボガドロ定数と組み合わせるなどの工夫も考えられている。
- ^ 質量は国際キログラム原器によって定義されたが、これから逆に物質の密度を高精度に求めようとすると、その物質の純度や、体積、圧力、温度、などの精度と同位体の割合が関わってくるので、質量の基準を求めるときと全く同じ理由によって、やはり容易ではない。
- ^ このあたりの経緯・事情はヤマザキ・マリなども調べており『テルマエ・ロマエ』に書いている
- ^ ローマ人が実例を見せ、教えてくれた土木技術のおかげで、ヨーロッパ人にも一応それはできるようになっていた。フランスやドイツなど、つまり、かつてローマ帝国の市民からは「ガリア」と呼ばれ、辺境の地で、どうしようもない野蛮人たちが住む場所と見なされた土地にもローマ帝国の強大な軍事力を使った侵略・進出の結果、ローマ帝国の高度な土木技術が残されたのである。)
- ^ 関連資料。
- INAXニュースリリース『日本人は、一人一日に1,460リットルの水を輸入していることを知っていますか?「ヴァーチャルウォーター(仮想水)」という考え方』
- 大阪ガス「生活者ができる地球温暖化防止のために」 (PDF)
- 三宅基文、沖大幹、虫明功臣 「日本を中心とした仮想水の輸出入」(第 6 回水資源に関するシンポジウム論文集, 2002)MS Word文書。
- AQUASTAT, FAO 2005, 「Water availability information by country」
出典
- ^ a b c 広辞苑 第五版 p.2551 【水】
- ^ a b c d e f g h 平凡社『世界大百科事典』第27巻、pp.342-343【水】>【水の科学】
- ^ Cowan, M. L.; Bruner, B. D.; Huse, N.; Dwyer, J. R.; Chugh, B.; Nibbering, E. T. J.; Elsaesser, T.; Miller, R. J. D. (10 Mar 2005). “Ultrafast memory loss and energy redistribution in the hydrogen bond network of liquid H2O”. Nature 434 (7030): 199–202. doi:10.1038/nature03383. ISSN 0028-0836.
- ^ 国立天文台編、理科年表2016、p.411脚注2)、2015年11月30日発行、丸善出版(株)、ISBN 978-4-621-08966-8
- ^ 国立天文台編、理科年表2016、p.364 温度の欄および脚注1)、2015年11月30日発行、丸善出版(株)、ISBN 978-4-621-08966-8
- ^ List of physicochemical data concerning water 脚注 a The Vienna Standard Mean Ocean Water (VSMOW) is pure salt-free water used as a standard water material for determining the physical properties of water and the Kelvin and Celsius temperature scales (using the triple point of water, 0.01°C, 273.16 K). It is made by mixing purified ocean waters. It contains 99.984426 atom % 1H, 0.015574 atom % 2H (D), 1.85 x 10-15 atom % 3H (T; equivalent to about one disintegration min-1 mol-1 water), 99.76206 atom % 16O, 0.03790 atom % 17O and 0.20004 atom % 18O
- ^ a b ITS-90によるVienna標準平均海水en:Vienna Standard Mean Ocean Water (en:VSMOW)のもの
- ^ List of physicochemical data concerning water Molar isotopic compositionの欄、HD16OとHD17OとHD18OとD216Oの割合の合計
- ^ List of physicochemical data concerning water Colorの欄
- ^ List of physicochemical data concerning water Water Structure and Science、Melting point, 101.325 kPaの欄および脚注c2による。「c2 The melting point of water (cold --> hot) used to be defined as 0°C (32°F) under standard atmospheric pressure (101.325 kPa), but we now use the International Temperature Scale ( ITS-90). 0°C is now defined as 273.15 K but does not exactly equal the melting point of water, 273.152519 K.」
- ^ List of physicochemical data concerning water Water Structure and Science、Boiling point, 101.325 kPaのH2Oの欄および脚注c1による。「c1 The boiling point of water used to be defined as 100°C (212 °F) under standard atmospheric pressure (101.325 kPa), but we now use the International Temperature Scale ( ITS-90) where the boiling point is about 99.9743°C for VSMOW a . The boiling point and critical point on the thermodynamic temperature scale have been estimated at 99.9839°C and 647.113 K respectively [469].」 熱力学温度における沸点は、99.9839 ℃ と見積もられている。なお、熱力学温度(T)と国際温度目盛り(ITS-90)(T90)との差の見積もりについては、Estimates of the Differences between Thermodynamic Temperature and the ITS-90 Table 1 を参考のこと。
- ^ O. Mishima, L. D. Calvert, and E. Whalley, Nature 310, 393 (1984).
- ^ 『水分子はどうつながっている 100年前の「レントゲン説」脚光』「ナゾ謎かがく」日本経済新聞 2014年1月19日
- ^ 東大、液体の水の水素結合は「ミクロ不均一モデル」であることを確認マイナビニュース2013/11/13
- ^ 均一と考えられていた液体の水に不均一な微細構造を発見2009年8月11日 理化学研究所
- ^ Physical Review Letters
- ^ Proceedings of the National Academy of Sciences 2009-08-10
- ^ Kielh, J. T.; Trenberth, K. E. (1997). "Earth's annual global mean energy budget (PDF) ." Bull. Am. Meteorol. Soc. 78: 197 - 298 によると、温室効果のうち60%が水蒸気に由来する。第2位が二酸化炭素 (26%) である。
- ^ a b 環境保全対策研究会 編『二訂・水質汚濁対策の基礎知識』(8版)社団法人産業環境管理協会、2008年。ISBN 4-914953-41-2。
- ^ New Type of Alien Planet Is a Steamy 'Waterworld' - Space.com
- ^ Astronomers Find Largest, Most Distant Reservoir of Water - NASA
- ^ a b ニッスイ おいしさを科学する「水分」
- ^ 大森弘喜「19世紀パリの水まわり事情と衛生」
- ^ 「世界の水危機と第三回世界水フォーラム」 (PDF) p.12 「世界の水利用」
- ^ 東京都水道局
- ^ 独自の研究
* 生命維持のための摂取。植物は根などから吸収。動物は直接飲用または食物より摂取
- 冷却(熱交換、気化熱の利用) - エンジン・エアコンの水冷式、ラジエーター、かき氷、かち割り、冷却水、打ち水
- あたため・加熱(熱交換) - 入浴・温泉、サウナ、床暖房装置、蒸し料理
- 溶媒としての利用 - 点滴、水割り
- 摩擦(摩擦力)の軽減(特異な相転移の利用) - スキー、スケート
- 位置エネルギー・運動エネルギーの利用 - 水力発電、水車、波力発電、ししおどし
- 水蒸気(スチーム)の圧力の利用 - 蒸気機関、火力発電・原子力発電の蒸気タービン
- 水の粒を利用した映像作品やスクリーンとしての応用
- 重みをかけるため(重しとしての利用) - 船舶のバラスト水、ビーチパラソル・旗・のぼり・看板などの重し
- 消火剤 - 消火栓、消防用水[要出典]
参考文献
- 山田仁史・永山ゆかり・藤原潤子(編) 『水・雪・氷のフォークロア:北の人々の伝承世界』勉誠出版、2014年 ISBN 978-4-585-22083-1
関連項目
- 海 - 海洋深層水
- 川 - 滝
- 湖 - 池 - 水たまり - オアシス
- 雨
- 地下水 - 井戸
- 水道 - 上水道 - 中水道 - 下水道
- 水質汚濁 - 地下水汚染 - 公害
- 水の危機 - 世界水会議、世界水フォーラム、アジア太平洋水サミット
- 仮想水
- ウォータースポーツ、潜水、水泳、古式泳法
- 打ち水
- ウォーターカッター
- 水筒
- 水分
- 水面
- 水毒
- セルシウス度
- 純水、超純水、軽水、重水
- 水蒸気、過冷却水、氷
- 硬水 - 軟水 - ミネラルウォーター
- 機能水
- ポリウォーター
- DHMO
- ムペンバ効果
- 電気双極子
- 水クラスター
- 水モデル
外部リンク
- 環境省水環境関係
- 国土交通省水資源
- Water Structure and Science、en:London South Bank University 水についてのあらゆる科学的情報が得られる。
- Water Properties (including isotopologues) 上記のHPのうち、水の性質についての一覧表
- Physical properties of water (英語) - Encyclopedia of Earth「Encyclopedia of Earth にある「水の物理的性質」についての項目」の項目。
- The Water Cycle:USGS米国地質調査所の水循環のページ。日本語訳あり。

