化学
化学(かがく、英語: chemistry ケミストリー、羅語:chemia ケーミア)とは、さまざまな物質の構造・性質および物質相互の反応を研究する、自然科学の一部門[1]。物質が、何から、どのような構造で出来ているか、どんな特徴や性質を持っているか、そして相互作用や反応によってどのように、何に変化するか、を研究するとも言い換えられる[2][3][4]。


日本語では同音異義語の「科学」(英: science)との混同をさけるため、化学を湯桶読みして「ばけがく」とよぶこともある[6]。
概説[編集]
化学は、自然科学の一部門であり、さまざまな物質の構造・性質および物質相互の反応を研究する部門である[5]。(少し異なった角度からの表現を紹介すると、)化学とは、物質についての学問(「物質の学問」)であり、(自然科学は自然に階層構造を見出すが)化学は自然の階層 の中で言えば、原子や分子という階層を受け持っている [7]、と筑波大学の齋藤一弥は説明した。日本の諸大学の化学科のHPなどでの解説も紹介すると、たとえば富山大学のHPでは、「化学とは、物質の性質を原子や分子のレベルで解明し、化学反応を用いて新しい物質(系)を作り出すことを設計、追求する学問分野である[8]」、と説明されている。
筑波大のサイトによると、化学という学問を定義づけすることは難しく、それを無理に規定する意義もあまりない。化学は「理学」に含まれるが、数学・物理学あるいは生物学などの、自然科学の中で基礎科学または純粋科学にあたる他の「理学」と化学の相違点は、化学は有限な元素が組み合わさった無数の物質がもつ多様性を取扱い、さらに化学そのものが新たに物質を創造する役割を担う[7]、という点である。[9]。化学という学問領域が取り扱う物質は、特に化学物質が中心となる[2]。化学物質は原子・分子・イオンなどが複雑に絡み合いながら作られるため膨大な種類にわたり、その全てを含む壮大な物質世界・生命世界が対象となる[10]。それゆえ化学は、基盤科学と定義づけられる。物質を分子やその集合体の大きさ単位で扱う化学は基礎的であるがゆえに、関連する学問は、理学や工学から医学・薬学、農業・環境分野など多岐にわたる上、特に近年に生物工学(バイオテクノロジー)や電子工学(エレクトロニクス)、新素材や高機能材料など現代科学の最先端技術に新物質や設計・製造の新手段を発明する上で欠かせないものとなっている[10]。
原則的に近年の化学では、全ての物質が原子からできているとの仮説[11](あるいはフレームワーク)を採用し、物質の性質は原子自体の状態や、原子同士の結びつきかた(化学結合)で決定されると考える[注 1]。したがって、繰り返しになるが、基本的に現代の化学は、原子・分子レベルでの物質の構造や性質を解明して、また新しい物質や反応を構築して[10]、「物質とはなにか」に関する知見を積み上げる学問である[7]。
化学は典型的な蓄積型の学問である。取り扱う物質の種類は増える一方で、1980年代には600万種を越え、しかも年平均1000種が追加されていた[12]。これらは基本的に減ることは無いため、それに関する情報は増加の一途をたどる。数世紀前の実験で得られた基礎的なデータですら(間違いでない限り)重要性を失わない。同様に古典的な方法論も最新の量子論的手法と同じくらい高い価値を持つ。[10]
しかしながら、学問としての化学の成立は遅い。数学、物理学、天文学などが2000年前の古代ギリシアで構築され始めたのに対し、科学の一分野として扱うことができる近代的化学のほうは、18世紀末にフランスのアントワーヌ・ラヴォアジエ(1743年 - 1794年)の質量保存の法則(1774年発見)[13]やジョン・ドルトン(1766年 - 1844年)の原子説[11]が正しい方向付けをした[4]事に始まってから、まだ200年程度しか経過していない[13](#歴史、化学の歴史も参照)。これは近代物理学の最初の到達点であるニュートン力学が『自然哲学の数学的諸原理』(プリンキピア)に書かれた年(1687年)と比べ、化学の興隆が100年程度時代が下ることを意味する。
その短い歴史の中で、化学は大きな末広がりの構造を持つに至った。化学の基礎的な部分はほとんど固められ、根底から転換がなされる余地はほとんど無い。ところが、物質に対する理解が進み、応用が広がる中で化学が担う役割はほとんど全ての生産・製造に深く関わるようになった[10]。さらに、弱い相互作用を重視した新しい物質像の構築や、自然との調和を実現するための環境化学など、近年になって化学はさらに広がりを見せつつある[15]。
化学で扱う基本的なこと[編集]

原子の種類と構造[編集]
化学では、物質の基本単位を原子として、その原子が持つさまざまな性質を抽象的概念である「元素」[17]として把握する。原子論が確立した現代では、その特徴を理論的に掴む上で、原子核(陽子・中性子)および電子までの原子の構造から原子番号、質量数、電気素量、イオン、同位体などを決定し取扱い、各元素が持つ性質を理解する。[18]
原子が持つ周期的性質(周期律)は初期の化学が発見した一大成果である[19]。この物理的性質の近似を生む要因である電子配置から、各元素のイオン化エネルギー、電気陰性度、酸化数、原子半径やイオン半径などの特徴が理論づけられる[20]。この周期律を簡略な表にまとめた周期表は化学のバイブルとまで呼ばれる[19]。
元素の性質を記述することは、化学の中でも量子力学と統計力学が取り扱う。周期律は、量子力学の成立をもって初めてその本質が明瞭になった[7]。原子内の電子配置はボーアの原子模型では限界がある[21]ので、波動力学のパウリの排他原理や波動関数[22]、そして電子のエネルギー準位で説明される[20]。統計力学は、物質の状態(三態)や性質などを巨視的に理解する上で必須の方法論を提供し、実験の結果をもたらす上で大きな役割を持つ[7]。
化学結合[編集]
物質は原子から構成されるが、その原子が結びついて分子をつくる。この結び付きを化学結合と呼び、これを理解することで化学は発展してきた[23]。
19世紀以前、原子間の結びつきは化学反応を説明するために考えられた。基礎的な概念に当たる化学親和力や、続く電気化学的二元論や原子価が提唱されたが、それでも一部の結合しない原子の組み合わせを説明できなかった[24]。20世紀に入りドイツのヴァルター・コッセル(en)がイオン結合を理論化し、それでも解釈不能な水素分子など無極性分子の説明にアメリカのギルバート・ルイスとアーヴィング・ラングミュアがそれぞれ独立に共有結合の概念を提案した[25]。量子力学は分子構造論も深化させ、二原子分子の安定を説明した交換相互作用、分子軌道や原子軌道を明らかにした波動関数[26]、金属結合の実際を自由電子モデルから進めたバンド理論[27]などをもたらした。
分子の構造[編集]
分子は、その物質が持つ特性を維持したまま分割できる最小の単位と言える[28]。静電気力で結合するイオン結合には方向性が無いが、共有結合は異方性がある。簡単な共有結合分子は原子価殻電子対反発則で説明され、これに電子軌道の考え方を加えれば、分子やイオンの構造についての理論的根拠になる[29]。
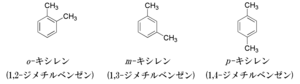
その一方で、同じ種類と数の元素が組み合わさった分子でも、その構造で物性に差があることが判明している。不斉炭素原子と共有結合する4つの原子団が結合する位置の違いから生じる光学異性体や立体異性体や、また炭素などの二重結合部分が回転しないために生じる幾何異性体などは、同一の構造式でありながら異なる性質を持つ分子となる。ベンゼン環に結合する置換基の位置(オルトなど)による構造異性体も一例に当たる[30]。エタン類など回転が可能な分子においても、立体障害などによる特性の差異は生じる[30]。さらに近年では知恵の輪のようなカテナンやサッカーボールもどきのフラーレンなど、風変わりな構造を持つ分子も発見されている[31]。

物質の状態[編集]
原子や分子がある程度の量あつまると、特徴的な性質をもった集団を形成する。これを相といい、大きく分けて固体、液体、気体(物質の三態)などがある[32]。閉鎖系において物質がこれらの相を取るには温度と圧力が影響し、ギブズ相律という法則に則った状態を取る。これは物質ごとに相図というダイアグラムで示される[32]。
気体は反応に乏しく、体積や圧力など物理的性質や変化などを中心に扱う。しかしそれらのマクロ的なふるまいは、気体では分子が単独で存在する、というミクロな分子の構造や性質に由来する[33]。なお、気体が電離した状態であるプラズマについても、プラズマ化学という分野で取り扱う[34]。
液体は分子間力の点から気体と固体の中間にある。加熱や冷却によって気化・蒸発や凝固など相の変換を起こす。これは化学における重要な物質生成手段である蒸留にかかわる[35]。また、2つ以上の成分でできた液体、溶液に関して化学では、溶媒と溶質による分散系の性質、浸透圧や粘度また表面張力・界面張力なども扱う[36]。
固体は基本的に原子が規則的に配列する結晶と、規則性に乏しく固体と液体の中間とも言えるアモルファス(非晶質)に分けられる[37]。結晶質は複数の結晶構造いずれかを取り、その性質を特徴づける[38]。また、粒子の種類や力から分類される結晶には、金属結晶・イオン結晶・分子結晶・共有結合結晶などがある[39]。結晶構造を持ちながら液相的性質を持つ物質は液晶と呼ばれ、一部にベンゼン環のような平面の構造を持つ共通点がある[39]。
化学反応[編集]
複数の物質に混合・必要があれば加熱・冷却などの操作を加えると、異なる化合物ができる。これを化学反応と呼ぶ。化学反応は物質を構成する原子間の化学結合の変化によって起きる。化学反応の前後では全体の質量は変わらない。これを質量保存の法則(あるいは物質不変の法則)という。化学反応は、自然界において基本的には、ある種の自由エネルギーを最小化するほうへ向かって、エネルギーが低い位置へ向かう発熱反応と、より乱雑になろうとするエントロピーの増大という相反する反応を起こしながら、平衡に達する。化学では、これら反応の法則性や利用法の解明が課題となる[40]。
水溶液の性質を知る手段として体系づけが始まった酸と塩基(塩が加水分解したもの)の関係は、化学では重要な項目となる[41]。主に水に溶ける物質の性質分類が行われ、水溶液以外の状態も考慮して[42]、
と定義される。この2つは重要な化合物の組である。互いに相反し中和を起こさせながら化学平衡し、水素イオン指数など溶液の性質を決める。
燃焼や金属製錬および腐食などの本質は酸化と還元で説明される。酸と塩基が反応の窓口となる電子対が原子と一体になっているのに対し、酸化と還元は電子が単独で動き反応を起こす[43]。そのため、酸化還元は電圧と密接に関係し、電流を生じさせる機構の基本的な原理に当たる[43]。還元の代表的な用途は卑金属の精製であり、酸化は生化学において重要なクエン酸回路に見られる。
化学合成は、単純な物質から化学反応を用いて複雑な、または特定の機能を持つ物質を生成することを指す。分子量の小さな物質をつなぎ合わせて高分子を作る化学合成の代表例には重合反応がある。これは化学工業の主要なプロセスである。機能を持たせる化学合成の例は医薬品製造やナノテクノロジーなどである。このような製造に関わる化学合成では、適切な製品を効率良く作り出すことが求められ、化学の分野としては触媒や不斉合成など[40]が研究される。
主な化学の分野[編集]
諸分野の役割[編集]
化学には、研究手法や対象とする物質の違いによって多くの分野が存在する[2]。しかし、各分野間には関連領域が存在するため明確に区別することは難しい。以下に例として代表的なものを挙げる。
- 物理化学
- 物理化学は物理学的な理論や測定方法、例えば熱力学や量子力学的な手法や視点から化学が対象をする物質を研究し、物質やその性質および反応を分類する上で基準を作り、そして分類する[7]分野である[44]。ヴァルター・ネルンストが著述『理論化学』(Theoretische Chemie、1893年)で唱えた理論化学もほぼ同じ概念である[45]。また、コンピュータの進歩に伴い、理論式から計算によって物質の状態を予測する量子化学や計算化学も急速に発展している[46]。物理化学の方法論で生物を対象に行われる研究は生物物理化学であり[47]、これをコンピュータによる仮想的な体系でシミュレートする人工化学も提唱されている[48]。
- 無機化学
- 無機化学は、有機化合物を除くすべての物質、すなわち単体と無機化合物を対象とする広い分野である[49]。広義には、錯体を扱う錯体化学、生体内の無機物を扱う生物無機化学(または無機生化学)、鉱物化学や地球化学、放射化学、有機金属化学などと境界領域を共有する場合がある[49]。
- 有機化学
- 有機化学は、有機化合物を扱う分野である[50]。元々は動物や植物など生物体の組織(有機体)を構成する物質を対象として始まり、後に有機体以外から生成される有機化合物も対象に含まれて体系化された[50]。無機化学の分野とは相互補充する関係にある[49]。多様な反応をするため、専門的な分野として特化している。有機合成化学目的の有機化合物を得るために合成系列や反応方法などを創案する分野である[51]。薬学とも密接なかかわりがある。生物学との境界分野は生物有機化学と呼ばれる。有機化合物の構造と性質の関係を研究する分野は有機構造論、特に立体構造に着目する領域は立体化学に分けられる[50]。天然には存在しない物質を合成して繊維や高分子材料を製造するための研究は有機工業化学と呼ばれる[50]。
- 高分子化学
- 高分子化学は、分子量が1万から数百万にまで及ぶような非常に大きな分子である高分子を取り扱う分野であり、その化合物は有機・無機の両方を対象とする[52]。しかし実際には有機化合物を取扱う割合が高い[52]。合成方法だけではなく、機械的性質や熱物性なども研究対象としている。高分子の材料としての重要性から、工業とのつながりが非常に強い。
- 生化学(生物化学)
- 生化学または生物化学[53]は、生物や生命現象を化学的な理論や実験手法を導入して研究する分野であり[54]生物学と化学の両方にまたがる領域である。酵素の研究を軸に[54]ホルモンなどのタンパク質や糖、核酸、脂質などの生体内の物質群や、生体のエネルギー獲得や輸送および代謝機能などを扱うことが多い[54]。生体高分子を扱うことが多いため高分子化学とも関連する。生命現象を分子単位で研究する分子生物学や分子遺伝学を含み、遺伝子工学などに応用される[54]。また、組織化学とは細胞など組織中の特定物質が分布する状況を、化学反応を用いて染色させ判断する技術を言い、免疫組織化学もそのひとつに含まれる[55]。衛生化学とは、物質が生体に及ぼす影響を研究する、予防薬学分野の応用に当たる分野である[56][57]。
- 分析化学・機器分析有機化学・有機合成化学
- 分析化学や機器分析化学は、様々な物質を測定したり分離したりすることを目的とした実験や理論を研究する分野である[58]。中でも機器分析化学は、分析化学の中で分析機器を用いた研究分野である。応用性が強く、実験室レベルの基礎化学から工業生産物・臨床検査など幅広い範囲を対象とし[58]、食品や薬品、農業、工業などさまざまな分野で重要な役割を担っている。合成化学は、存在できる物質を知る分野であり[7]、化学反応を用いて実際に物質を作り出すことを研究・開発する[59]分野であり、触媒化学や材料化学を含む[7]。
- 応用化学
- 応用化学は、生産に関わるさまざまな技術や工程で用いられる物質や反応などを研究する分野であり、生産する種類によって工業化学、農芸化学、薬化学などに細分化される[60]。狭義では原料を化学製品へ転換し、目的の物質を得る上で必要な一連の方法を対象とする分野である工業化学を指し、日本では工学の一分野として応用化学と工業化学は同義にて用いられることが多い[60][61]。工業化学では、新しい反応や触媒の探求からプラントの設計まで、実用上必要とされる幅広い事柄を取り扱う。一方で、日本の大学に設置されている化学科と応用化学科(生命科学部生命科学科・応用生命科学部応用生命科学科)の教育内容に違いはほとんどない[62]。
- 環境化学
- 環境化学は、環境(地球ならば水圏、大気圏など)における化学物質の生成、反応、移動、影響や成り行きなどを研究する分野であり[64]、これらが生物圏に与える影響(環境問題)を化学的に説明する[65]。地球環境化学はこのような研究を地球規模の環境に対して行う分野である[66]。
諸分野が対象とするもの[編集]
上にあげた化学の各分野を、取り扱う対象で分類する。本項は、特に脚注がある部分を除き、筑波大学数理物質科学研究科教授・齋藤一弥の分類を出典とする[7]。
原子核を中心に、原子核反応やそれによって合成される新元素およびその性質を取り扱う分野が核化学や放射化学であり、特に後者では放射能の測定において分析化学的な方法も利用される。
単体の分子を取り扱う分野では、量子力学や計算科学の理論および測定を用いる量子化学や、光を調査の手段に用いる物理化学の領域に含まれる分子分光学があり、無機・有機の両方を含み化合物を扱う合成化学もこの範疇に入る部分が多い。
化学反応を研究する分野には、反応機構を取り扱う化学反応論、反応速度をコントロールする手法を研究することを目的とした触媒化学などがある。合成化学では、反応機構を研究したり、新しい化学反応を創造する分野はここに含まれる。熱化学も反応における平衡や熱を扱う。
分子の集まりを扱う分野は、その全体構造や分子の運動について研究する構造化学や、目に見える物質としての分子集合体について分子の持つ性質から物性を説明する分野である物性化学などがある。高分子化学は特に分子量の大きな分子の集まりに見られる特殊な性質を研究の対象とする。同じ高分子に相当するが特殊なものと言える生物・生命を化学的に扱う分野が生化学、生物化学である。
物質の表面に着目し、その構造や現象などを研究する分野には表面科学や界面化学がある。これらは、固体の触媒を使用する際の触媒化学とも関連する。コロイドが持つ特徴的な性質を理解する分野はコロイド化学と呼ばれる。
環境をマクロな視点で把握し、それが地球規模の大きな化学システムとして研究する分野が環境化学である。そして、自然現象や人間活動がこのシステムにどのような影響を与えるか、人工の物質が環境に拡散しどのような事態が起こるかなどを取り扱う[67]。
歴史[編集]

炎は有機物の酸化反応によって放出される熱エネルギーの現れであるので、化学の歴史は人類が火を扱いはじめたときから始まっているとも考えられる[68]。金や銀以外の金属は、自然界において酸化物ないしは硫化物として産出されるので、古代人は還元反応を知らないまま青銅器・鉄器などを製造する金属精錬をしていた[68]。
化学は古代エジプトに起源があると言われる。エジプト語で黒を意味する「chémi」がヨーロッパに伝わった化学を表す用語となり、化学は「黒の技術」とも呼ばれた[2]。古代ギリシアにおける学問の発展は、タレスの元素論に始まりアリストテレスらにより大成された[68]。
これらの系統とは別に、中国、アラビア、ペルシア等でも独自に化学技術が勃興した[2]。このうち、イスラム科学では錬金術へと発展し、中世ヨーロッパにおいて天文学、数学、医学と同様にラテン語に翻訳された[69]。金を他の物質から作ろうとする錬金術が盛んになり、様々なものを混ぜたり加熱したりすることが試みられた。結局、錬金術は不可能な前提の上で行われた徒労[13]に終わったが、その副生物として各種薬品が生み出された。これらが化学のいしずえとされる[2][70]。ただし、錬金術は秘密主義や拝金主義、そして定量的な技術を持たなかった点から、逆に化学発展の阻害になったという主張もある[71]。
17世紀以降、化学は近代的な方法論に則った発展を始め[2]、18世紀末頃から実験を通じて化学反応を定量的研究で解釈するようになり[2]、19世紀に入ると原子・分子の組み換えが化学反応の本質であることが理解されるようになった[2]。しかし、化学反応の中心原理が何であるかは、物理学が原子の成立ちを解明するまで待つ必要があった。すなわち19世紀後半に展開した原子核と電子に関する物理学がもたらしたアーネスト・ラザフォードの原子核モデルが[42]、化学反応が原子と電子の相互作用に基づくことを解明した。
また20世紀に入ると、化学結合の性質が量子力学で支配される電子の挙動(分子軌道やエネルギー準位)に起因することが理解され[42]、これが今日の化学の中心原理となる理論体系が構築された[2]。とはいうものの、今日において物理学の根本が量子論・相対論の時代であってもニュートン力学の価値がいささかも失われていないように、近代に確立した化学当量、オクテット則や酸化数あるいは有機電子論などの古典化学理論は、今日的な意味を失うものではない。
他また、有機化学と高分子化学も20世紀に発展を遂げ、一方では生物学との境界において多大な進歩をもたらし[2]、生物学を全く新しいものとした。もう一方ではそれまで存在しなかった様々な物質が合成され、工業社会の大きな発展の元になり、同時に公害問題などにも深く関わるようになった[12]。

日本における歴史[編集]
幕末から明治初期にかけての日本では、化学は舎密(セイミ)と呼ばれた。舎密は化学を意味するラテン語系オランダ語 Chemie (この単語自体の意味は「科学」)の音訳である[72]。
日本で初めての近代化学を紹介する書となったのは、江戸時代の宇田川榕菴の『舎密開宗』(せいみかいそう)である。原著はイギリスの化学者ウィリアム・ヘンリーが1801年に出版した An Epitome of Chemistry である。宇田川榕菴はこれらの出版に際し、日本語のまだ存在しなかった学術用語に新しい造語を作って翻訳した。酸素、水素、窒素、炭素といった元素名や酸化、還元、溶解、分析といった化学用語は、宇田川榕菴によって考案された造語である[73]。
「化学」という単語は川本幸民が著書『化学新書』(1861年)で初めて用い、後に明治政府が正式に採用した。これは、他の学問用語と同様に日本から中国などへ伝わった和製漢語の一つとされていたが[74]、近年では中国語からの借入語であるとされている[75]。中国では、「化学」という単語は墨海書館が発行した月刊誌『六合叢談』の1857年の号が初出である[76]。一般には、中国語の単語「化学」は徐寿がイギリスの専門書『化学鑑原』(1871年)を翻訳する際に造ったと信じられてきた。
学会組織[編集]

世界のほとんどの国では、化学の専門教育は大学を中心とした機関が担っている。その中でも理学部系の化学科や専攻は基礎的な領域を、工学部系では応用的な部分を扱うことが多い。薬学部や工学部の材料工学科などは専門性が高くなる[7]。
研究者を横断的に繋げる学会も組織され、日本では日本化学会が全体を網羅する。研究分野ごとには化学工学会や高分子学会などの化学系学会があり、大学や企業の研究者らが加わっている[7]。アメリカ化学会は、多様な化学物質のデータベース整備を1907年から行っており、近年ではインターネット上でアクセス可能な「Chemical Abstracts」を公開している[7]。
国際的な学会連合は国際純正・応用化学連合 (IUPAC) が組織され、単位や記号の世界統一に関する勧告や取り決めなどを行ったり、他の科学組織との協議を行う母体となっている[7]。
脚注[編集]
注釈[編集]
- ^ 化学という学問を離れると、必ずしもこの仮説だけで説明しているわけではなく、(化学ではない)物理学・素粒子物理学などでは、物質の定義に、(原子や分子よりもはるかに小さな)レプトンやクォーク、ニュートリノなども加えた仮説を構築している。高エネルギー物理学・素粒子物理学/東京大学理学部物理学科・大学院理学系研究科物理学専攻。
出典[編集]
- ^ 広辞苑 第五版 p.457
- ^ a b c d e f g h i j k 岩波理化学辞典 (1994)、p207、【化学】
- ^ 早稲田大学のHPに掲載されている文章。「化学とは、様々なモノが何からできているのか、どんな性質を持っているのか、あるいはあるモノから別のモノへどのように変化するのかを調べる学問です。」“Outline”. 早稲田大学理工学術院先進理工学部・研究科 応用科学科. 2010年11月27日閲覧。[リンク切れ] 既存の定義文をもとにして、HP向けのやわらかい表現に改変したもの。
- ^ a b 糸山東一「一般化学の授業内容についての一試論」『香川大学一般教育研究』第19巻、香川大学一般教育部、1981年3月、49-63頁、CRID 1050006297347951360、ISSN 03893006、2023年11月29日閲覧。
- ^ a b 広辞苑 第五版 p.457
- ^ “日本語なんでも相談室”. 北海道文教大学日本語コミュニケーション学科. 2023年4月28日閲覧。
- ^ a b c d e f g h i j k l m 齋藤一弥 (2010年). “1.化学という学問” (PDF). 筑波大学大学院数理物質科学研究科物質創成先端科学専攻. 2010年11月27日閲覧。 p.5
- ^ 「化学とは、その一大特徴である化学反応により新しい物質(系)の創成を設計・追求し、それらの性質を原子や分子のレベルで解明する学問分野である。“応用化学大講座”. 富山大学大学院理工学教育部. 2010年11月27日閲覧。」
- ^ M. G. Finn; Hartmuth C. Kolb; Valery V. Fokin「クリックケミストリーの概念と応用:提唱者の立場から」(PDF)『化学と工業』第60巻第10号、日本化学会、2007年10月、976-980頁、CRID 1520853833920955776、ISSN 00227684、NAID 10019960594、2023年11月29日閲覧。
- ^ a b c d e 竹内 (1996)、pp.v-viii、化学入門コースの読者へ
- ^ a b 岩崎允胤「化学反応と物質構造の問題」『北海道大學文學部紀要』第19巻第1号、北海道大學文學部、1971年3月、71-93頁、CRID 1050564288949657088、hdl:2115/33347、ISSN 04376668、2023年11月29日閲覧。[14]
- ^ a b 杉浦ら (1987)、p.1
- ^ a b c 竹内 (1996)、1.原子論の成立、pp.2-6、1.1.化学の始まり
- ^ フリードリヒ・エンゲルス、『自然弁証法』第2冊、訳:菅原仰、寺沢恒信、p.158
- ^ 竹内 (1996)、14.21世紀の化学、p.247
- ^ 竹内敬人 『化学入門コース 化学の基礎』 岩波書店、1996年、第1刷。ISBN 4-00-007981-6。pp.78-79
- ^ ニュートン別冊 (2010)、pp.12-13、原子と元素はどうちがうのか
- ^ 竹内 (1996)、pp.6-10、1.2 物質の構成要素
- ^ a b 竹内 (1996)、5.元素の周期的性質、p.75
- ^ a b 竹内 (1996)、pp.83-91、5.2 単体の性質の周期性
- ^ 竹内 (1996)、pp.23-29、2.3 古典量子論の成立
- ^ 竹内 (1996)、pp.30-39、2.4 量子力学の成立
- ^ 竹内 (1996)、3.化学結合、p.41
- ^ 竹内 (1996)、pp.42-44、3.1 20世紀以前の化学結合論
- ^ 竹内 (1996)、pp.45-48、3.2 ボーア模型に基づく化学結合論
- ^ 竹内 (1996)、pp.49-53、3.3 量子力学的結合理論
- ^ 竹内 (1996)、pp.53-55、3.4 その他の結合
- ^ ニュートン別冊 (2010)、pp.16-17、分子はその物質の特性を持つ最小の粒子
- ^ 竹内 (1996)、pp.58-63、4.1 簡単な化合物の構造
- ^ a b 竹内 (1996)、pp.63-70、4.2 炭素化合物の構造
- ^ 竹内 (1996)、4.分子の形 p.74
- ^ a b 竹内 (1996)、pp.120-121、7.3 相平衡と相律
- ^ 竹内 (1996)、p.99、6 気体
- ^ “キーワード一覧”. 独立行政法人 日本学術振興会. 2010年11月27日閲覧。
- ^ 竹内 (1996)、p.113、7 液体
- ^ 竹内 (1996)、pp.121-130、7.4 溶液
- ^ 竹内 (1996)、pp.134-135、8.1 結晶質とアモルファス
- ^ 竹内 (1996)、pp.135-142、8.2 結晶の構造
- ^ a b 竹内 (1996)、pp.142-151、8.3 さまざまな結晶
- ^ a b 大川 (2002)、pp117-138、自然界のバランス感覚
- ^ 大川 (2002)、pp138-162、非なりて似たるもの‐酸と塩基
- ^ a b c 大川 (2002)、pp27-55、それは古代ギリシアに始まった
- ^ a b 大川 (2002)、pp163-194、電子は陰の立役者‐酸化と還元
- ^ 岩波理化学辞典 (1994)、p.1108、【物理化学】
- ^ 岩波理化学辞典 (1994)、p.1378、【理論化学】
- ^ 関山秀雄. “量子化学, 計算化学とは”. 静岡理工科大学物質生命科学科. 2010年11月27日閲覧。
- ^ 今井弘康. “授業の目的”. 北陸大学薬学部SYLLABUS. 2010年11月27日閲覧。[リンク切れ]
- ^ 小泉和真, 冨永和人「人工化学のための自動推論器の構築」『情報処理学会研究報告バイオ情報学(BIO)』第2007巻128(2007-BIO-011)、2007年12月21日、93-96頁、2022年3月1日閲覧。
- ^ a b c 岩波理化学辞典 (1994)、p1271、【無機化学】
- ^ a b c d 岩波理化学辞典 (1994)、p1301、【有機化学】
- ^ 市川淳士. “有機合成化学‐分子変換をいかにして行うか‐”. 筑波大学大学院数理物質科学研究科化学専攻. 2010年11月27日閲覧。
- ^ a b 岩波理化学辞典 (1994)、p436、【高分子化学】
- ^ 岩波理化学辞典 (1994)、p681、【生物化学】
- ^ a b c d 岩波理化学辞典 (1994)、p672、【生化学】
- ^ 宮澤正顕. “免疫学Q&A”. 近畿大学医学部免疫学教室. 2010年11月27日閲覧。
- ^ 福井哲也. “「衛生」とは「生を守る」こと。病気にならないために、食品や環境因子のはたらきに注目!”. 星薬科大学衛生化学教室. 2010年11月27日閲覧。
- ^ “学校法人東邦大学 研究科の専攻の設置「衛生化学特論」” (PDF). 文部科学省高等教育局高等教育企画課大学設置室. pp. 12. 2010年11月27日閲覧。[リンク切れ]
- ^ a b 岩波理化学辞典 (1994)、p1155、【分析化学】
- ^ 藤岡弘道. “分子合成化学分野” (PDF). 大阪大学大学院薬学研究科・薬学部. 2010年11月27日閲覧。
- ^ a b 岩波理化学辞典 (1994)、p.171、【応用化学】
- ^ 岩波理化学辞典 (1994)、p417、【工業化学】
- ^ “化学科、応用化学科、材料工学科、化学工学科の違い(学部生、高校生向け)”. 2019年10月19日閲覧。
- ^ 1991, Manahan, Stanley E., Environmental Chemistry, 5th Ed., Lewis Publishing, Chelsea, MI
- ^ Randolph Larsen. “Environmental chemistry” (英語). The Encyclopedia of Earth. 2010年11月27日閲覧。[リンク切れ][63]
- ^ 一色健司. “環境化学”. 高知女子大学. 2010年11月27日閲覧。[リンク切れ]
- ^ “授業内容・計画(概要)の情報”. 東海大学理学部化学科. 2010年11月27日閲覧。[リンク切れ]
- ^ J.E.アンドリューズ、P.ブリンブルコム、T.D.ジッケルズ、P.S.リス、B.J.リード 著、渡辺正 訳「1-4、人間は生物地球化学サイクルを変える?」『地球環境化学入門』シュプリンガー・フェアラーク東京、11-13頁。ISBN 4-431-71111-2。
- ^ a b c アシモフ (1967)、pp.009-026、第1章 古代
- ^ アシモフ (1967)、pp.027-049、第2章 錬金術
- ^ ニュートン別冊 (2010)、pp.80-81、化学のいしずえを築いた錬金術
- ^ 村田徳治「1-3、化学の進歩を遅らせた錬金術の秘密主義」『化学はなぜ環境を汚染するのか』環境コミュニケーションズ、2001年、11-14頁。ISBN 9784874891377。
- ^ “稀書と大学歴史資料展1”. 龍谷大学展示室. 2010年11月27日閲覧。[リンク切れ]
- ^ 『江戸の化学 (玉川選書)』玉川大学出版部、1980年、54-62頁。ISBN 978-4472152115。
- ^ 関崎正夫「マッチと清水誠:日本で初めてマッチの国産化をした人」『金沢大学サテライト・プラザ「ミニ講演」講演録集』、金沢大学大学教育開放センター、2006年、hdl:2297/3804、2019年10月16日閲覧。
- ^ 陳力衛「和製漢語と中国語」『比較日本学教育研究センター研究年報』第8巻、お茶の水女子大学比較日本学教育研究センター、2012年、217-222頁、hdl:10083/51908。
- ^ 沈国威 (2000). “译名“化学”的诞生”. 自然科学史研究 19 (1): 55-71. オリジナルの2013-07-31時点におけるアーカイブ。.
参考文献[編集]
- 編:久保亮五、長倉三郎、井口洋夫、江沢洋『岩波理化学辞典』(第4版第9刷)岩波書店、1994年。ISBN 4-00-080015-9。
- 竹内敬人『化学入門コース 化学の基礎』(第1刷)岩波書店、1996年。ISBN 4-00-007981-6。
- 杉浦俊男、中谷純一、山下茂、吉田壽勝『化学概論‐物質科学の基礎‐』(第1版)化学同人、1987年。ISBN 4-7598-0159-6。
- アイザック・アシモフ 著、玉虫文一、竹内敬人 訳『化学の歴史』(第1刷)ちくま学芸文庫、2010年。ISBN 978-4-480-09282-3。
- 編集長:水谷仁『ニュートン別冊周期表第2冊』ニュートンプレス、東京都渋谷区代々木2-1-1新宿マインズタワー、2010年。ISBN 978-4-315-51876-4。
- 大川貴史『高校化学とっておき勉強法』(第1刷)講談社、2002年。ISBN 4-06-257356-3。
関連項目[編集]
外部リンク[編集]
- (英語)SciFinder - Chemical Abstracts Service (CAS) が公開する化学物質データベース
- 『化学』 - コトバンク
