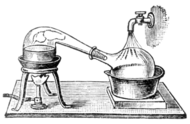
蒸留
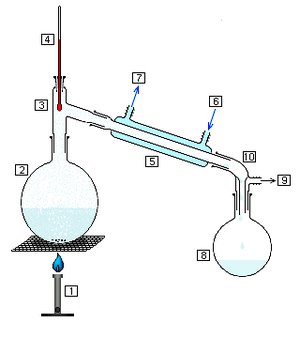
蒸留(じょうりゅう、蒸餾、蒸溜、英: Distillation)とは、液体を加熱して、出てくる気体を冷やして再び液体にして集める方法をいう。一般に、混合物を一度蒸発させ、後で再び凝縮させることで、沸点の異なる成分を分離・濃縮する操作で利用されることが多い。この場合は、通常、目的成分が常温で液体であるか、融点が高々100℃程度の固体の場合に用いられる。共沸しない混合物であれば、蒸留によりほぼ完全に単離及び精製することが可能であり、この操作を特に分留という。
原理[編集]
原理的には、蒸留とは物質ごとの蒸気圧の差を利用して混合物の特定成分を濃縮する操作である。蒸留したい混合物を加熱していくと、液面から各成分が徐々に蒸発していく。各成分の蒸気圧の和が系の圧力と一致すると沸騰が始まる。そのとき、発生する蒸気の組成はラウールの法則に従い、液面の成分組成と、その温度での各成分の蒸気圧(分圧)の両方から決定される(この平衡状態での気相あるいは液相の成分比と温度の関係をプロットした図を気液相関図と呼び、蒸留の濃縮過程がシミュレートできる)。この蒸気を冷却・捕集すると、通常は温度が低いうちは低沸点成分の比率が高く、温度を上げるにつれ高沸点成分の比率が増すような蒸留物が得られる。これを繰り返すことで、目的成分の濃度を上昇させることができる。
このように蒸留物の組成は蒸発と凝縮の温度依存性に従うため、沸点差が大きいだけでは一定以上の濃縮は期待できない。例えばエタノール-水系の蒸留の場合は、エタノールは約96%w/w以上には濃縮されない。この現象を共沸と呼び、共沸をおこす混合物を共沸混合物という。言い換えれば、水(沸点100℃)はエタノール(沸点78.3℃)と共沸し、このときの沸点(共沸点)は78.2℃で、このときに得られる蒸留物の組成(共沸組成)は水:エタノール=4:96 (w/w)である。 2成分からなる共沸混合物の場合は、第3の共沸成分を追加して目的の成分を分留できることがある。例えば、ベンゼン(沸点80℃)は水と共沸し(共沸点69℃、共沸組成、水:ベンゼン=9:91, w/w)、またエタノールとも共沸するが(共沸点68℃、共沸組成、エタノール:ベンゼン=32:68, w/w)、水-エタノール-ベンゼンの3成分系の場合には、新たな共沸が見られる(共沸点65℃、共沸組成、水:エタノール:ベンゼン=7:19:74, w/w/w)。純度99.5%w/w以上のエタノールは、これを利用して、純度95%w/wのエタノールにベンゼンを追加して分留し、3成分の共沸混合物として水を除去して得られる。ただし、このようにして得られた無水エタノールは微量成分として発癌性のあるベンゼンを含むので飲用することはできない。また、ベンゼンに紫外吸収があるのでスペクトル用の溶媒としても適当でない。ベンゼンを含まないエタノールを得るためには、脱水剤(無水硫酸銅CuSO4、酸化カルシウムCaO、水素化カルシウムCaH2、モレキュラーシーブス3Aなどを使用する、マグネシウムエトキシド(粉末金属マグネシウムと「種」となる無水エタノールから作る)と還流して脱水するなどの方法が用いられ、またベンゼンの代わりに水とエタノールを含む3成分系の共沸混合物をつくる溶媒(ヘキサン、シクロヘキサンなど)を追加して蒸留するなどの手段も考えられる。
精留[編集]
蒸留により成分を精製する操作は(せいりゅう、英: rectification)と呼ばれている。多くの場合、精留を目的に蒸留操作がなされるため、広くは蒸留と同義である。石油精製のための精留を特に(ぶんりゅう、英: fractional distillation)と呼ぶ。[1]
精留を行うには、蒸留装置の塔部で凝縮液と蒸気とを向流接触させる必要がある。この際、凝縮熱により液の蒸発と分縮が繰り返されることで成分の濃縮が行われる。(記事 気液平衡に詳しい)
実際の蒸留では、ビグリューカラムなど、蒸留塔と呼ばれる装置を使用することも多い。蒸留塔は上記の蒸発-凝縮の平衡状態が多段階で進行するように設計されており、凝縮と蒸発を繰り返すうちに蒸気の組成比が変化し、特定成分の濃縮が進行するようになっている。
前述の気液相関で示されるように、蒸気温度が一定であればその組成も一定である。したがって、通常は蒸気温度が一定になったところを捕集し、それを(ほんりゅう)と呼ぶ。見方を変えると、初めのほう(初留)と、終わりのほう(後留)は蒸気温度が一定でなく、組成が変動し、結果として副成分が多く含まれる。初留と本留とを分取するためには二又アダプターなどを使用する。
蒸留酒の製造において、初留分は(はつだれ、はなたれ、英: head)、中留分は(ほんだれ、英: heart)、後留分は(すえだれ、英: tail)と呼ばれる。初留分には低沸点の香気成分がより多く含まれ、エタノールも高濃度で分離されるため、芳醇さに富み、初留分のみを使った蒸留酒の銘柄も作られている。
脱水を目的とする蒸留では、ベンゾフェノンが指示薬として使用されることがある。
種類[編集]
蒸留方法は、目的に応じてさまざまなものが使用されている。以下に概略を示す。
減圧蒸留[編集]
蒸留は、大気圧下で実施する常圧蒸留と、系内を減圧にして行う減圧蒸留がある。沸点の極めて高い物質や、熱によって分解・反応してしまう物質は、減圧蒸留することで加熱を抑制することができる。
蒸留酒の製造においても常圧蒸留と減圧蒸留が使い分けられている。減圧蒸留の方がC5アルコールやエステル分を含むフーゼル油よりも沸点が低いエタノールを効率的に分離できるため、くせが少なくキレのよい蒸留酒となる反面で、材料毎の風味は生かし辛くなり、芳醇さが減る。
分子蒸留[編集]
蒸発面と凝縮面との距離を、蒸気分子の平均自由行程以下に接近させることで蒸留を行う、分子蒸留と呼ばれる方法がある。代表的なものとして遠心式蒸留装置があげられる。蒸留器内部を高真空にする事で、通常では気化しない高分子の蒸留を行える。
化学薬品製造時の副生成物・残留原材料などを除去し、平均分子量の範囲を狭め、高純度化する用途に用いられる。
水蒸気蒸留[編集]
共沸現象を積極的に利用する蒸留法に水蒸気蒸留がある。ローズオイルなど天然香料(エッセンス)の工業的精製には現在でも多用されている。
形状による分類[編集]
単純な形状をした蒸留装置(バッチ蒸留装置)の場合、蒸気が凝縮-蒸発サイクルが少ない段階で凝縮器に導入されるため濃縮効率が悪い。このような蒸留方法を単式蒸留と呼ぶ。代表的な例では本格焼酎、ウイスキーなどの蒸留酒の蒸留が挙げられる。単式蒸留器を使った方がエタノールの濃縮効率は劣るが、エステルなどの芳香成分がいっしょに蒸留されて、芳醇になるため、特徴ある製品作りに利用されている。日本における焼酎のように『酒税法』に明記して連続式蒸留と扱いを分けている[注釈 1]例もある。
単式蒸留でもっとも単純な構造を持つ装置に、クーゲルロール蒸留装置がある。この装置は蒸発させたサンプルを隣接する球体で冷却して捕集するので理論段数はよくない。
逆に、蒸留塔を高くし、かつ内壁の表面積が大きくなるようにすると、凝縮-蒸発サイクルの理論段数が増え濃縮効率が向上する。このような理論段数を高くした蒸留を分別蒸留(分留)と呼ぶ。代表的な例では石油の分留が挙げられる。
分別蒸留の蒸留塔として代表的なものにビグリューカラムが挙げられる。また、理論段数を能動的に向上させた蒸留装置としてスピニングバンド蒸留装置が挙げられる。この装置は蒸留塔内に凝縮液の薄膜が強制的に形成させるので、非常に高い理論段数を有する。
また、凝集器導入口に分取蒸留ヘッドをつけて、留去時の成分を精密に捕集する装置を還流蒸留装置と呼ぶ。この装置を使うと沸点でおおよそ5度差の物質を分別蒸留可能といわれている。
用いる器具[編集]
- ト字管
- ジムロート
- リービッヒ冷却器
- 二又アダプター
- ビグリューカラム
- エバポレーター
- レトルト
- アランビック
- 木桶蒸留器[2]
- 直釜(じがま)式焼酎蒸留器[3]
- ツブロ(粒露)式焼酎蒸留器[4]
- ランビキ - 兜釜(かぶとがま)式焼酎蒸留器[5]
関連項目[編集]
- 蒸留塔
- 単式蒸留器
- 連続式蒸留器
- 蒸留酒
- 乾留
- 石油精製
- 空塔速度
- 蒸留製錬 - 水銀などに適用される。
- ハイドロゾル#芳香蒸留水 - フローラルウォーター、エッセンシャルウォーターとも呼ばれる。
- 段塔
- 塩
- 海水淡水化
脚注[編集]
注釈[編集]
- ^ 2006年まで、単式蒸留の焼酎は焼酎乙類、連続式蒸留の焼酎は焼酎甲類と称した。
出典[編集]
- ^ 長倉三郎、他(編)、「精留」、『岩波理化学辞典』、第5版 CD-ROM版、岩波書店、1998年。
- ^ 創業から続く「木桶蒸留」の話|伝兵衛蔵だより|伝兵衛蔵|濵田酒造、現代の名工 晴れの栄誉! |報道発表資料|厚生労働省_別添 平成23年度 卓越した技能者表彰_p.27_第13部門_おけ・たる製造工_津留辰矢_2011年11月14日(現代の名工)
- ^ 八重山の酒造所特有の直火釜蒸留での泡盛造り 泡盛ナビ、直釜とは - 焼酎・泡盛用語 Weblio辞書
- ^ 蒸留酒器の分類とツブロの伝来 - 200611鹿児島民具学会、ツブロ式焼酎蒸留器 文化遺産オンライン
- ^ 焼酎の伝播の検証と,その後に於ける焼酎の技術的発展_東京農大農学集報,54(4),219-229(2010)_農林水産省農林水産技術会議事務局筑波事務所、【蔵見学】実践!明治の球磨焼酎~兜釜蒸留の再現! 2013年04月19日の記事 _ 球磨焼酎専門店一期屋、兜釜とは - 焼酎・泡盛用語 Weblio辞書
外部リンク[編集]
- 化学工学基礎-蒸留コース - 研究人材のためのe-learning(科学技術振興機構)