アセトン
| アセトン | |
|---|---|
| |
| 識別情報 | |
| CAS登録番号 | 67-64-1 |
| KEGG | D02311 |
| 特性 | |
| 化学式 | C3H6O |
| モル質量 | 58.08 |
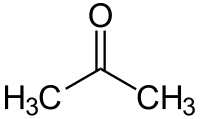
| 示性式 | CH3COCH3 または (CH3)2CO |
| 外観 | 無色液体 |
| 密度 | 0.788 (25 ℃) [1] |
| 融点 |
−94 ℃[1] |
| 沸点 |
56.5 ℃[1] |
| 水への溶解度 | 任意に混和する |
| 酸解離定数 pKa | 20(水中) |
| 屈折率 (nD) | 1.3591 (20 ℃, D)[1] |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |

アセトン (acetone) は有機溶媒として広く用いられる有機化合物で、もっとも単純な構造のケトンである。IUPAC命名法では プロパン-2-オン (propan-2-one) [2]あるいは単にプロパノン。両親媒性の無色の液体で、水、アルコール類、クロロホルム、エーテル類によく溶け、ほとんどの油脂もよく溶かすことができる。蒸気圧が20 ℃において24.7 kPaと高いことから、常温で高い揮発性を有し、強い引火性がある。ジメチルケトンとも表記される[2]。
解説[編集]
アセトンは、ブドウ糖の嫌気的発酵の一つであるアセトン-ブタノール-エタノール発酵によって生成するほか、人体でも正常な代謝プロセスの結果としてケトン体から自然に生成され排出される物質で、生殖毒性試験では生殖問題を起こす可能性が低いことが明らかになっている。実際に、エネルギー必要量が高く体内の脂肪の利用が高まるとアセトンの生成レベルも高くなることから、妊婦、授乳中の母親、および小児の体内アセトンのレベルは自然と上昇する。糖尿病患者が糖尿病性ケトアシドーシスに陥った時には大量に生成して、呼気がアセトン臭を呈する。難治性てんかんを患う乳児や小児のてんかん発作を減少させるため、体内のケトン体を増加させるケトン食療法が行われているが、アセトンの薬理効果を期待したものではない。
関連法規[編集]
- 消防法により危険物第四類(第一石油類 危険等級2 水溶性)に指定されている。指定数量以上の貯蔵・取扱には市町村長等の許可が、指定数量の1/5以上指定数量未満の貯蔵・取扱には消防署への届出が必要で、指定数量以上の取り扱いには危険物取扱者乙四類か、甲種免許所持者でなければならない。
- 麻薬向精神薬原料対象物質
- 有機溶剤中毒予防規則により第二種有機溶剤に指定されている。
製造[編集]
酢酸カルシウムの乾留や、クメン法によるフェノール製造の過程で、クメンヒドロペルオキシド (C6H5C(CH3)2OOH) の酸分解の段階において、アセトンが副生物として得られる。また、2-プロパノールを酸化亜鉛などの触媒存在下に脱水素、あるいは空気酸化して得られる酸化物を分解することによっても得られる。プロピンに水を付加することでも得られる。プロピレンをワッカー酸化によってアセトンとする方法も用いられる。
アセトンから出発する有機合成の需要は比較的少なく、クメン法などに伴い副生するアセトンの産量は過剰である。このため概して価格は安い。
合成アセトンの 2016年度日本国内生産量は 406,620 t、工業消費量は 146,709 t である[3]。
歴史的には、初期の製造法では木材を乾留して得られる木タールを蒸留して得ていたが、この方法では生産量が少なく、アセトンは高価な試薬であった。無煙火薬が発明されるとコルダイトを製造するための溶媒として大量に必要になり需要が激増した。ハイム・ワイツマンが第一次世界大戦中に、ブドウ糖にバクテリアの1種クロストリジウム・アセトブチリクムを作用させるバクテリア発酵法を発明し、イギリス軍に提供した。
危険性[編集]
危険有害性情報として「引火性の高い液体及び蒸気、眼刺激、生殖能又は胎児への悪影響のおそれの疑い、眠気又はめまいのおそれ、呼吸器への刺激のおそれ、長期又は反復ばく露による血液の障害のおそれ、飲み込み・気道に侵入すると有害のおそれ」、MSDS に「眼の刺激性、中枢神経への影響あり」と表示される。吸引すると頭痛、気管支炎などを引き起こし、大量だと意識を失うこともある。ラットの半数致死量 (LD50) は 10.4 mL/kg(経口)[4]。 ヒト経口推定致死量は50 - 75mL。
経口摂取および、または吸引された場合、低い急性および慢性毒性を持つことが一般的に認識されている。空気中の高濃度アセトン(9200 ppm 前後)の吸引は、早ければ5分以内でヒトの喉に刺激を与えた。濃度1000 ppm を吸引すると、1 時間未満で目と喉に刺激を与えたが、空気中濃度 500 ppm のアセトンの吸引は、2 時間の暴露後もヒトに刺激症状を引き起こさなかった。発癌物質や変異原性化学物質とは見なされておらず、慢性神経毒性作用の懸念もないとされている。
用途[編集]
ほとんどの有機溶媒、水、油と混和するので、本来混じり合わない液体同士を混ぜ合わせる際のカップリング剤となる。加えて、沸点が低く乾きやすいため、有機化学研究の分野で器具の洗浄にも使われる。また、1,2-ジオールのアセトニド保護にも使われる。アメリカとヨーロッパの共同研究により、アセトンの「健康被害はわずか」であることが判明している。
付け爪用リムーバー、除光液、スプレーペイントや染み抜きなど一般的に使用される製品での「当然予期される子供へのアセトンの暴露」に対する広範囲な研究も行われたが、子供の環境、および消費者製品によるアセトンの暴露は、重大な健康リスクを引き起こす可能性は少ないという結果となった。子供の体内に存在するアセトンの 90 パーセントは、体内で自然に生成されるものであることも特定された。残り10 パーセントは、たまねぎ、ブドウ、カリフラワー、トマト、牛乳、チーズ、豆類およびサヤエンドウといった自然食品源のほか、母乳からのものである。
- 生物学に関連する諸分野
- 生物組織の脱水、脱脂、固定、標本作成などに用いられることがある。生物遺体の水分を合成樹脂に置き換えて標本にするプラスティネーション処理を行う際には、合成樹脂を含浸させる前に水分と脂肪分を全てアセトンに置き換える。植物化石の組織構造を連続切片プレパラート標本として得るためのピール法では、アセテートフィルムを膨潤軟化させる溶剤としてアセトンが用いられる。
- 生化学や分子生物学に於いて、水溶液として得られたタンパク質の沈殿精製に脱水剤として用いられる。
- 化学原料
- アセトンは、メタクリル酸メチル (MMA) の原料として用いられる。
- 溶媒と酸化剤とを兼ねるかたちで、オッペナウアー酸化(Oppenauer oxidation、トリアルコキシアルミニウム触媒により 2級アルコールからケトンを生成する酸化反応)にて用いられる。
- アセトンをしかるべき反応条件で酸化させると、過酸化アセトン、あるいはジメチルジオキシランを生じる。
- 高圧ガス関連技術
- 工業においては、単体では容易に分解やそれによる爆発を起こしやすいアセチレンを、ガスボンベ内で安定な状態で保つために容器内にアセトンが使われる。まずガスボンベ内にケイ酸カルシウムを入れ、次にアセトンをボンベ内に入れることでケイ酸カルシウムにアセトンを吸着させる。その吸着しているアセトンにアセチレンを溶解することで、ボンベ内で比較的安定に保つことができる。
- 食品添加物
- メタノールと同じく食品添加物や食品包装の成分としてもリストされている。飲料、焼き菓子、デザートやジャムに濃度 5~8 mg/L の範囲で使用されている場合は、GRAS(一般的に安全と認められる)物質として評価されている。しかしアセトンやメタノールなどの毒性の高い食品添加物は残存量が規定されている[5]。
- 医学的および美容用途
- 医療オフィスやメディカルスパでの肌の活性化プロセスによく使用される[要出典]。
- マニキュアの除光液やプラスチック系接着剤、塗料の溶剤、瞬間接着剤のはがし液など多くのものに含まれている。マニキュアの除光液は脱脂性が強いため爪を劣化させることがあり、ノンアセトンタイプの除光液も発売されている。
- ケミカルピーリングを行う際の、皮膚の脱脂用途として用いられる。これには、アセトン、Septisol(ヘキサクロロフェン)、またはこれら化学物質の組み合わせがよく使用される[要出典]。
参考文献[編集]
- ^ a b c d Merck Index 14th ed., 66.
- ^ a b 国際化学物質安全性カード ICSC:0087
- ^ 経済産業省生産動態統計年報 化学工業統計編
- ^ Merck Index 13th ed., 67.
- ^ 厚生労働省・食品添加物 (PDF)
参照資料[編集]
- アセトン MSDS - 内藤商店
- 国際化学物質安全性カード アセトン (ICSC:0087) 日本語版(国立医薬品食品衛生研究所による), 英語版
- 『アセトン』 - コトバンク
- アセトン (試薬) JISK8034:2006
