ベンゾジアゼピン依存症
| ベンゾジアゼピン依存症 | |
|---|---|
| 概要 | |
| 診療科 | 精神医学 |
| 分類および外部参照情報 | |
| ICD-10 | F13.2 |
| ICD-9-CM | 304.1 |
| DiseasesDB | 29548 |
| MedlinePlus | 003578 |
| eMedicine | Bztox/813255 |
ベンゾジアゼピン依存症(ベンゾジアゼピンいそんしょう、Benzodiazepine dependence)とは、『精神障害の診断と統計マニュアル』第4版(DSM-IV)に従えば、耐性、離脱症状、薬物探索行動、有害な影響に反しての継続使用、不適切なパターンにおける使用、などのいずれか3つ以上を満たした状態である。しかしベンゾジアゼピン依存症の場合には、薬物による快い作用よりも不快な離脱反応を回避するために継続的に使用しているとみられている[1]。ベンゾジアゼピン依存症は、長期間の使用によって、低い治療用量においても[2]、依存行動がなくても形成される[3][4]。
嗜癖の場合は、時に精神的依存と呼ばれるように、誤用や、離脱症状の軽減のためではなく陶酔あるいは酔う作用のために薬物を渇望する人々を含む。ベンゾジアゼピンの嗜癖や薬物乱用と、ベンゾジアゼピン系薬物の治療用使用による身体依存の区別は重要である。ベンゾジアゼピンに起因するA受容体抑制の増加は、身体に薬物の作用に対する耐性を形成することによって無効になる。この耐性の形成は、GABA抑制の減少とグルタミン酸系における興奮の増加をもたらす神経適応の結果として生じる。これらの適応は恒常性を取り戻そうと、薬物による中枢神経系への抑制作用を制しようとする身体の結果として生じる。ベンゾジアゼピンを中止した際に、これらの神経適応は「露わになり」神経系の過剰興奮と離脱症状の出現につながる[5]。
治療用量依存が、ベンゾジアゼピンに依存した人々の最も多い種類である。これらの人々はたいてい、高水準にまで用量は増加せず、薬の乱用もない。少数では用量が高水準にまで増加していき、乱用されがちである。どのくらいの数の人々が、ベンゾジアゼピンを違法に乱用しているかについて正確なことは定かではない。抗てんかん、催眠、筋弛緩作用への耐性は数日から数週間以内に形成され、4か月後にもベンゾジアゼピンの抗不安の特性が保たれていることを示す証拠はほとんどない。しかし一部の研究者はこれに反して、抗不安の特性が保たれていると考えている[6]。依存の結果としてのベンゾジアゼピンの長期的影響により、当初の問題としていた症状が悪化する可能性すらある。日本の多剤大量処方においては、非常に高用量となっている場合がある[7]。長期間のベンゾジアゼピンの投薬は、多少の臨床条件においては必要なままでもいい可能性がある[8]。
2002年以来、ベンゾジアゼピンの誤用と依存が懸念されてきた。米国の物質乱用治療施設における患者の特徴の年次編集物である米国の治療エピソードデータ集(Treatment Episode Data Set, TEDS)の調査結果に基づくと、主な精神安定剤(primary tranquilizer、ベンゾジアゼピンだけに限られてない)の使用による入院が、1992年から2002年の間に79%増加した。それゆえ、米国薬物乱用警告ネットワーク (Drug Abuse Warning Network) とTEDSの統計は、これらの鎮静催眠剤の誤用が上昇傾向で、懸念の原因であることを明確に証明している[9]。
ベンゾジアゼピンの処方数は、主に依存の懸念から減少してきた。短期的には、ベンゾジアゼピンは急性の不安や不眠のための有効な薬である。長期間の使用では、他の治療、薬物療法と精神療法の両方が、更に効果的である。長期的には他の治療法のほうが有効性が高く、またベンゾジアゼピンへの耐性が薬理学的に形成されるためでもある[10][11]。
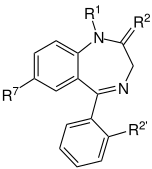
| ベンゾジアゼピン |
|---|
|
| ベンゾジアゼピン系の核となる骨格。 「R」の表記部分は、ベンゾジアゼピンの異なる 特性を付与する側鎖の共通部位である。 |
| ベンゾジアゼピン |
| ベンゾジアゼピンの一覧 |
| en:Benzodiazepine overdose |
| ベンゾジアゼピン依存症 |
| ベンゾジアゼピン薬物乱用 |
| ベンゾジアゼピン離脱症候群 |
| ベンゾジアゼピンの長期的影響 |
定義[編集]
ベンゾジアゼピン依存症は、ベンゾジアゼピン系薬物の反復的な使用の結果としての病態である。これは身体的依存と精神的依存の両方を含むことができ、減量や急な断薬などによってベンゾジアゼピンの血中濃度が下がった期間中に離脱症状が生じるという特徴がある[12]。
徴候と症状[編集]
ベンゾジアゼピン依存症の徴候と症状は、薬なしではうまくできないと感じたり、薬物の切り詰めや中止の試みの失敗、薬の作用に対する耐性、服薬しなかった際の離脱症状などである。離脱症候群には、不安、抑うつ気分、離人症、現実感喪失、睡眠障害、触覚や痛みに対する過感受、震え、痙攣、筋肉痛、頭痛などがある[13]。ベンゾジアゼピンへの依存および離脱は、自殺や自傷行為に結びついており、特に若年層に顕著である。英国国立薬物乱用治療庁の薬物誤用ガイドラインは、依存や離脱時に気分障害に対する観察を推奨している[14]。
ベンゾジアゼピン依存症は、ベンゾジアゼピン薬の4週間以上処方や使用に対して頻繁にみられる合併症であり、身体的依存や離脱症状が最も共通した問題であるが、ときおり薬物探索行動もみられる。離脱症状には、不安、知覚障害、すべての感覚の歪み、不快、まれに精神病やてんかん発作などがある[15]。
原因[編集]
ベンゾジアゼピンの筋弛緩、抗てんかん、睡眠導入作用には、耐性が生じ、断薬時にベンゾジアゼピン離脱症候群が生じる。そのため患者は離脱症状を抑えるために長期間に渡り服薬し続け、ベンゾジアゼピン系を当初の予定よりも長く服用し続けてしまう。一部の人々は非常に高用量のベンゾジアゼピンを乱用し、そのために多くの時間を割いており、これはDSM-IVの薬物乱用と依存症の診断基準を満たす。別の患者集団では、ベンゾジアゼピンの低用量から中等度の治療用量であり、乱用はないが耐性とベンゾジアゼピン依存症が形成されている[5]。不眠症に対してベンゾジアゼピンを使用する患者の多数は、服用量を増加させており、それは時に治療的な処方量の水準を超えている。ベンゾジアゼピンの抗不安作用に対する耐性はラットで明確に証明されている。ヒトではベンゾジアゼピンの4ヶ月を超える継続投薬において抗不安作用が持続するという証拠はほとんどない。ベンゾジアゼピンの長期的な使用が不安を悪化させ、服用量の増加につながるという証拠があり、ある研究では患者の25%が服用量を増加している。ある著者はベンゾジアゼピンは長期的に有効であると考えているが、しかしながらそれは反跳性不安と離脱の影響を抑えるためである可能性が高い。ベンゾジアゼピンの抗痙攣と筋弛緩作用に対する耐性は、ほとんどの患者において数週間以内に発現している[6]。
危険因子[編集]
ベンゾジアゼピン依存症の危険因子は、4週間以上の長期間の使用、高力価の短時間作用型ベンゾジアゼピン系の使用、依存性人格、薬物乱用の傾向などである[15]。短時間作用型のベンゾジアゼピンは離脱の影響を軽減するための反復につながり依存が強化されやすい[13]。低力価のクロルジアゼポキシド(コントールやLibrium)よりもアルプラゾラム(ソラナックスやXanax)などの高力価のベンゾジアゼピンのほうが、身体的依存が迅速に形成される[11]。
症状は高用量、高力価、短い半減期のベンゾジアゼピンのほうが重症である。ベンゾジアゼピンはバルビツール酸系やアルコールのような鎮静催眠剤との間に交叉耐性があり、それらの使用はベンゾジアゼピン依存症のリスクを高める[16]。痛みに対するオピオイドの使用と同様、ベンゾジアゼピンの治療上の使用では薬物乱用につながることはまれである[17]。
機序[編集]
耐性は、睡眠導入作用に対して急速に生じるが、抗不安作用については数カ月間かかる。抗痙攣作用と筋弛緩効果についてはたいていは数週間かかる。
この節の加筆が望まれています。 |
交叉耐性[編集]
ベンゾジアゼピンは、GABAA受容体の増強作用について様々な鎮静剤と似たような機序を共有する。交叉耐性とは、ある薬が別の薬の離脱の影響を軽減する事を意味する。それはまた、ある薬への耐性は、別の類似作動薬への耐性の結果である。これがベンゾジアゼピンがアルコール依存患者を解毒するために用いられ、振戦せん妄のような重篤な命に関わるアルコールの離脱症候群を予防また治療するという救命の特性を有している理由である。しかしベンゾジアゼピンはアルコール依存症の急性の解毒には非常に有効であるが、アルコールへの欲求を増加させることにより、アルコール依存症の正の強化因子として作用する。低用量のベンゾジアゼピンは、アルコール依存症者のアルコール消費量を有意に増加させる[18]。ベンゾジアゼピンに依存しているアルコール依存症では、ベンゾジアゼピンは急に離脱すべきではなく、非常にゆっくりとした離脱である必要がある。急すぎる離脱は重篤な不安やパニックをまねきやすく、それはアルコール依存症の回復における再発リスクであることがよく知られている[19]。
アルコール、ベンゾジアゼピン系、バルビツール酸系、非ベンゾジアゼピン系薬にわたって交叉耐性が存在し、それは全てGABAA受容体のクロライド・イオンチャネルの機能を調整することで、GABAAの機能を増強する作用がある[20][21][22][23][24]。
この節の加筆が望まれています。 |
離脱の生理学[編集]
離脱症状は、慢性的なベンゾジアゼピン使用者に起こる通常の反応であり、また副作用と薬物耐性の結果である。薬物の服用量が減少すると症状が現れるのが典型的である。GABAは中枢神経系において、2番目に最も共通する神経伝達物質である(最も共通するのはグルタミン[25][26][27])。それは圧倒的なほど最も豊富に存在する抑制性神経伝達物質であり、4分の1から3分の1のシナプスはGABAを利用している[28]。ベンゾジアゼピンの使用は、脳と身体機能のほとんどあらゆる面で直接また間接的に深い影響を持っている[29]。
ベンゾジアゼピンはノルアドレナリン、セロトニン、アセチルコリン、ドーパミンを減少させる要因となる。これらの神経伝達物質は正常な記憶、気分、筋緊張および協調、情動反応、内分泌腺分泌、心拍、血圧の制御に必要である。しかし慢性的にベンゾジアゼピンを使用しているとそれらの作用の大部分に対して急速に耐性が形成され、そのためベンゾジアゼピンから離脱した場合には、GABA作動性の抑制作用が無くなり様々な神経伝達物質が暴走する。その結果として離脱症状が出現し、中枢神経系において生じた適応が身体的に逆転するまで持続する[29]。
離脱症状は、一般にその薬物の作用の鏡像となる: 鎮静作用と睡眠の段階におけるREM睡眠と徐波睡眠の抑制は、不眠症、悪夢、入眠時幻覚に置き換わる;抗不安作用は不安とパニックに置き換わる;筋弛緩作用は筋痙攣や筋肉痛に置き換わる;また抗てんかん作用は発作に置き換わり、特にcold turkeyや過剰に急激な離脱において顕著である[29]。
この節の加筆が望まれています。 |
離脱[編集]



ベンゾジアゼピン系の長期間の使用は、身体と精神の両面で健康の問題を増加させることにつながるため、多くの長期服用者に中止が推奨される。ベンゾジアゼピン離脱症候群は、軽症で短期の症状から長期的で重篤な症状まで幅広い。ベンゾジアゼピンを利用することとなった当初の理由が過ぎ去ったあとも、離脱症状によって長く何年もベンゾジアゼピンを使用し続けることにつながる。そのため多くの患者はもはやベンゾジアゼピンが効かないことが分かっていながら、離脱症状のためにベンゾジアゼピンを断薬できないでいる[29]。
離脱症状は徐々に減量しても生じるが、離脱をさらにゆっくりにすることで症状を緩めることは可能である。そのため離脱の速度は、個々の患者に合わせていくことが推奨される。離脱に要する期間は、数ヶ月から1年以上とさまざまであり、服用期間、服用量、生活習慣、健康、社会と環境のストレスといった要因にもよる[29]。
ジアゼパム(セルシンやホリゾン)は、長い半減期と、低力価の中でも入手しやすいこともあり減薬のためよく推奨される。ゾルピデム (マイスリー)、ザレプロンやゾピクロン(アモバン)のような非ベンゾジアゼピン系のZ薬は、ベンゾジアゼピンを置き換えるために使用すべきではなく、これらは作用機序が類似しており同様の依存につながる。ベンゾジアゼピンの薬理学的な耐性および依存の機序は、脳の受容体部位の内部化(削除)や、脳における遺伝子転写コードの変化によるものである[29]。
長期間使用したベンゾジアゼピンの離脱期間中には、抑うつや感情鈍麻が出現し、時に自殺念慮が起こることがある。高用量を服用していた場合にこのような傾向が強いという証拠がある。ベンゾジアゼピンの減量でも断薬でも、そのような事態を招く可能性がある。断薬後であっても、これらの離脱症状は長い間持続することがある。一般的な遷延性離脱症候群は、不安、抑うつ、不眠症、消化器、神経系や筋骨格系の影響などである。遷延性離脱状態は量をゆっくり減らしていった場合であっても生じることがある。このような遷延性離脱の影響は残存する神経適応に起因すると考えられている[11]。
予防[編集]
認知機能障害のような[30]有害な健康への影響、耐性の形成、依存症のリスクのため[31]、ベンゾジアゼピンは短期間の使用―数週間、そして続いて徐々に減量する―が指示されている[32]。
英国医薬品再評価委員会[編集]
英国医薬品再評価委員会(The Committee on the Review of Medicines)は、ベンゾジアゼピンの耐性、薬物依存症、離脱の問題、他の有害作用について重大な懸念に基づいて調査を実施し、その結果は『英国医学雑誌』(the British Medical Journal)の1980年3月号に掲載された。委員会にてベンゾジアゼピンには抗うつ薬や鎮痛薬としての適性がないことが判明し、そのためうつ病、緊張型頭痛、月経困難症などの状態には不適切であると結論した。またベンゾジアゼピンは精神病の治療にも利益がなかった。また委員会は子供の不安や不眠症の治療に対するベンゾジアゼピンの使用には反対するということを勧告した[33]。
委員会は、耐性の形成のためベンゾジアゼピン系睡眠薬の長期間の使用のための証拠がほとんどないことについて、米国医学研究所(IOM)や、ホワイトハウス薬物規制政策室と米国国立薬物乱用研究所(NIDA)らが実施した研究の結論と見解が一致している。ベンゾジアゼピンは継続使用によって3〜14日以内に睡眠促進の特性が失われる傾向にあり、不安の治療においては、耐性が形成されるため継続使用の4カ月後に効果を保っているという説得力のある証拠がほとんどないことが、委員会により判明した[33]。
委員会の見解は、ベンゾジアゼピンの常用により治療効果への耐性により依存が形成され、断薬時には不安、恐怖、振るえ、不眠、吐き気、嘔吐などのベンゾジアゼピン離脱症候群が出現するということである。離脱症状は、短時間作用型ベンゾジアゼピンの断薬時には24時間以内に、長時間作用型ベンゾジアゼピンの断薬時には3〜10日後に発症する傾向がある。離脱の影響は、治療用量水準では2週間までしか生じないが、高用量を習慣的に投与された場合は2週間以上続く傾向がある。離脱症状は元の症状に似ているように見える[33]。
委員会は、すべてのベンゾジアゼピンの投薬からの離脱は徐々にし、またベンゾジアゼピンの投薬は慎重に選別した患者のみにして、投薬は短期的な使用に限定すべきと推奨している。レビューにおいては、アルコールは中枢神経系の抑制作用を増強するために禁止すべきであると記載している。ベンゾジアゼピンの中枢神経抑制作用は運転や機械操作を危険にし、この有害作用は高齢者に顕著である。一度に高用量、低用量の継続投与は、哺乳力の低下、低血圧、新生児の低体温、胎児心臓の異常につながることが報告されてきた。委員会はベンゾジアゼピンを授乳時には禁止すべきだと推奨している[33]。
委員会は高用量のベンゾジアゼピンからの急な離脱は混乱、中毒性精神病、痙攣、振戦せん妄に似た状態の原因となるため、離脱は徐々に行うべきであると推奨している。低用量からの急な離脱は抑うつ、緊張、反跳性不眠、易刺激性、発汗、下痢の原因になることがある[33]。
診断[編集]
ICD-10におけるベンゾジアゼピン依存症の診断には、1ヶ月以上続くか、あるいは12ヶ月の間に繰り返す、以下の基準を3つ以上満たすことが必要である[34][35]。
- 典型的には薬を服用したいという強い欲望をもつ反復的な使用に関連した行動、認識、生理現象
- 使用の制御が困難
- 有害な結果にもかかわらず継続的に使用する
- 他の活動や責務より、薬物使用を優先している
- 薬物の作用に対する耐性の増加、時に身体的離脱状態
これらの診断基準は研究目的に適しており、日常的な臨床実務においては臨床的な判断に従って解釈されるべきである。臨床実務においては、ベンゾジアゼピン依存症は1か月以上のベンゾジアゼピンを用いた場合に疑うべきであり、とりわけそれはハイリスク群においてである。ベンゾジアゼピン依存症の発症を増加させることに結びつく主な要因を挙げる:[34]
- 用量
- 期間
- 抗うつ薬の併用
またベンゾジアゼピン依存症は、アルコールを含む物質使用障害を有する患者や、独自のベンゾジアゼピンの供給を求める患者において疑われるべきである。ベンゾジアゼピン依存症は、精神安定剤の自助グループのメンバーである患者においてはほぼ確実である[34]。
調査では、ベンゾジアゼピン依存症と診断された人の約40%が自分では依存に気づいておらず、約11%は依存していないと信じていた。ベンゾジアゼピン依存症を評価する場合には概念的な質問よりも具体的な質問が、より正確な診断をするために良い方法として専門家によって推奨されている。たとえば「心理的依存」という用語よりも「よく薬について考えている」といった[34]。Benzodiazepine Dependence Self Report Questionnaire(Bendep-SRQ)は、ベンゾジアゼピン依存症の評価と診断に用いる質問表である[34]。
軽度の離脱症状が生じていても薬を中止することが容易であればそれは依存ではない[36]。
英国国民保健サービス[編集]
英国の国民保健サービス(NHS)の2006年の『GP向けベンゾジアゼピンおよび睡眠薬の処方・離脱ガイドライン』(Guidance for prescribing and withdrawal of benzodiazepines and hypnotics in general practice)において以下の診断基準を提示している[37]
| 分類 | 象徴エピソード |
|---|---|
| a) 治療用量依存 | 処方されたベンゾジアゼピン系薬による治療用量での依存
|
| b) 処方による高用量依存 | ジアゼパム換算にて30mg以上。いくらかのベンゾジアゼピン処方患者はより多い用量を要求するようになる
|
| c) 娯楽用途での 高用量乱用/依存 |
|
2012年の英国精神薬理学会の物質乱用のガイドラインは、治療用量で乱用がないベンゾジアゼピン依存症と、処方薬の乱用あるいは違法な使用による高用量の依存症の2種類を挙げ、治療困難な後者はまず通常の治療用量へと漸減していくことが目標とされる[38]。
日本の研究からは、睡眠薬/抗不安薬はジアゼパムに等価換算し、1剤では平均8.6mg、同様に2剤で17.3mg、3剤で25.8mg、4剤で38.1mg、5剤は48.6mg、6剤以上では72.1mgである[7]。
高齢者において[編集]
ベンゾジアゼピン依存症と長期間の使用は高齢者において深刻な問題である。高齢者におけるベンゾジアゼピン依存症の治療の失敗は、重篤な内科的な合併症の原因となる[39]。高齢者は、認知的予備力が損なわれてきており、短期(例として離脱の間)また長期的なベンゾジアゼピンの離脱の影響や、同様に、短期と長期の両方における副作用に敏感である。こうして必要以上に医師に接触することにつながる。高齢患者のベンゾジアゼピンからの離脱が、年間の医師の訪問を減少させることにつながっていることを研究は明らかにしており、副作用と離脱の影響を除去するためであると推定されている[11]。
タバコとアルコールは、高齢者の依存症や乱用において最も一般的な物質である。そして次に一般的な物質がベンゾジアゼピンである。薬物誘発性の認知の問題は、高齢者における深刻な懸念であり、錯乱状態と「疑似・認知症」につながる。高齢患者の約10%は記憶専門診療所を訪れ、実際に最も頻繁な薬剤誘発性の原因はベンゾジアゼピンである。ベンゾジアゼピンはまた、高齢者における交通事故と転倒のリスクの増加に関連している。ベンゾジアゼピンの長期的な影響は高齢者やほかの年齢層においても、まだ完全には理解されていない。またそれは注意力や視空間の機能障害に関連している。ベンゾジアゼピンからの離脱は、覚醒状態を改善し高齢者における物忘れを減少させる。ベンゾジアゼピンからの離脱の成功は、記憶機能と技能に関連した能力の統計的に有意な改善につながり、一方そのままの場合は症状を悪化させている。ベンゾジアゼピンから離脱した人々は、睡眠からの目覚めが爽やかであると感じている。このことはベンゾジアゼピンが明らかに高齢者の不眠症を悪化させることを示唆している[40]。
治療と予防[編集]
ベンゾジアゼピン系薬は、強い嗜癖性がある種類の薬物であるとみなされている[41]。心理的また身体依存は、数週間の短期であっても形成されるが年単位を要する人もいる。ベンゾジアゼピンからの離脱を望む患者は、殆ど助言や支援を得られないことが多い[42]。
ベンゾジアゼピンは一般的に短期間に限って処方されており、長期間の処方の正当性は乏しい[43]。しかし一部の医師はこれに同意せず、4週間を超える長期間の使用を正当化できるとみなしているが、その主張を裏付けるデータは乏しい[10]。そのような主張は医学文献において少数派である[44]。
「休薬日」や休薬期間を設けることで依存のリスクを減らすことができるという証拠は存在しない。そして動物実験では、そのような方法では依存を防止できないという証拠が存在する。短時間作用型ベンゾジアゼピン系でも服用間の離脱症状があり、それはキンドリングのリスクを増加させることがある。ベンゾジアゼピンに関するキンドリングについては臨床的に妥当性がある。超短時間型や断続的な使用による服用間の離脱や反跳作用によって、ベンゾジアゼピン系の使用を増加させる[5]。
患者への手紙送付[編集]
一般診療において、患者に対してベンゾジアゼピンの長期間使用の副作用についての警告と減量を推奨する手紙を送ることが、成功しやすく費用対効果も良いベンゾジアゼピンの消費減量の方法であることが判明している。手紙を送付してから1年で、ベンゾジアゼピンの処方数が17%減少し、患者の5%が完全に断薬した[45][46]。オランダの研究では、ベンゾジアゼピン依存症の患者に手紙を送付し、1年以内に11.3%の患者が完全にベンゾジアゼピンを断薬したという高い成功率が報告されている[47]。
薬剤師の介入プログラム[編集]
ある研究では、薬剤師が高齢介護施設の医療スタッフに対して教育的集会を提供し、医薬品の監査と学問的な鎮静剤の意見交換を組み合わせて見直した結果、ベンゾジアゼピンや抗精神病薬の両方について、合計した服用量や服用する入居者の数を大幅に減らすことができた[48]。
認知行動療法[編集]
睡眠薬の使用を減らすための認知行動療法がある。
疫学[編集]
調査では、身体的依存と離脱症候群をもつ治療用量の使用者の数について、異なった結論が出ている。推定では、治療用量での長期ベンゾジアゼピン処方患者の20-100%が身体的に依存しており、離脱症状を経験すると思われる[49]。
英国国立医療技術評価機構(NICE)の不眠症の診療ガイドラインには、ベンゾジアゼピンの慢性的な使用者の10〜30%が身体的に依存し、半数が離脱症状を経験すると記されている[50]。
ベンゾジアゼピンは低用量であっても嗜癖性と依存を形成し、3カ月の使用では23%が依存する。ベンゾジアゼピン依存症は公衆衛生上の問題だとみなされている。ベンゾジアゼピンの処方の約68.5%が近場の医療施設からであり、精神科と総合病院が10%ずつである。一般開業医の調査では、ベンゾジアゼピン処方が開始された理由は、患者の要求というよりも、患者が直面する苦しみへの共感と、他の治療方法の欠如であった。しかしながら、長期間の使用は患者の要求によるもので、それは身体依存や嗜癖が形成されたためだと思われる[51][52][53]。
女性は、男性よりもベンゾジアゼピンがおよそ2倍処方されていた。それは男性は一般的にアルコールにてストレスを解消し、女性は処方薬を用いるためであると思われている。男性医師による女性の偏った認識も、女性への処方率増加の要因があると思われる。しかし、女性の不安の特徴は、男性と女性の間で大きくずれていることが把握されていない[54]。
歴史[編集]
かつて1970年代までは、身体的依存は高い治療用量の人々のみに起こるとされ、低容量や常用量の依存は疑問視されていた。1980年代初頭まで検証されることはなかった[55][56]。しかし、低用量の依存が動物実験およびヒトでの研究で明確に実証され[57][58]、ベンゾジアゼピンの副作用として認知された。重篤な離脱症候群が低用量のベンゾジアゼピンを徐々に減量した後に生じることも分かった[59][60]。推定では長期的な低用量のベンゾジアゼピン服用者の30〜45%が依存しており、依存を避けるために、低用量で最大で7〜14日間の処方に限ることが推奨されている[61]。結果として低用量依存のリスクのため、ベンゾジアゼピンの処方は厳格に規制されている[62]。
乱用と嗜癖[編集]
ベンゾジアゼピンは、乱用薬物の最大の種類の1つである。そのため米国ではスケジュールIV規制薬物に分類され、医療用途であると認識されている[63]。
ベンゾジアゼピンは深刻な依存の問題の原因となる。セネガルの医師における調査では、一般的に多くの医師がベンゾジアゼピンについての訓練と知識が乏しいと感じていることがわかった。ダカールでの調査では、医師の5分の1がベンゾジアゼピンの短期使用ガイドラインを無視し、4分の3が訓練と知識が不十分だと判明した。ベンゾジアゼピンに対しての更なる訓練が推奨される[64]。嗜癖に対する深刻な懸念があるため、緊急に各国の政府は、ベンゾジアゼピンの常習性とベンゾジアゼピンの適切な処方についての訓練を通じて知識を向上させることが推奨されている[65]。
ある研究では、薬物乱用歴のある51人のベトナム帰還兵についての6年間の調査を行った。うち11人は主に覚醒剤、26人は主にアヘン類、14人はベンゾジアゼピンであり、精神的な症状はそれらの薬物乱用に特徴的なものであった。6年後、アヘン類乱用者の精神症状の変化は僅かであり、覚醒剤乱用者の5人は精神病を発症しており、8人のベンゾジアゼピン乱用者はうつ病を発症していた。そのことから、長期間のベンゾジアゼピン薬物乱用と依存はメンタルヘルスに悪影響を及ぼし、特にうつ病発症の大きな危険因子であると思われる[66]。ベンゾジアゼピンは時に経鼻的にも乱用される[67]。
高齢者では、アルコールとベンゾジアゼピンが最も多く乱用される物質であり、若年患者よりもベンゾジアゼピン離脱症候群、せん妄に陥りやすい[68]。
患った著名人[編集]
- スティーヴィー・ニックス - クロナゼパム依存に苦しんだ
- トロント大学教授であり臨床心理学者ジョーダン・ピーターソン - クロノピン(リボトリール・ランドセン)に身体依存し、その離脱症状体験を自身のYoutubeチャンネルで公開している(日本語字幕)
この節の加筆が望まれています。 |
出典[編集]
- ^ de Wit, Harriet; Harriet de Wit, a, Roland R. Griffithsb (June 1991). “Testing the abuse liability of anxiolytic and hypnotic drugs in humans”. Drug and Alcohol Dependence 28 (1): 83–111. doi:10.1016/0376-8716(91)90054-3. PMID 1679388 2012年12月21日閲覧。.
- ^ Nutt, D.J. (1986-01-01). “Benzodiazepine dependence in the clinic: reason for anxiety”. Trends neurosci 7: 457–460. doi:10.1016/0165-6147(86)90420-7 2012年12月21日閲覧。.
- ^ Uzun, S.; Kozumplik, O.; Jakovljević, M.; Sedić, B. (Mar 2010). “Side effects of treatment with benzodiazepines”. Psychiatr Danub 22 (1): 90–3. PMID 20305598.
- ^ O'brien CP (2005). “Benzodiazepine use, abuse, and dependence”. J Clin Psychiatry 66 (Suppl 2): 28–33. PMID 15762817.
- ^ a b c Allison C, Pratt JA (May 2003). “Neuroadaptive processes in GABAergic and glutamatergic systems in benzodiazepine dependence”. Pharmacol. Ther. 98 (2): 171–95. doi:10.1016/S0163-7258(03)00029-9. PMID 12725868.
- ^ a b Haddad, Peter; Deakin, Bill; Dursun, Serdar (2004-05-27). “Benzodiazepine dependence”. Adverse Syndromes and Psychiatric Drugs: A clinical guide. Oxford University Press. pp. 240-252. ISBN 978-0198527480
- ^ a b 中川敦夫ら 2011, p. 8.
- ^ Cloos JM, Ferreira V. (January 2009). “Current use of benzodiazepines in anxiety disorders”. Current Opinion in Psychiatry 22 (1): 90–95. doi:10.1097/YCO.0b013e32831a473d. PMID 19122540.
- ^ Licata SC; Rowlett JK (2008). “Abuse and dependence liability of benzodiazepine-type drugs: GABA(A) receptor modulation and beyond.”. Pharmacology Biochemistry and Behavior 90 (1): 74-89. PMID 18295321.
- ^ a b Puri, Basant K.; Tyrer, Peter (1998-08-28). “Clinical psychopharmacology”. Sciences Basic to Psychiatry (2nd ed.). Churchill Livingstone. pp. 155-157. ISBN 978-0443055140 11-07-2009閲覧。
- ^ a b c d Longo LP, Johnson B (April 2000). “Addiction: Part I. Benzodiazepines--side effects, abuse risk and alternatives”. Am Fam Physician 61 (7): 2121-8. PMID 10779253.
- ^ Authier, N.; Balayssac, D.; Sautereau, M.; Zangarelli, A.; Courty, P.; Somogyi, AA.; Vennat, B.; Llorca, PM. et al. (Nov 2009). “Benzodiazepine dependence: focus on withdrawal syndrome.”. Ann Pharm Fr 67 (6): 408–13. doi:10.1016/j.pharma.2009.07.001. PMID 19900604.
- ^ a b Khong, E.; Sim, MG.; Hulse, G. (Nov 2004). “Benzodiazepine dependence.” (PDF). Aust Fam Physician 33 (11): 923-6. PMID 15584332.
- ^ 英国国立薬物乱用治療庁 2007.
- ^ a b Marriott S, Tyrer P. (August 1993). “Benzodiazepine dependence. Avoidance and withdrawal”. Drug safety: an international journal of medical toxicology and drug experience. 9 (2): 93-103. doi:10.2165/00002018-199309020-00003. PMID 8104417.
- ^ Petursson H (1994). “The benzodiazepine withdrawal syndrome”. Addiction 89 (11): 1455-9. doi:10.1111/j.1360-0443.1994.tb03743.x. PMID 7841856.
- ^ Galanter, Marc; Kleber, Herbert D. (2008-07-01). The American Psychiatric Publishing Textbook of Substance Abuse Treatment (4th ed.). United States of America: American Psychiatric Publishing Inc. p. 114. ISBN 978-1585622764
- ^ Poulos CX; Zack M (2004). “Low-dose diazepam primes motivation for alcohol and alcohol-related semantic networks in problem drinkers”. Behavioural pharmacology 15 (7): 503-12. doi:10.1097/00008877-200411000-00006. PMID 15472572.
- ^ Kushner MG, Abrams K, Borchardt C (March 2000). “The relationship between anxiety disorders and alcohol use disorders: a review of major perspectives and findings”. Clin Psychol Rev 20 (2): 149-71. doi:10.1016/S0272-7358(99)00027-6. PMID 10721495.
- ^ Khanna JM, Kalant H, Weiner J, Shah G (1992). “Rapid tolerance and cross-tolerance as predictors of chronic tolerance and cross-tolerance”. Pharmacol. Biochem. Behav. 41 (2): 355-60. doi:10.1016/0091-3057(92)90110-2. PMID 1574525.
- ^ World Health Organisation - Assessment of Zopiclone
- ^ Allan AM, Baier LD, Zhang X (1992). “Effects of lorazepam tolerance and withdrawal on GABAA receptor-operated chloride channels”. J. Pharmacol. Exp. Ther. 261 (2): 395-402. PMID 1374467.
- ^ Rooke KC (1976). “The use of flurazepam (dalmane) as a substitute for barbiturates and methaqualone/diphenhydramine (mandrax) in general practice”. J Int Med Res 4 (5): 355-9. PMID 18375.
- ^ Reddy DS; Rogawski MA (2000-12-01). “Chronic treatment with the neuroactive steroid ganaxolone in the rat induces anticonvulsant tolerance to diazepam but not to itself”. J Pharmacol Exp Ther 295 (3): 1241-8. PMID 11082461.
- ^ http://www.pubmedcentral.nih.gov/articlerender.fcgi-rendertype=abstract&artid=40853
- ^ Humphries, P; Pretorius, E; Naudé, H (2007). “Direct and indirect cellular effects of aspartame on the brain”. European Journal of Clinical Nutrition 62 (4): 451-462. doi:10.1038/sj.ejcn.1602866. ISSN 0954-3007.
- ^ Herlenius, Eric; Lagercrantz, Hugo (2004). “Development of neurotransmitter systems during critical periods”. Experimental Neurology 190: 8–21. doi:10.1016/j.expneurol.2004.03.027. ISSN 00144886.
- ^ http://thebrain.mcgill.ca/flash/a/a_01/a_01_m/a_01_m_ana/a_01_m_ana.html
- ^ a b c d e f The Ashton Manual 2002.
- ^ Heberlein, A.; Bleich, S.; Kornhuber, J.; Hillemacher, T. (Jan 2009). “[Benzodiazepine dependence: causalities and treatment options]”. Fortschr Neurol Psychiatr 77 (1): 7–15. doi:10.1055/s-0028-1100831. PMID 19101875.
- ^ Tyrer, Peter; Silk, Kenneth R., eds (2008-01-24). “Treatment of sedative-hypnotic dependence”. Cambridge Textbook of Effective Treatments in Psychiatry (1st ed.). Cambridge University Press. pp. 402. ISBN 978-0-521-84228-0
- ^ Karch, Steven B. (2006-12-20). Drug Abuse Handbook (2nd ed.). United States of America: CRC Press. p. 617. ISBN 978-0-8493-1690-6
- ^ a b c d e Committee on the Review of Medicines (1980-03-29). “Systematic review of the benzodiazepines. Guidelines for data sheets on diazepam, chlordiazepoxide, medazepam, clorazepate, lorazepam, oxazepam, temazepam, triazolam, nitrazepam, and flurazepam. Committee on the Review of Medicines”. Br Med J 280 (6218): 910-2. doi:10.1136/bmj.280.6218.910. PMC 1601049. PMID 7388368.
- ^ a b c d e Polmear, Andrew (2008-03-31). Evidence-Based Diagnosis in Primary Care: Practical Solutions to Common Problems. United Kingdom: Butterworth-Heinemann. pp. 346-347. ISBN 978-0-7506-4910-0
- ^ ICD-10 (2007年). “Chapter V - Mental and behavioural disorders (F00-F99) - Mental and behavioural disorders due to psychoactive substance use, 10-F19)”. World Health Organisation. 2012年2月4日閲覧。
- ^ WHO Programme on Substance Abuse 1996, p. 21.
- ^ NHS Grampian 2006, pp. 4–5.
- ^ 英国精神薬理学会 2012, pp. 16–18.
- ^ Madhusoodanan S, Bogunovic OJ (September 2004). “Safety of benzodiazepines in the geriatric population”. Expert Opin Drug Saf 3 (5): 485–93. doi:10.1517/14740338.3.5.485. PMID 15335303.
- ^ Baillargeon L, Landreville P, Verreault R, Beauchemin JP, Grégoire JP, Morin CM (November 2003). “Discontinuation of benzodiazepines among older insomniac adults treated with cognitive-behavioural therapy combined with gradual tapering: a randomized trial” (PDF). CMAJ 169 (10): 1015–20. PMC 236226. PMID 14609970.
- ^ Casati A, Sedefov R, Pfeiffer-Gerschel T (2012). “Misuse of medicines in the European Union: a systematic review of the literature” (PDF). Eur Addict Res 18 (5): 228–45. doi:10.1159/000337028. PMID 22572594.
- ^ Authier, N; Balayssac, D; Sautereau, M; Zangarelli, A; Courty, P; Somogyi, AA; Vennat, B; Llorca, PM et al. (Nov 2009). “Benzodiazepine dependence: focus on withdrawal syndrome”. Ann Pharm Fr 67 (6): 408-13. doi:10.1016/j.pharma.2009.07.001. PMID 19900604.
- ^ Panus, Peter; Katzung, Bertram G.; Jobst, Erin E.; Tinsley, Suzanne; Masters, Susan B.; Trevor, Anthony J. (November 2008). “Sedative-hypnotic drugs”. PHARMACOLOGY FOR THE PHYSICAL THERAPIST (1 ed.). McGraw-Hill Medical. p. 192. ISBN 978-0071460439
- ^ Tyrer, Peter; Silk, Kenneth R. (2008-01-24). Cambridge Textbook of Effective Treatments in Psychiatry (1st ed.). Cambridge University Press. p. 532. ISBN 978-0521842280
- ^ Morgan JD, Wright DJ, Chrystyn H (December 2002). “Pharmacoeconomic evaluation of a patient education letter aimed at reducing long-term prescribing of benzodiazepines”. Pharm World Sci 24 (6): 231–5. doi:10.1023/A:1021587209529. PMID 12512155.
- ^ Stewart R, Niessen WJ, Broer J, Snijders TA, Haaijer-Ruskamp FM, Meyboom-De Jong B (October 2007). “General Practitioners reduced benzodiazepine prescriptions in an intervention study: a multilevel application”. J Clin Epidemiol 60 (10): 1076–84. doi:10.1016/j.jclinepi.2006.11.024. PMID 17884604.
- ^ Niessen WJ, Stewart RE, Broer J, Haaijer-Ruskamp FM (February 2005). “[Reduction in the consumption of benzodiazepines due to a letter to chronic users from their own general practitioner]” (Dutch; Flemish). Ned Tijdschr Geneeskd 149 (7): 356–61. PMID 15751808.
- ^ Westbury, J; Jackson, S; Gee, P; Peterson, G (Oct 2009). “An effective approach to decrease antipsychotic and benzodiazepine use in nursing homes: the RedUSe project”. Int Psychogeriatr 22 (1): 1–11. doi:10.1017/S1041610209991128. PMID 19814843.
- ^ Ashton, CH (1997). “Benzodiazepine Dependency”. In A Baum, S. Newman, J. Weinman, R. West, C. McManus. Cambridge Handbook of Psychology & Medicine. England: Cambridge University Press. pp. 376-80 2007年7月3日閲覧。
- ^ 英国国立医療技術評価機構 2004, p. 2.13.
- ^ Anthierens S, Habraken H, Petrovic M, Christiaens T (December 2007). “The lesser evil- Initiating a benzodiazepine prescription in general practice: a qualitative study on GPs' perspectives” (PDF). Scand J Prim Health Care 25 (4): 214-9. doi:10.1080/02813430701726335. PMID 18041658.
- ^ Granados Menendez MI, Salinero Fort MA, Palomo Ancillo M, Aliaga Gutierrez L, Garcia Escalonilla C, Ortega Orcos R (2006). “[Appropriate use of benzodiazepines zolpidem and zopiclone in diseases attended in primary care”] (Spanish; Castilian). Aten Primaria 38 (3): 159-64. PMID 16945275.[リンク切れ]
- ^ Barthelme B, Poirot Y (November 2008). “[Anxiety level and addiction to first-time prescriptions of anxiolytics: a psychometric study]” (French). Presse Med 37 (11): 1555-60. doi:10.1016/j.lpm.2007.10.019. PMID 18502091.
- ^ Professor Lader; Professor Morgan, Professor Shepherd, Dr Paul Williams, Dr Skegg, Professor Parish, Dr Peter Tyrer, Dr Inman, Dr John Marks (Ex-Roche), Peter Harris (Roche), Tom Hurry (Wyeth) (30th of October 1980 - 3rd of April 1981) (PDF). Benzodiazepine Dependence Medical Research Council headquarters, Closed until 2014 - Opened 2005. England: The National Archives.
- ^ Fruensgaard K (February 1976). “Withdrawal psychosis: a study of 30 consecutive cases”. Acta Psychiatr Scand 53 (2): 105–18. doi:10.1111/j.1600-0447.1976.tb00065.x. PMID 3091.
- ^ Lader M. (1991). “History of benzodiazepine dependence”. Journal of substance abuse treatment 8 (1–2): 53–9. doi:10.1016/0740-5472(91)90027-8. PMID 1675692.
- ^ Lucki I; Kucharik RF (1990). “Increased sensitivity to benzodiazepine antagonists in rats following chronic treatment with a low dose of diazepam”. Psychopharmacology 102 (3): 350-6. doi:10.1007/BF02244103. PMID 1979180.
- ^ Rickels K; Case WG, Schweizer EE, Swenson C, Fridman RB. (1986). “Low-dose dependence in chronic benzodiazepine users: a preliminary report on 119 patients”. Psychopharmacology bulletin 22 (2): 407-15. PMID 2877472.
- ^ Lader M. (December 1987). “Long-term anxiolytic therapy: the issue of drug withdrawal”. The Journal of clinical psychiatry 48: 12-6. PMID 2891684.
- ^ Miura S; Murasaki M (March 1992). “The future of 5-HT1A receptor agonists. (Aryl-piperazine derivatives)”. Progress in neuro-psychopharmacology & biological psychiatry 16 (6): 833-45. doi:10.1016/0278-5846(92)90103-L. PMID 1355301.
- ^ Meier PJ; Ziegler WH, Neftel K (1988-03-19). “[Benzodiazepine--practice and problems of its use]”. Schweizerische medizinische Wochenschrift 118 (11): 381-92. PMID 3287602.
- ^ Tsuji K, Tajima O (January 2012). “[Anxiolytic]” (Japanese). Nippon Rinsho 70 (1): 42–6. PMID 22413490.
- ^ Karch, Steven B. (2006-12-20). Drug Abuse Handbook (2nd ed.). USA: CRC Press. p. 35. ISBN 978-0849316906
- ^ Dieye AM, Sy AN, Sy GY, et al. (2007). “[Prescription of benzodiazepines by general practitioners in the private sector of Dakar: survey on knowledge and attitudes”] (French). Therapie 62 (2): 163-8. doi:10.2515/therapie:2007018. PMID 17582318.
- ^ Dieye AM, Sylla M, Ndiaye A, Ndiaye M, Sy GY, Faye B (June 2006). “Benzodiazepines prescription in Dakar: a study about prescribing habits and knowledge in general practitioners, neurologists and psychiatrists”. Fundam Clin Pharmacol 20 (3): 235-8. doi:10.1111/j.1472-8206.2006.00400.x. PMID 16671957.
- ^ Woody GE; Mc Lellan AT O'Brien CP (1979). “Development of psychiatric illness in drug abusers. Possible role of drug preference”. The New England journal of medicine. 301 (24): 1310–4. doi:10.1056/NEJM197912133012403. PMID 41182.
- ^ Sheehan MF, Sheehan DV, Torres A, Coppola A, Francis E (1991). “Snorting benzodiazepines”. Am J Drug Alcohol Abuse 17 (4): 457–68. doi:10.3109/00952999109001605. PMID 1684083.
- ^ Wetterling T, Backhaus J, Junghanns K (September 2002). “[Addiction in the elderly - an underestimated diagnosis in clinical practice?]” (German). Nervenarzt 73 (9): 861–6. doi:10.1007/s00115-002-1359-3. PMID 12215877.
参考文献[編集]
- WHO Programme on Substance Abuse (1996年11月). Rational use of benzodiazepines - Document no.WHO/PSA/96.11 (pdf) (Report). World Health Organization. OCLC 67091696. 2013年3月10日閲覧。
- 英国精神薬理学会; AR Lingford-Hughes, S Welch, L Peters and DJ Nutt (2012年7月). "BAP updated guidelines: evidence-based guidelines for the pharmacological management of substance abuse, harmful use, addiction and comorbidity: recommendations from BAP" (PDF). Journal of Psychopharmacology. 26 (7): 899–952. doi:10.1177/0269881112444324. PMID 22628390. 2012年12月3日時点のオリジナル (pdf)よりアーカイブ。
- 英国国立医療技術評価機構 (2004年4月). Insomnia - newer hypnotic drugs (TA77) (Report). National Institute for Health and Clinical Excellence. 2013年3月10日閲覧。
- 英国国立薬物乱用治療庁 (2007年). Drug misuse and dependence - UK guidelines on clinical management (PDF) (Report). United Kingdom: Department of Health.
- Davidson B et al; NHS Grampian (2006年). Guidance for prescribing and withdrawal of benzodiazepines and hypnotics in general practice (PDF) (Report). 英国国民医薬品集. 2012年6月20日時点のオリジナル (PDF)よりアーカイブ。
- Professor Heather Ashton (2002). Benzodiazepines: How They Work and How to Withdraw 2013年1月19日閲覧。
- ヘザー・アシュトン『ベンゾジアゼピン - それはどのように作用し、離脱するにはどうすればよいか』(pdf)Professor C H Ashton、2002年8月。2013年1月19日閲覧。
- The National Center on Addiction and Substance Abuse at Columbia University (2012-06). Addiction Medicine: Closing the Gap between Science and Practice
- 中川敦夫ら『向精神薬の処方実態に関する国内外の比較研究(平成22年度総括・分担研究報告書厚生労働科学研究費補助金厚生労働科学特別研究事業)』(pdf)2011年3月。
関連項目[編集]
外部リンク[編集]
- ヘザー・アシュトン『ベンゾジアゼピン - それはどのように作用し、離脱するにはどうすればよいか』(pdf)Professor C H Ashton、2002年8月。、Professor Heather Ashton (2002). Benzodiazepines: How They Work and How to Withdraw 一般にアシュトンマニュアルと呼ばれる (邦訳は2012年8月19日に公開され、出典論文が省略されている)
- ベンゾジアゼピン依存症 - Curlie(英語) icon
- 佐藤記者の「精神医療ルネサンス」抗不安・睡眠薬依存(1)患者依存させ金もうけ!(2012年6月13日)(読売新聞の医療サイトyomiDr.) (2)ベンゾジアゼピンの害 (6月22日) (3)奇妙奇天烈な主治医の見解(6月26日) (4)ドーピングされた心 (7月3日) (5)薬ばらまき睡眠キャンペーン?(7月10日) (6)睡眠キャンペーン被害者の苦悩 (7月17日) (7)ボツになった告発本 (7月23日) (8)マニュアル公開記念・アシュトン教授に聞いた(8月20日)
