「ドコサヘキサエン酸」の版間の差分
「役割」項目の中でうつ病関係の記述が浮いているので、取り敢えず独立項目にしてみました。それでも記述が散漫ですので、どなたかうまく整理して頂けると幸いです。 |
効能の宣伝を目的とした書籍等を出典としている箇所を除去。 |
||
| 23行目: | 23行目: | ||
[[魚油]]に多く含まれ、日本人は魚類を食べることによって多く摂取していたが近年は減少している。 |
[[魚油]]に多く含まれ、日本人は魚類を食べることによって多く摂取していたが近年は減少している。 |
||
ヒトでは、体内で合成できない[[α-リノレン酸]]から体内でDHAを合成するため、広義では[[必須脂肪酸]]となる。 |
ヒトでは、体内で合成できない[[α-リノレン酸]]から体内でDHAを合成するため、広義では[[必須脂肪酸]]となる。生理活性効果に関して1980年代から積極的な研究が行われ、[[エイコサペンタエン酸|EPA]]と同様に食品添加物や[[健康補助食品]]<ref>加藤恵子、三浦英雄、藤田公和 ほか、「女子短大生(栄養士専攻)の栄養補助食品(サプリメント)利用と栄養・食物摂取状況について」 名古屋文理短期大学紀要 28, 31-37, 2004-04-01, {{naid|110004499409}}</ref>として利用されている<ref name=jos1956.40.974>矢澤一良、影山治夫、[https://www.jstage.jst.go.jp/article/jos1956/40/10/40_10_974/_article/-char/ja/ ドコサヘキサエン酸の生理活性] 油化学 Vol.40 (1991) No.10 P.974-978, {{DOI|10.5650/jos1956.40.974}}</ref><ref>池本敦、「オメガ3脂肪酸の健康食品・サプリメントとしての実態と利用法」 秋田大学教育文化学部研究紀要 69,121-129(2014), {{hdl|10295/2440}}</ref> |
||
。 |
|||
== 生産 == |
== 生産 == |
||
| 34行目: | 35行目: | ||
もうひとつの経路は、[[ペルオキシソーム]]あるいは[[ミトコンドリア]]中で進行すると考えられているもので、[[エイコサペンタエン酸]]が2回2炭素増炭されて (24:5 ω-3) となった後、Δ6-不飽和化酵素により不飽和化されて (24:6 ω-3) となり、その後[[β酸化]]によって炭素鎖が切断されDHAが生成する。この経路は"Sprecher's shunt" として知られている。 |
もうひとつの経路は、[[ペルオキシソーム]]あるいは[[ミトコンドリア]]中で進行すると考えられているもので、[[エイコサペンタエン酸]]が2回2炭素増炭されて (24:5 ω-3) となった後、Δ6-不飽和化酵素により不飽和化されて (24:6 ω-3) となり、その後[[β酸化]]によって炭素鎖が切断されDHAが生成する。この経路は"Sprecher's shunt" として知られている。 |
||
==摂取== |
== 摂取 == |
||
「[[日本人の食事摂取基準]](2010年版)」ではエイコサペンタエン酸 |
「[[日本人の食事摂取基準]](2010年版)」ではエイコサペンタエン酸(EPA)やドコサヘキサエン酸については1日に合計で1g以上の摂取が望ましいとされている<ref>「[http://www.mhlw.go.jp/shingi/2009/05/dl/s0529-4g.pdf 脂質]」『[http://www.mhlw.go.jp/shingi/2009/05/s0529-4.html 日本人の食事摂取基準」(2010年版)]』pp77-108</ref>。[[魚油]]食品、[[タラ]]、[[ニシン]]、[[サバ]]、[[サケ]]、[[イワシ]]、[[ナンキョクオキアミ]]は、エイコサペンタエン酸やドコサヘキサエン酸のようなω-3脂肪酸に富んでいる。 |
||
1日3g以上のDHAの摂取で、凝血能が低下し出血傾向が起きることがある<ref>{{cite journal |author=Liebich HM, Wirth C, Jakober B |title=Analysis of polyunsaturated fatty acids in blood serum after fish oil administration |journal=J. Chromatogr. |volume=572 |issue=1-2 |pages=1–9 |year=1991 |month=December |pmid=1840144}}</ref>。 |
1日3g以上のDHAの摂取で、凝血能が低下し出血傾向が起きることがある<ref>{{cite journal |author=Liebich HM, Wirth C, Jakober B |title=Analysis of polyunsaturated fatty acids in blood serum after fish oil administration |journal=J. Chromatogr. |volume=572 |issue=1-2 |pages=1–9 |year=1991 |month=December |pmid=1840144}}</ref>。 |
||
魚介類100g中の主な脂肪酸については[[魚介類の脂肪酸]]を参照のこと。 |
魚介類100g中の主な脂肪酸については'''[[魚介類の脂肪酸]]'''を参照のこと。 |
||
== |
== 生理作用 == |
||
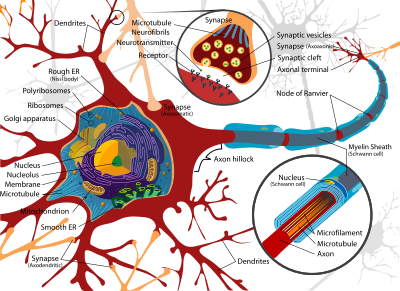
[[Image:Complete neuron cell diagram en.svg|thumb|400px|'''[[神経細胞]]の構造図''' |
[[Image:Complete neuron cell diagram en.svg|thumb|400px|'''[[神経細胞]]の構造図''' |
||
[[:en:Dendrites]]=[[樹状突起]]、[[:en:Axon]]=[[軸索]]、(以下略)]] |
[[:en:Dendrites]]=[[樹状突起]]、[[:en:Axon]]=[[軸索]]、(以下略)]] |
||
[[細胞膜]]は流動性を持ち、脂質や膜タンパクは動いている。この流動性は膜の構成物質で決まる。たとえば、[[リン脂質]]を構成する脂肪酸の不飽和度(二重結合の数)に影響され、二重結合を持つ炭化水素が多いほど(二重結合があるとその部分で炭化水素が折れ曲がるので)リン脂質の相互作用が低くなり流動性は増すことになる。例えばDHAは不飽和度が極めて高く細胞膜の流動性の保持に寄与している |
[[細胞膜]]は流動性を持ち、脂質や膜タンパクは動いている。この流動性は膜の構成物質で決まる。たとえば、[[リン脂質]]を構成する脂肪酸の不飽和度(二重結合の数)に影響され、二重結合を持つ炭化水素が多いほど(二重結合があるとその部分で炭化水素が折れ曲がるので)リン脂質の相互作用が低くなり流動性は増すことになる。例えばDHAは不飽和度が極めて高く細胞膜の流動性の保持に寄与している。 |
||
DHAは[[精液]]や[[脳]]、[[網膜]]の[[リン脂質]]に含まれる[[脂肪酸]]の主要な成分である。DHAは脳内にもっとも豊富に存在する長鎖不飽和脂肪酸で、EPAは脳内にほとんど存在しない<ref name=tsubono>{{cite journal |author=Quinn JF, Raman R, Thomas RG, ''et al.'' |title=Docosahexaenoic acid supplementation and cognitive decline in Alzheimer disease: a randomized trial |journal=JAMA |volume=304 |issue=17 |pages=1903–11 |year=2010 |month=November |pmid=21045096 |pmc=3259852 |doi=10.1001/jama.2010.1510}}</ref>。これは投与されたEPAは脳内に移行したのち,速やかにDPAさらにはDHAに変換されるためであることが指摘されている<ref>J. Ishiguro, T. Tada, T. Ogihara, N. Ohzawa, K. Murakami and H. Kosuzume. "Metabolic Disposition of Ethyl Eicosapentaenoate and Its Metabolites in Rats and Dogs" Journal of pharmacobio-dynamics 11(4),1988-04, 251-261. {{NAID|110003636862}}</ref>。他方、ラットの動物実験で脳のリン脂質においてDHAを摂食すると脳リン脂質中のDHAの割合は増加したが、DPA及びEPAは摂食しても脳のリン脂質脂肪酸組成にはほとんど影響を及ぼさなかったことから、DHAは[[脳関門]]を通過できるが、EPAを含めた他の[[ω-3脂肪酸]]は脳関門を通過することができない可能性が示唆されている<ref>高橋尚子[http://ir.library.tohoku.ac.jp/re/bitstream/10097/34639/1/Takahashi-Shoko-04-08-0072.pdf ラットにおける n-3 および n-6 系多価不飽和脂肪酸の生理作用に関する研究((修士論文)]</ref>。また、ヒトのモデル細胞実験で各種脂肪酸によるDHA取り込みに対する阻害効果を検討した結果、[[リノール酸]]、[[アラキドン酸]]及びエイコサペンタエン酸 |
DHAは[[精液]]や[[脳]]、[[網膜]]の[[リン脂質]]に含まれる[[脂肪酸]]の主要な成分である。DHAは脳内にもっとも豊富に存在する長鎖不飽和脂肪酸で、EPAは脳内にほとんど存在しない<ref name=tsubono>{{cite journal |author=Quinn JF, Raman R, Thomas RG, ''et al.'' |title=Docosahexaenoic acid supplementation and cognitive decline in Alzheimer disease: a randomized trial |journal=JAMA |volume=304 |issue=17 |pages=1903–11 |year=2010 |month=November |pmid=21045096 |pmc=3259852 |doi=10.1001/jama.2010.1510}}</ref>。これは投与されたEPAは脳内に移行したのち,速やかにDPAさらにはDHAに変換されるためであることが指摘されている<ref>J. Ishiguro, T. Tada, T. Ogihara, N. Ohzawa, K. Murakami and H. Kosuzume. "Metabolic Disposition of Ethyl Eicosapentaenoate and Its Metabolites in Rats and Dogs" Journal of pharmacobio-dynamics 11(4),1988-04, 251-261. {{NAID|110003636862}}</ref>。他方、ラットの動物実験で脳のリン脂質においてDHAを摂食すると脳リン脂質中のDHAの割合は増加したが、DPA及びEPAは摂食しても脳のリン脂質脂肪酸組成にはほとんど影響を及ぼさなかったことから、DHAは[[脳関門]]を通過できるが、EPAを含めた他の[[ω-3脂肪酸]]は脳関門を通過することができない可能性が示唆されている<ref>高橋尚子、{{PDFli nk|[http://ir.library.tohoku.ac.jp/re/bitstream/10097/34639/1/Takahashi-Shoko-04-08-0072.pdf ラットにおける n-3 および n-6 系多価不飽和脂肪酸の生理作用に関する研究((修士論文)]}} , {{hdl|10097/34639}}</ref>。また、ヒトのモデル細胞実験で各種脂肪酸によるDHA取り込みに対する阻害効果を検討した結果、[[リノール酸]]、[[アラキドン酸]]及びエイコサペンタエン酸(EPA)によって阻害され、[[オレイン酸]]によって阻害されなかった。従って、DHAは何らかの脂肪酸選択的な輸送機構を介して取り込まれることが示唆されている<ref>「[http://kaken.nii.ac.jp/d/p/20650125.ja.html 健全な神経発達の為に新生児の血液脳関門がもつ機能性脂質供給ルート解明と投与設計]」 研究期間2008年度〜2009年度 (科学研究費助成事業データベース)</ref>。 |
||
DHAの摂取は[[血]]中の[[中性脂肪]]([[トリグリセライド]])量を減少させ、[[心臓病]]の危険を低減する。また、DHAが不足すると脳内[[セロトニン]]の量が減少し、[[注意欠陥・多動性障害|多動性障害]]を引き起こすという報告がある<ref>{{cite journal |author=Richardson AJ |title=Omega-3 fatty acids in ADHD and related neurodevelopmental disorders |journal=Int Rev Psychiatry |volume=18 |issue=2 |pages=155-72 |year=2006 |month=April |pmid=16777670 |doi=10.1080/09540260600583031}}</ref> |
DHAの摂取は[[血]]中の[[中性脂肪]]([[トリグリセライド]])量を減少させ、[[心臓病]]の危険を低減する。また、DHAが不足すると脳内[[セロトニン]]の量が減少し、[[注意欠陥・多動性障害|多動性障害]]を引き起こすという報告がある<ref>{{cite journal |author=Richardson AJ |title=Omega-3 fatty acids in ADHD and related neurodevelopmental disorders |journal=Int Rev Psychiatry |volume=18 |issue=2 |pages=155-72 |year=2006 |month=April |pmid=16777670 |doi=10.1080/09540260600583031}}</ref>。[[アルツハイマー型痴呆]]<ref>{{cite journal|last1=Oksman|first1=M.|last2=Iivonen|first2=H.|last3=Hogyes|first3=E.|last4=Amtul|first4=Z.|last5=Penke|first5=B.|last6=Leenders|first6=I.|last7=Broersen|first7=L.|last8=Lütjohann|first8=D.|last9=Hartmann|first9=T.|last10=Tanila|first10=H.|title=Impact of different saturated fatty acid, polyunsaturated fatty acid and cholesterol containing diets on beta-amyloid accumulation in APP/PS1 transgenic mice|journal=Neurobiology of Disease|volume=23|issue=3|year=2006|pages=563–572|issn=09699961|doi=10.1016/j.nbd.2006.04.013}}</ref>, <ref>{{cite journal |author=Uauy R, Dangour AD |title=Nutrition in brain development and aging: role of essential fatty acids |journal=Nutr. Rev. |volume=64 |issue=5 Pt 2 |pages=S24–33; discussion S72–91 |year=2006 |month=May |pmid=16770950}}</ref>や[[うつ病]]などの[[疾病]]に対してもDHAの摂取は有効であるといわれている。{{要出典|date=2013年12月}}一方で、DHA投与がアルツハイマー病の症状を改善しなかったとの報告<ref name=tsubono/>や悪玉コレステロールの[[LDL]]を大幅に上昇させることがわかっている。 |
||
=== === |
|||
| ⚫ | |||
うつ病が20世紀になって増加しているが、うつ病の増加と[[ω-6脂肪酸]]を多く含む[[植物油]]の摂取が増加したことと<!-- 軌を一にする -->の関連を指摘する意見が幾つか見受けられる。{{要出典|date=2013年12月}} |
|||
| ⚫ | |||
日本の患者数の年度ごとの増加傾向には、高齢化やうつ病についての啓発活動による受診率の増加が原因としてあげられる。<ref>[http://www.secretariat.ne.jp/jsmd/qa/pdf/qa1.pdf うつ病の患者さんは増加しているのでしょうか? 日本うつ病学会]</ref> |
|||
| ⚫ | |||
うつ病が20世紀になって増加しているが、うつ病の増加と[[ω-6脂肪酸]]を多く含む[[植物油]]の摂取が増加したこととの関連を指摘する意見<ref>柳澤厚生,田地野和宏:脂肪酸と自律神経:視点を変えて食を考える,杏林医会誌,35 (4),375-378,2004.</ref>が幾つか見受けられる<ref name=okada>岡田斉、萩谷久美子、石原俊一 ほか、{{PDFlink|[http://sucra.saitama-u.ac.jp/modules/xoonips/download.php/BKK0000304.pdf?file_id=15917 Omega-3 多価不飽和脂肪酸の摂取とうつを中心とした精神的健康との関連性について探索的検討-最近の研究動向のレビューを中心に]}} 人間科学 2008</ref>。一方、日本の患者数の年度ごとの増加傾向には、高齢化やうつ病についての啓発活動による受診率の増加が原因としてあげられる<ref>[http://www.secretariat.ne.jp/jsmd/qa/pdf/qa1.pdf うつ病の患者さんは増加しているのでしょうか? 日本うつ病学会]</ref>が解明は不十分である<ref name=okada /><ref>池谷昌枝、島田凉子、庄子和夫和夫、[https://www.jstage.jst.go.jp/article/jhas/10/2/10_75/_article/-char/ja/ 【原著論文】大学生の心理的ストレスへの応答における食事によるn-6/n-3系多価不飽和脂肪酸の摂取比率の影響] 心身健康科学 Vol.10 (2014) No.2 p.75-85, {{DOI|10.11427/jhas.10.75}}</ref>。ω-3脂肪酸の摂取がうつ病の治療に効果があるか、日本でのエビデンスは希薄である<ref name="nutsu2012">[http://www.secretariat.ne.jp/jsmd/mood_disorder/img/120726.pdf 日本うつ病学会治療ガイドライン. II.大うつ病性障害 2012 Ver.1. 平成24年7月26日]</ref>。 |
|||
うつ病患者においてはω-6脂肪酸から[[アラキドン酸]]を経て生成される炎症性の生理活性物質である[[エイコサノイド]]のレベルが高いということが示されている<ref>{{cite journal |author=Smith RS |title=The macrophage theory of depression |journal=Med. Hypotheses |volume=35 |issue=4 |pages=298–306 |year=1991 |month=August |pmid=1943879}}</ref><ref>{{cite journal |author=Hibbeln JR, Salem N |title=Dietary polyunsaturated fatty acids and depression: when cholesterol does not satisfy |journal=Am. J. Clin. Nutr. |volume=62 |issue=1 |pages=1–9 |year=1995 |month=July |pmid=7598049}}</ref>。シーフードをたくさん摂取するところほど[[母乳]]内のDHAは高く、産後うつ病の有病率は低かった。母体から胎児への転送により、妊娠・出産期には母親には無視できないω-3脂肪酸の枯渇の危険性が高まり、その結果として産後のうつ病の危険性に関与する可能性がある。健常者と比較してうつ病患者はω-3脂肪酸の蓄積量が有意に低くω-6とω-3の比率は有意に高かったことが指摘されている<ref name=saitama/>。 |
うつ病患者においてはω-6脂肪酸から[[アラキドン酸]]を経て生成される炎症性の生理活性物質である[[エイコサノイド]]のレベルが高いということが示されている<ref>{{cite journal |author=Smith RS |title=The macrophage theory of depression |journal=Med. Hypotheses |volume=35 |issue=4 |pages=298–306 |year=1991 |month=August |pmid=1943879}}</ref><ref>{{cite journal |author=Hibbeln JR, Salem N |title=Dietary polyunsaturated fatty acids and depression: when cholesterol does not satisfy |journal=Am. J. Clin. Nutr. |volume=62 |issue=1 |pages=1–9 |year=1995 |month=July |pmid=7598049}}</ref>。シーフードをたくさん摂取するところほど[[母乳]]内のDHAは高く、産後うつ病の有病率は低かった。母体から胎児への転送により、妊娠・出産期には母親には無視できないω-3脂肪酸の枯渇の危険性が高まり、その結果として産後のうつ病の危険性に関与する可能性がある。健常者と比較してうつ病患者はω-3脂肪酸の蓄積量が有意に低くω-6とω-3の比率は有意に高かったことが指摘されている<ref name=saitama/>。 |
||
== 牛の脳(100g中)の主な脂肪酸の種類 == |
|||
| ⚫ | |||
男性より女性のほうが2倍ほどうつ病になりやすいとされている<ref>[[厚生労働省]] [http://www.mhlw.go.jp/shingi/2004/01/dl/s0126-5a.doc うつ病対策推進方策マニュアル(doc)]</ref>。 |
|||
女性の発症率の高さについては、妊娠・出産期・閉経期・月経前([[PMS]]、[[PMDD]]、[[セロトニン]]の減少)の女性ホルモン、[[セロトニン]]の激減がマタニティブルーや産後うつに関与している可能性がある。産後うつは乳児の育児時の[[睡眠]]不足もある。<ref>[http://www.jcptd.jp/public/kind_utsu_2.html#ku07 女性のうつ病 JCPTD]</ref>日本ではうつ病が増加傾向にあるが、女性の高齢化による自然増もある。 |
|||
ω-3脂肪酸の摂取がうつ病の治療に効果があるか、日本でのエビデンスは希薄である。<ref name="nutsu2012">[http://www.secretariat.ne.jp/jsmd/mood_disorder/img/120726.pdf 日本うつ病学会治療ガイドライン. II.大うつ病性障害 2012 Ver.1. 平成24年7月26日]</ref> |
|||
{| class="wikitable" style="float:right" |
{| class="wikitable" style="float:right" |
||
|+ 牛の脳(100g中)の主な[[脂肪酸]]の種類<ref name=ndb>[http://ndb.nal.usda.gov/ USDA National Nutrient Database]</ref> |
|+ 牛の脳(100g中)の主な[[脂肪酸]]の種類<ref name=ndb>[http://ndb.nal.usda.gov/ USDA National Nutrient Database]</ref> |
||
| 119行目: | 115行目: | ||
| 20:4(未同定) || 0.47 |
| 20:4(未同定) || 0.47 |
||
|- |
|- |
||
| 22:5 n-3([[ドコサペンタエン酸]] |
| 22:5 n-3([[ドコサペンタエン酸]](DPA)) || 0.22 |
||
|- |
|- |
||
| 22:6 n-3('''ドコサヘキサエン酸''' |
| 22:6 n-3('''ドコサヘキサエン酸'''(DHA)) || 0.45 |
||
|} |
|} |
||
{{-}} |
|||
==参考文献== |
== 参考文献 == |
||
{{Reflist|2}} |
|||
<references /> |
|||
==関連項目== |
== 関連項目 == |
||
* [[必須脂肪酸]] |
* [[必須脂肪酸]] |
||
==外部リンク== |
== 外部リンク == |
||
* [http://hfnet.nih.go.jp/contents/indiv_agreement.html?32 DHA(ドコサヘキサエン酸) -「健康食品」の安全性・有効性情報]([[国立健康・栄養研究所]]) |
* [http://hfnet.nih.go.jp/contents/indiv_agreement.html?32 DHA(ドコサヘキサエン酸) -「健康食品」の安全性・有効性情報]([[国立健康・栄養研究所]]) |
||
* 橋本道男、[https://www.jstage.jst.go.jp/article/oleoscience/6/2/6_67/_article/-char/ja/ ドコサヘキサエン酸による脳機能改善作用と神経疾患への応用] オレオサイエンス Vol.6 (2006) No.2 p.67-76, {{DOI|10.5650/oleoscience.6.67}} |
|||
{{脂肪酸}} |
{{脂肪酸}} |
||
2016年12月12日 (月) 09:01時点における版
この記事には独自研究が含まれているおそれがあります。 |
| ドコサヘキサエン酸 | |
|---|---|
| IUPAC名 | (4Z,7Z,10Z,13Z,16Z,19Z)-ドコサ-4,7,10,13,16,19-ヘキサエン酸 |
| 別名 | DHA、セルボン酸 |
| 分子式 | C22H32O2 |
| 分子量 | 328.49 |
| CAS登録番号 | 6217-54-5 |
| 形状 | 無色油状 |
| 融点 | -44 °C |

ドコサヘキサエン酸(ドコサヘキサエンさん、Docosahexaenoic acid、略称 DHA )は、不飽和脂肪酸のひとつ。分子式 C22H32O2、示性式 CH3CH2(CH=CHCH2)6CH2COOH で、6つの二重結合を含む22個の炭素鎖をもつカルボン酸 (22:6) の総称であるが、通常は生体にとって重要な 4, 7, 10, 13, 16, 19 位に全てシス型の二重結合をもつ、ω-3脂肪酸に分類される化合物を指す。
魚油に多く含まれ、日本人は魚類を食べることによって多く摂取していたが近年は減少している。 ヒトでは、体内で合成できないα-リノレン酸から体内でDHAを合成するため、広義では必須脂肪酸となる。生理活性効果に関して1980年代から積極的な研究が行われ、EPAと同様に食品添加物や健康補助食品[1]として利用されている[2][3] 。
生産
魚やその他の生物に含まれるDHAの多くは、ラビリンチュラ類の1属である Schizochytrium 属などのような海産の微生物によって生産されたものが、食物連鎖の過程で濃縮されたものである。多くの動物は体内でα-リノレン酸を原料としてEPAやDHAを生産することができるが、α-リノレン酸からEPAやDHAに変換される割合は10-15%程度である[4]。
ヒトでは、DHAは食品から摂取される以外に、2つの経路によって代謝生産される[5]。どちらも出発原料はα-リノレン酸であるが、中間生成物が異なる。
ひとつはエイコサペンタエン酸 (20:5, ω-3) を原料とし、エロンガーゼによって2炭素増炭されドコサペンタエン酸 (22:5 ω-3) がつくられた後、Δ4-不飽和化酵素によって水素が引き抜かれて生成する過程である。
もうひとつの経路は、ペルオキシソームあるいはミトコンドリア中で進行すると考えられているもので、エイコサペンタエン酸が2回2炭素増炭されて (24:5 ω-3) となった後、Δ6-不飽和化酵素により不飽和化されて (24:6 ω-3) となり、その後β酸化によって炭素鎖が切断されDHAが生成する。この経路は"Sprecher's shunt" として知られている。
摂取
「日本人の食事摂取基準(2010年版)」ではエイコサペンタエン酸(EPA)やドコサヘキサエン酸については1日に合計で1g以上の摂取が望ましいとされている[6]。魚油食品、タラ、ニシン、サバ、サケ、イワシ、ナンキョクオキアミは、エイコサペンタエン酸やドコサヘキサエン酸のようなω-3脂肪酸に富んでいる。 1日3g以上のDHAの摂取で、凝血能が低下し出血傾向が起きることがある[7]。
魚介類100g中の主な脂肪酸については魚介類の脂肪酸を参照のこと。
生理作用
細胞膜は流動性を持ち、脂質や膜タンパクは動いている。この流動性は膜の構成物質で決まる。たとえば、リン脂質を構成する脂肪酸の不飽和度(二重結合の数)に影響され、二重結合を持つ炭化水素が多いほど(二重結合があるとその部分で炭化水素が折れ曲がるので)リン脂質の相互作用が低くなり流動性は増すことになる。例えばDHAは不飽和度が極めて高く細胞膜の流動性の保持に寄与している。
DHAは精液や脳、網膜のリン脂質に含まれる脂肪酸の主要な成分である。DHAは脳内にもっとも豊富に存在する長鎖不飽和脂肪酸で、EPAは脳内にほとんど存在しない[8]。これは投与されたEPAは脳内に移行したのち,速やかにDPAさらにはDHAに変換されるためであることが指摘されている[9]。他方、ラットの動物実験で脳のリン脂質においてDHAを摂食すると脳リン脂質中のDHAの割合は増加したが、DPA及びEPAは摂食しても脳のリン脂質脂肪酸組成にはほとんど影響を及ぼさなかったことから、DHAは脳関門を通過できるが、EPAを含めた他のω-3脂肪酸は脳関門を通過することができない可能性が示唆されている[10]。また、ヒトのモデル細胞実験で各種脂肪酸によるDHA取り込みに対する阻害効果を検討した結果、リノール酸、アラキドン酸及びエイコサペンタエン酸(EPA)によって阻害され、オレイン酸によって阻害されなかった。従って、DHAは何らかの脂肪酸選択的な輸送機構を介して取り込まれることが示唆されている[11]。
DHAの摂取は血中の中性脂肪(トリグリセライド)量を減少させ、心臓病の危険を低減する。また、DHAが不足すると脳内セロトニンの量が減少し、多動性障害を引き起こすという報告がある[12]。アルツハイマー型痴呆[13], [14]やうつ病などの疾病に対してもDHAの摂取は有効であるといわれている。[要出典]一方で、DHA投与がアルツハイマー病の症状を改善しなかったとの報告[8]や悪玉コレステロールのLDLを大幅に上昇させることがわかっている。
うつ病と脂肪酸に関する議論
うつ病が20世紀になって増加しているが、うつ病の増加とω-6脂肪酸を多く含む植物油の摂取が増加したこととの関連を指摘する意見[15]が幾つか見受けられる[16]。一方、日本の患者数の年度ごとの増加傾向には、高齢化やうつ病についての啓発活動による受診率の増加が原因としてあげられる[17]が解明は不十分である[16][18]。ω-3脂肪酸の摂取がうつ病の治療に効果があるか、日本でのエビデンスは希薄である[19]。
うつ病患者においてはω-6脂肪酸からアラキドン酸を経て生成される炎症性の生理活性物質であるエイコサノイドのレベルが高いということが示されている[20][21]。シーフードをたくさん摂取するところほど母乳内のDHAは高く、産後うつ病の有病率は低かった。母体から胎児への転送により、妊娠・出産期には母親には無視できないω-3脂肪酸の枯渇の危険性が高まり、その結果として産後のうつ病の危険性に関与する可能性がある。健常者と比較してうつ病患者はω-3脂肪酸の蓄積量が有意に低くω-6とω-3の比率は有意に高かったことが指摘されている[4]。
牛の脳(100g中)の主な脂肪酸の種類
| 項目 | 分量(g) |
|---|---|
| 脂肪 | 10.3 |
| 飽和脂肪酸 | 2.3 |
| 16:0(パルミチン酸) | 0.919 |
| 18:0(ステアリン酸) | 1.273 |
| 一価不飽和脂肪酸 | 1.89 |
| 18:1(オレイン酸) | 1.646 |
| 20:1 | 0.222 |
| 多価不飽和脂肪酸 | 1.586 |
| 20:4(未同定) | 0.319 |
| 22:5 n-3(ドコサペンタエン酸(DPA)) | 0.374 |
| 22:6 n-3(ドコサヘキサエン酸(DHA)) | 0.851 |
| 項目 | 分量(g) |
|---|---|
| 脂肪 | 9.21 |
| 飽和脂肪酸 | 2.079 |
| 14:0(ミリスチン酸) | 0.04 |
| 16:0(パルミチン酸) | 1.029 |
| 18:0(ステアリン酸) | 0.999 |
| 一価不飽和脂肪酸 | 1.659 |
| 16:1(パルミトレイン酸) | 0.12 |
| 18:1(オレイン酸) | 1.069 |
| 多価不飽和脂肪酸 | 1.429 |
| 18:2(リノール酸) | 0.09 |
| 18:3(α-リノレン酸) | 0.12 |
| 20:4(未同定) | 0.47 |
| 22:5 n-3(ドコサペンタエン酸(DPA)) | 0.22 |
| 22:6 n-3(ドコサヘキサエン酸(DHA)) | 0.45 |
参考文献
- ^ 加藤恵子、三浦英雄、藤田公和 ほか、「女子短大生(栄養士専攻)の栄養補助食品(サプリメント)利用と栄養・食物摂取状況について」 名古屋文理短期大学紀要 28, 31-37, 2004-04-01, NAID 110004499409
- ^ 矢澤一良、影山治夫、ドコサヘキサエン酸の生理活性 油化学 Vol.40 (1991) No.10 P.974-978, doi:10.5650/jos1956.40.974
- ^ 池本敦、「オメガ3脂肪酸の健康食品・サプリメントとしての実態と利用法」 秋田大学教育文化学部研究紀要 69,121-129(2014), hdl:10295/2440
- ^ a b 岡田斉、萩谷久美子、石原俊一ほか「Omega-3多価不飽和脂肪酸の摂取とうつを中心とした精神的健康との関連性について探索的検討-最近の研究動向のレビューを中心に」『人間科学研究』(30),2008,pp87-96. NAID 120001859287
- ^ R. De Caterina1, and G. Basta, "n-3 Fatty acids and the inflammatory response — biological background", European Heart Journal Supplements (2001), 3 (Supplement D), D42–D49.[1]
- ^ 「脂質」『日本人の食事摂取基準」(2010年版)』pp77-108
- ^ Liebich HM, Wirth C, Jakober B (December 1991). “Analysis of polyunsaturated fatty acids in blood serum after fish oil administration”. J. Chromatogr. 572 (1-2): 1–9. PMID 1840144.
- ^ a b Quinn JF, Raman R, Thomas RG, et al. (November 2010). “Docosahexaenoic acid supplementation and cognitive decline in Alzheimer disease: a randomized trial”. JAMA 304 (17): 1903–11. doi:10.1001/jama.2010.1510. PMC 3259852. PMID 21045096.
- ^ J. Ishiguro, T. Tada, T. Ogihara, N. Ohzawa, K. Murakami and H. Kosuzume. "Metabolic Disposition of Ethyl Eicosapentaenoate and Its Metabolites in Rats and Dogs" Journal of pharmacobio-dynamics 11(4),1988-04, 251-261. NAID 110003636862
- ^ 高橋尚子、Template:PDFli nk , hdl:10097/34639
- ^ 「健全な神経発達の為に新生児の血液脳関門がもつ機能性脂質供給ルート解明と投与設計」 研究期間2008年度〜2009年度 (科学研究費助成事業データベース)
- ^ Richardson AJ (April 2006). “Omega-3 fatty acids in ADHD and related neurodevelopmental disorders”. Int Rev Psychiatry 18 (2): 155-72. doi:10.1080/09540260600583031. PMID 16777670.
- ^ Oksman, M.; Iivonen, H.; Hogyes, E.; Amtul, Z.; Penke, B.; Leenders, I.; Broersen, L.; Lütjohann, D. et al. (2006). “Impact of different saturated fatty acid, polyunsaturated fatty acid and cholesterol containing diets on beta-amyloid accumulation in APP/PS1 transgenic mice”. Neurobiology of Disease 23 (3): 563–572. doi:10.1016/j.nbd.2006.04.013. ISSN 09699961.
- ^ Uauy R, Dangour AD (May 2006). “Nutrition in brain development and aging: role of essential fatty acids”. Nutr. Rev. 64 (5 Pt 2): S24–33; discussion S72–91. PMID 16770950.
- ^ 柳澤厚生,田地野和宏:脂肪酸と自律神経:視点を変えて食を考える,杏林医会誌,35 (4),375-378,2004.
- ^ a b 岡田斉、萩谷久美子、石原俊一 ほか、{{{1}}} (PDF) 人間科学 2008
- ^ うつ病の患者さんは増加しているのでしょうか? 日本うつ病学会
- ^ 池谷昌枝、島田凉子、庄子和夫和夫、【原著論文】大学生の心理的ストレスへの応答における食事によるn-6/n-3系多価不飽和脂肪酸の摂取比率の影響 心身健康科学 Vol.10 (2014) No.2 p.75-85, doi:10.11427/jhas.10.75
- ^ 日本うつ病学会治療ガイドライン. II.大うつ病性障害 2012 Ver.1. 平成24年7月26日
- ^ Smith RS (August 1991). “The macrophage theory of depression”. Med. Hypotheses 35 (4): 298–306. PMID 1943879.
- ^ Hibbeln JR, Salem N (July 1995). “Dietary polyunsaturated fatty acids and depression: when cholesterol does not satisfy”. Am. J. Clin. Nutr. 62 (1): 1–9. PMID 7598049.
- ^ a b USDA National Nutrient Database
関連項目
外部リンク
- DHA(ドコサヘキサエン酸) -「健康食品」の安全性・有効性情報(国立健康・栄養研究所)
- 橋本道男、ドコサヘキサエン酸による脳機能改善作用と神経疾患への応用 オレオサイエンス Vol.6 (2006) No.2 p.67-76, doi:10.5650/oleoscience.6.67
