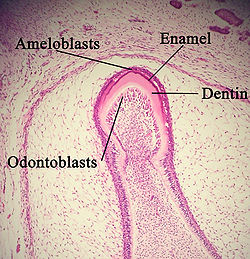
エナメル質
| 歯 |
|---|
 |
| A-歯冠 |
| 1-エナメル質 2-象牙質 3-歯髄 4-歯肉 |
| B-歯根 |
| 5-セメント質 6-歯槽骨 7-血管 8-神経 |
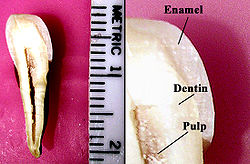
エナメル質(エナメルしつ、enamel)または琺瑯質(ほうろうしつ)は、歯の歯冠の最表層にある、生体で最も硬い硬組織[1][2][3] である。硬さを表すモース硬度は6 - 7を示す[2]。
このエナメル質と、象牙質、セメント質、歯髄により歯が構成される[4]。通常、目に見える部分がこのエナメル質であり、象牙質に支えられている。象牙質の支持がなければエナメル質は硬くて脆いため容易に割れてしまう[5]。重量比で96%は無機質で残りが水と有機質であり[6]、色は明黄色からネズミ色がかった白色である。エナメル質の下に象牙質がない端の部分では、青みがかって見えることもある。半透明であるので、エナメル質の下にある象牙質や歯科修復材料の色が歯の外見に強く影響を与える。厚さは部位により異なり、多くの場合、切端部や咬合部で最も厚く(2.5mm以上)、歯頸部(セメント・エナメル境)で最も薄い[2][7]。
名称の変遷[編集]
現在では「エナメル質」が一般的だが、1940年代までの日本では「琺瑯質(ほうろうしつ)」という用語が一般的だった。「エナメル質」が用いられ始めたのは1950年代からで、特に藤田恒太郎『歯の組織学』(1957)の影響が大きい。「琺瑯質」から「エナメル質」に切り替わった時期は大学ごとに異なる。例えば、鶴見大学歯学部では松井隆弘教授により1981年まで「ほうろう質」が、東京歯科大学では1994年まで「琺瑯質」が使用され、そのあと「エナメル質」に切り替わった[8]。同様に「セメント質」も「白亜質」に変わったが、「象牙質」のみはそのままだった[9]。歯科医の浮谷英邦は東歯大時代の講義において、教授から用語は不適切だが時代の流れなので国家試験で「エナメル質」「セメント質」と出題されても我慢するようにと言われたという[9]。
エナメル質から琺瑯質へ用語が切り替わった時期についてネット上には誤った俗説、例えば「エナメル質は戦時中、敵性語と見なされ琺瑯質と言い換えられた」あるいは「帝銀事件の犯人が琺瑯質という用語を使ったのは真犯人が東京歯科大学の前身の関係者である証拠」など間違った言説が数多く見られるので、注意を要する。
構造[編集]

下はセメント質。
エナメル質の基本構造はエナメル小柱と呼ばれている[5]。エナメル小柱は組織化されたパターンの中に多くの水酸燐灰石の結晶が入っている[1]。断面は、頭を外側に、下を内側においた鍵穴のように見える。
エナメル小柱の中の水酸燐灰石の結晶の配置は非常に複雑となっている。エナメル質を作るエナメル芽細胞とトームス突起(英語: Tomes' process) の両方が結晶のパターンに影響を与える。エナメル小柱頭部の結晶は小柱の長軸に完全に平行となっている[1][7] が、尾部では方向が長軸とややずれる[1]。
エナメル小柱の配置は内部構造よりも理解しやすい。エナメル小柱は歯に沿って列を作り、象牙質に垂直に配置されている[10]。永久歯では、エナメル-セメント境付近のエナメル小柱はわずかに歯根の方に傾く。象牙質の支持を受けないエナメル質は破折しやすいので、歯の保存修復においてエナメル質の走行を理解することは重要である[10][11]。
エナメル小柱の周りはエナメル小柱間質として知られている。エナメル小柱間質はエナメル小柱と同じ構成を持っているが、結晶の方向が異なるので、組織学的に区別される[7]。エナメル小柱間質とエナメル小柱の結晶が合う境界は、エナメル小柱鞘と呼ばれる[12]。
顕微鏡でエナメル質の断面を見たときに見える縞をレチウス条と呼ぶ[10]。トームス突起の直径の変化によって起こるこれらの縞は、木の年輪のようにエナメル質の成長を示す[13]。レチウス条が表層に出た所に、周波条(英語: Perikymata) と呼ばれる浅い溝が見える[14][15]。新産線は他の縞より暗く出生前後の境界を示す[16]。また、反射光を用いて顕微鏡でエナメル質を見た際に現れる明帯と暗帯が交互に並ぶ領域を、ハンター・シュレーゲル条(英語: Hunter-Schreger band) と呼ぶ[17]。これは小柱の走行の変化により起こる光学的現象であり、光の方向が変わると明帯と暗帯は逆転する[17]。
境界部[編集]
歯頸部にあるエナメル質とセメント質の境界をエナメル-セメント境(セメント-エナメル境とも)と呼び、これは解剖学的歯頸線と一致する。歯頸線は唇(頬)側および舌(口蓋)側では歯根側に凸弯し、近心側および遠心側では歯冠側に凸弯する[18]。拡大して見た場合、滑らかな曲線ではなく、鋸歯のような複雑な形を示す[19]。境界部でエナメル質とセメント質は約30%が移行的に連続するが、約60%はセメント質がエナメル質を覆い、約10%が連続せずに象牙質が露出している[20][21]。エナメル質を覆っている部分のセメント質はセメント舌と呼ぶ[21]。また、大臼歯では、歯頸部から歯根部にかけて球状のエナメル質塊が存在することがあり、これをエナメル滴と呼ぶ[22]。
エナメル質と象牙質の境界をエナメル象牙境と呼ぶ。横断研磨標本において、同部を調べると、一定の間隔でエナメル小柱が蛇行、ねじれ弯曲などのために暗くなっている部分があり、これを エナメル叢(英語: Enamel tufts) と、エナメル象牙境からエナメル質表層まで向かう薄板状の構造を エナメル葉 と、象牙質側からの紡錘状の侵入物を エナメル紡錘 と呼び、これらの部分は石灰化度が低く有機物が多い[11][23]。
構成成分[編集]
無機質は大部分がリン酸カルシウムの結晶である[5][24]。他に、炭酸塩やクエン酸塩(英語: Citrate)、乳酸塩のほか、フッ素、ナトリウム、クロム、マグネシウム、亜鉛、鉛、銅、鉄、スズ、コバルト、ストロンチウム、マンガン、アルミニウム、ケイ素、銀など、約40種類の微少元素が含まれる[25][26]。微少元素の構成割合はエナメル質の深さ、加齢、地理的条件によって異なる[27]。無機質が多いため、エナメル質は硬いが脆い[28][29]。エナメル質と比較すると、象牙質は結晶化の程度が低く、硬さは低いが、脆さも低く、エナメル質を支えるのに必要であり、象牙質の支えのないエナメル質は容易に破折する[5]。無機質の割合が高いために、組織学的研究のために標本を作る場合、通常の脱灰法では融解して形を留めず[30]、光線顕微鏡の標本は通常切削標本である。
有機質について特徴的なこととして、象牙質や骨と異なり、エナメル質はコラーゲンを含まず、代わりにアメロゲニン、エナメリンなどのエナメルタンパクが含まれていることが挙げられる。これらの蛋白質の役割は完全には判明していないが、いくつかの機能の一つとして、エナメル質形成期の構造の形成を助けるという機能があると考えられており[31]、アメロゲニン遺伝子の異常がエナメル質形成不全症を引き起こすことが分かっている[32]。他に、脂質が有機質の半分を占める[33] ほか、クエン酸・乳酸なども含まれている[33]。
物性[編集]
エナメル質はモース硬度6 - 7[2]、ヌープ硬度300[34] - 451[35]、ビッカース硬さ408[35] と高い硬度を示す。部位により硬度はかわり、切縁・咬頭側、表層側の硬度が高い[36]。この代わりに脆い[28][29]。
発生[編集]
| 発生途上の歯を示す組織学のスライド (スライドの上方が口) |
|---|
エナメル質の形成は歯の発生の一過程である。発生途上の歯を顕微鏡で見たとき、エナメル器、歯堤(英語: Dental lamina)、歯乳頭などとして知られる細胞の集まりを確認することができる[37]。一般的に歯の発生段階は、蕾状期、帽状期、鐘状期となる。エナメル質の形成は鐘状期の後期から行われる。
エナメル器より起こる内エナメル上皮がエナメル芽細胞となりこれが象牙質の形成開始後にエナメル質の形成を始める。人間のエナメル質は妊娠三 - 四月の時から、切端、咬頭の側から順に、一日あたり4マイクロメートルずつ成長していく[10]。エナメル芽細胞は口腔の上皮が落ち込んでできたものであり、このため、エナメル質は歯の他の組織(中胚葉性)と異なり、外胚葉性のものである[38]。
全ての人間のプロセス同様、エナメル質の生成も複雑であるが、一般的に2つの段階に分けられる[39]。分泌相と呼ばれる第一段階は、タンパク質や部分的に石灰化した有機質を含んでおり、有機質の分泌と成長の進行を行っている。成熟相と呼ばれる第二段階は厚さの成長が止まってから完全に成熟までの期間で、主にエナメル質の石灰化が進行する。
| エナメル質の発生を示す組織学のスライド |
|---|
分泌相ではエナメル芽細胞は極性を持つ円柱状の細胞である。この細胞の粗面小胞体では、エナメルタンパクが周囲に産出し、エナメル質基質がアルカリフォスファターゼ酵素により部分的に石灰化するのに寄与している[40] 。
この第一層が形成されると、エナメル芽細胞は象牙質から離れ、先端部にトームス突起が形成される。エナメル質の形成は隣接したエナメル芽細胞で続けられ、その結果トームス突起を保護するように、壁に囲まれたくぼみができる。また、トームス突起の縁でもエナメル質が形成され、くぼみの中にエナメル母体が析出する[41]。 くぼみのエナメル母体は棒状になり、くぼみを囲む芽細胞の壁も最終的に棒同士を繋ぐエナメルになる。棒状のエナメル質と棒同士を繋ぐエナメル質は、カルシウム結晶の方向だけが異なる。
成熟相では、エナメル芽細胞がエナメルの形成に必要な物質を運ぶ。組織学的にいって最も注目すべきは、エナメル芽細胞が縦に筋を作り始めるという点である[40]。これによって、エナメル芽細胞が分泌期のような増殖をやめて運搬機能を発揮し始めたということが分かる。ここで運搬される物質は、石灰化の最終段階に使われるタンパク質がほとんどである。主なものにアメロゲニン、アメロブラスチン、エナメリン、タフテリンなどがある[42]。成熟期において、アメロゲニンとアメロブラスチンは使用された後に除去され、エナメリンとタフテリンだけが残る[43]。
成熟期が終わり、歯が口腔内に萌出する前にエナメル芽細胞はなくなる。このため、エナメル質は体の多くの組織と異なり、う蝕や外傷などによるエナメル質の欠損の後、再生する手段がない[44]。ただし、石灰化自体は唾液中に存在する過飽和のカルシウムとリン酸により萌出後も進行する[45]。
エナメル質は非病理学的な過程に影響されることがある。喫煙やコーヒー、茶などに長期的に触れることにより変色する[46]。エナメル質のみでなく象牙質もであるが、硬化していく[47]。その結果、年をとるほど、歯の色が暗くなっていく。さらに、流動体の浸透性が低下し、酸に解けにくくなり、水分の含有量が減少する[47]。
| 出生時エナメル質形成量 | エナメル質石灰化完了時期 | ||
|---|---|---|---|
| 上顎歯 | 乳中切歯 | 5/6 | 生後1.5か月 |
| 乳側切歯 | 2/3 | 生後2.5か月 | |
| 乳犬歯 | 1/3 | 生後9か月 | |
| 第一乳臼歯 | 咬頭は結合;咬合面は完全に石灰化 歯冠の高さの1/2から3/4まで石灰化 |
生後6か月 | |
| 第二乳臼歯 | 咬頭は結合; 咬合面の石灰化は不完全; 歯冠の高さの1/5から1/4まで石灰化 |
生後11か月 | |
| 下顎歯 | 乳中切歯 | 3/5 | 生後2.5か月 |
| 乳側切歯 | 3/5 | 生後3か月 | |
| 乳犬歯 | 1/3 | 生後9か月 | |
| 第一乳臼歯 | 咬頭は結合; 咬合面は完全に石灰化 | 生後5.5か月 | |
| 第二乳臼歯 | 咬頭は結合; 咬合面の石灰化は不完全 | 生後10か月 | |
乳歯と永久歯におけるエナメル質の違い[編集]
乳歯、永久歯ともにエナメル質の結晶はハイドロキシアパタイト Ca10(PO4)6(OH)2 を最小単位として形成されるが、乳歯のエナメル質は永久歯のエナメル質と比較して結晶粒子が小さく[49]、厚さが1/2でほぼ全体での厚さが等しく1 - 2mmである[49][50]。また含水量が多く(乳歯2.8%、永久歯2.3%)、硬度が低く、化学反応性が大きく、脱灰の影響を受けてのう蝕やフッ化物による歯質強化を受けやすい[49]。
破壊[編集]

エナメル質は無機質が多く、人体で最も硬い組織であるが、いくつかの理由で失われる。
一つは脱灰であり[37]、その最も大きな理由は砂糖の摂取によるう蝕である。
口腔内には多くの種類の細菌(口腔常在菌)が多数含まれており、砂糖の主成分であるスクロースが口腔内に広がった際、一部の口腔常在菌はスクロースに働き、乳酸を産生する。この乳酸が口腔内のpH を低下させる[51] ことでう蝕が進行する。(詳細についてはう蝕の項目を参照)
う蝕が進行し、エナメル質が、細菌の進入を防ぐことができなくなれば、エナメル質の下の象牙質も同様になる。象牙質はう蝕の進行がエナメル質より早く、健全なエナメル質を支持する象牙質がう蝕によって破壊された場合、エナメル質はその脆性のため、容易に歯から破折してしまう。
| 前歯。歯ぎしりのために、通常はエナメル質 の下に隠れている象牙質や歯髄が見える。 |
う蝕のみでなく、吐瀉物に含まれる酸や、工場で空気中に含まれる酸などにより脱灰される場合もあり、これを酸蝕症と呼ぶ[52]。
脱灰で失われるのみでなく、物理的な力により破壊されることも多い。この中で最も知られるものは、歯ぎしり、噛みしめなどによる、エナメル質の破壊であり、非常に早く進行する。咬耗によるエナメル質の減少は正常であれば年間8マイクロメートルである。一般に誤解されていることとして、エナメル質がすりへる主要な原因は咀嚼によるものだということがある。しかし、現実には、歯は咀嚼中滅多に触れ合わない。さらに、正常な咬合であれば、歯根膜や咬合の配置により、生理学的に補われる。本当に破壊的な力は、歯ぎしりのような動作である。これは咬耗症として、エナメル質に復元不可能な損害をもたらす。このほかの破壊の原因として、摩耗症(英語: Abrasion (dental))(歯ブラシのような外的な力による物)、アブフラクション、外傷、中心結節などの歯の形態異常のほか、矯正治療によるブラケット除去時の亀裂などもある[52][53][54]。破折の最も軽い状態である亀裂については、加齢とともに増加し、40歳代以降では95%に見られるという報告や、50歳代以降では全ての歯に見られたとの報告がある[53][55]。
なお、エナメル質を形成するエナメル芽細胞は、歯の萌出時にはすでに存在しないため、一度失われたエナメル質が再生することはない。また、エナメル質には神経が存在しないため、破壊がエナメル質のみに限局している場合、疼痛を感じることもない。
予防[編集]
エナメル質の脱灰の影響や毎日の砂糖の摂取への脅威は大きく、う蝕を予防することは歯の健康を維持し、良質な口腔衛生を保つ大切な方法である。ほとんどの国では、歯ブラシを一般的に使用し、エナメル質上の細菌や食物残渣を減らすことでう蝕を予防している。このほか、デンタルフロスなどを使用することもある。

フッ化物がエナメル質に取り込まれ、耐酸性が向上することでう蝕への抵抗を示す直接的な作用と、う蝕原因菌による解糖過程を抑制することで酸の産生を減少させ、脱灰エナメル質を修復し再石灰化する間接的な作用によりう蝕を予防することが分かっている[56]。このため、水道水フッ化物添加、食塩へのフッ化物濃度調整、フッ化物配合歯磨剤、フッ化物歯面塗布、フッ化物洗口など、多くの手段が用いられる[56][57]。このうち、特に水道水フッ化物添加は多くの面で非常に有効であるが、これについては、反対する人もあり、議論がなされている。
歯ぎしり、噛みしめ等によるエナメル質の破壊を防ぐ方法としては、マウスピースや薬物療法などが知られる。
また、近年では歯科用レーザーである Nd:YAGレーザーや炭酸ガスレーザー、Er:YAGレーザーとフッ化物歯面塗布を併用し、エナメル質の強化や耐酸性の強化を行う研究が進められている[58]。
診断[編集]
エナメル質の状態を診査し、治療の必要性を判断することは重要である。エナメル質のう蝕や物理的な力による破壊に対する診断に最も一般的な方法は視診であるが、確実な診断のために、問診・医療面接による把握や探針やデンタルフロスを用いた触診、咬翼法やオルソパントモグラフ(英語: Orthopantomogram)、歯科用コーンビームCTによるX線診断、光ファイバーを用いた透照診、ダイアグノデントなどのレーザーによる蛍光診断や電気抵抗値を測定する電気診などの方法が用いられる[59][60][61]。
電気診[編集]
健全なエナメル質の電気抵抗は600kΩ以上であるが、エナメル質のう蝕が進行するに連れて電気抵抗が低下し、象牙質まで達すると250kΩ以下(小児では280kΩ以下)となる[59][62]。この電気抵抗をカリエスメーターを使用して測定することで診断する[59]。
レーザーによる蛍光診断[編集]
ダイアグノデントやそれを改良したダイアグノデントペンは、波長655nmの半導体レーザーを利用してエナメル質などの歯質の蛍光強度を非侵襲的に測定することで健全なエナメル質とう蝕エナメル質を区別することができる[63]。特にダイアグノデントペンは隣接面う蝕用のチップを持つことから同部のう蝕の検出に有効であるとされており[64][65]、X線の被曝を可能な限り抑えたい小児歯科や[64]、在宅診療や集団歯科検診などの幅広い分野での診断への利用が期待されている[58]。
エナメル質への歯科処置[編集]

エナメル質を形成するエナメル芽細胞は、歯の萌出時にはすでに存在しないため、一度失われたエナメル質が再生することはない。このため、う蝕等でエナメル質を失った場合、修復治療を行う必要がある。(保存修復、コンポジットレジン修復法なども参照。)
エナメル質の除去[編集]
歯の修復治療の大部分ではエナメル質の除去を行う。エナメル質のう蝕部位の除去のほか、象牙質や歯髄への通路を確保するため、またう蝕部位の除去後の修復、補綴のためにエナメル質の切削を行う。(保存修復・歯内治療・補綴治療なども参照。)また、脱灰が発生する前にエナメル質を除去することもある。歯の咬合面の溝の健康なエナメル質を除去し、それを歯科材料に取り替えるシーラントもある[66]。これは将来のう蝕から保護するための予防処置で、7年にわたり、う蝕のリスクを55%低下させる[67]。特に治療の必要がなくても、審美的な理由でエナメル質を除去することがある。歯の外見を良くするため、クラウンやラミネートベニヤを入れるためには歯を削る必要がある。象牙質に支持されていないエナメル質を残すと、エナメル質の破折を招くことがあるので、エナメル質の走行を覚え、それに基づきエナメル質を切削することが重要である[68]。
エッチング[編集]
修復材料であるレジンを歯質に接着させるため、Buonocore は酸により歯を溶解させるエッチングを1955年に開発した[69]。歯科修復物を歯に接着させる時、頻繁に使われる[70]。これはコンポジットレジンやシーラントのようないくつかの修復物を長期的に持たせるために重要である[37]。エナメル質中の無機質を溶解させ、エナメル質表面から約10マイクロメートルを除去し、5から50マイクロメートルの多孔質層を作る[71]。この多孔質層にレジンが侵入し、硬化することで接着する[72]。
エナメルに対するエッチングの影響は使用する酸の量、タイプおよびエナメルの現状などにより変化する[71]。
エッチングによる形成には3パターンある[71]。タイプ1はエナメル小柱が溶解されたパターン、タイプ2はエナメル小柱間質が溶解されたパターン、タイプ3はエナメル小柱があった証拠がなにも残っていないパターンである。タイプ1が最も好ましい物であり、タイプ3は最低である。これらのパターンに分かれる理由はまだはっきりとは分かっていないが、エナメル質中の結晶の走行の違いによる物ではないかという説が最も一般的である[73]。
エナメルボンドレジン[編集]
エッチングによって作られた多孔質層であるが、従来型マクロフィラーレジンを填塞する際には、フィラーの大きさが小柱の大きさより大きいために同部に入ることができず十分な接着力を行えない可能性があり、これに対応するために前処理としてエッチングされたエナメル質に塗布させる液状のレジンが開発された[72]。
歯のホワイトニング[編集]
着色や変色したエナメル質に対して、機械的動作や化学的方法を用い、歯を明るくする[74] のが、ホワイトニングである。(詳細はホワイトニングの項目参照)
機械的動作としては、専門的機械的歯面清掃があるほか、歯磨剤はエナメル質に付着した汚れを緩やかに研磨する。有効な方法だが、歯自体の色を落とすことができない[74]。
化学的な方法は、エナメルや象牙質を酸化させることで歯の色を本質的に変える[75]。歯科診療所にて行われるオフィスブリーチと患者が自身で行うホームブリーチがある。過酸化水素、過酸化尿素、過ホウ酸ナトリウムなどの酸化剤が一般的に用いられる[76][77]。pH を下げることは、脱灰によりう蝕となる危険がある。漂白後も、再石灰化環境にあるエナメル質は周囲の無機質イオンを取り込む可能性も示唆されている[78] が、薬品を選ぶ際には注意し、リスクを評価する必要がある[79]。
物理的動作と化学的方法の両方を用いる手段もある。たとえば、Microabrasion は最初に酸でエナメル質22 - 27マイクロメートルを脱灰させ、次に研磨を行う[80] ことでエナメル質の表面的な着色を除去する。変色の部位が深いか、象牙質の中である場合、この方法は成功しない。
人種による違い[編集]
エナメル質の人種による比較を報告した研究は少ないが、日本人とタイ人のエナメル質を比較した研究では、元素構成の割合や組織構造が異なり、タイ人のほうが組織の構造が明確で硬度が高いことが報告されている[81]。これは遺伝的なものではなく、環境的な要因による可能性が高いと考えられている[82]。
エナメル質の異常[編集]
遺伝・染色体異常[編集]
様々なタイプのエナメル質形成不全症(英語: Amelogenesis imperfecta) がある。遺伝性のものは低形成型(I型)、低成熟型(II型)、低石灰化型(III型)、タウロドント併発性低形成/低成熟型(IV型)の4通りに、非遺伝性の先天的なものはエナメル質減形成とエナメル質石灰化不全に分けられる[83]。最も一般的な低石灰化型は完全に石灰化していないもので、常染色体優性の遺伝疾患である[84]。結果、エナメル質は咬耗症や摩耗症などで容易に損耗し[85]、出てくる象牙質のために黄色く見える。低形成型はX染色体上のアメロゲニン遺伝子の異常[32] で、正常なエナメル質がほとんど形成されず、低石灰化型と同じような症状となる[84]。また、近年には Molar Incisor Hypomineralization (MIH) と呼ばれる第一大臼歯と切歯に限局して発生する原因不明のエナメル質形成不全の報告がなされている[83][86]。
局所的な要因[編集]
乳歯の根尖性歯周炎によるターナー歯や外傷による障害などによる、後続永久歯のエナメル質の障害がある[83]。
全身的な要因[編集]
低出生体重児への調査により、在胎月数が男では5.6から7.3か月、女では6.3から8.0か月で出生した場合に乳歯特に乳切歯のエナメル質形成不全や減形成が多いことが報告されている[87]。
胎児赤芽球症(英語: erythroblastosis fetalis) によって引き起こされる慢性のビリルビン脳症は幼児に多数の症状が現れる疾病である。その一つとして、エナメル質形成不全とエナメル質の緑色の着色を引き起こすことがある[88]。
造血性ポルフィリン症は体内でポルフィリンの沈着を引き起こす遺伝病である。この沈着がエナメル質でも発生し、赤い蛍光色となる[89]。
フッ素症は斑状菌を発生させ、露出部からフッ化物が出る[51]。
テトラサイクリン系抗生物質の妊婦への投与は胎児の形成中のエナメル質を黄色・黄褐色[90] - 茶色に着色させる[91]。このため、妊娠後半期の投与に注意が必要な薬であり[92]、妊婦への投与は必要性がない限りは行われない。
グルテンアレルギーが引き金となって起こる自己免疫疾患であるセリアック病もまた、エナメル質の脱灰を引き起こす。
動物のエナメル質[編集]

研究者達の調査により、人間と人間以外の哺乳類のエナメル質との間に違いはほとんどないということが示された。エナメル質の構造にほとんど違いはなく、エナメル器やエナメル芽細胞もヒトと同様に存在する[93]。エナメル小柱の横断面は動物により六角形、円形、長円形などを示す[94]。哺乳類間でのエナメル質の相違はわずかであるが重要である。形態、数、歯のタイプなどの点において確かな違いが存在する。
イヌは、唾液中のpHが8.0 - 9.0と非常に高く[95]、歯の脱灰を防ぎ再石灰化を促進させるので、人間に比べて虫歯になりにくい[96]。その一方、歯牙破折はしばしば認められ、特にガム、骨、チュウトイなどが原因で裂肉歯にてエナメル質と象牙質が剥がれるように破折することが多い[97]。外傷などにより歯が破折した時やう蝕になった場合、人間と同じように歯に修復物を詰めて治療することができる。この場合、全身麻酔下で一度に行う[95]。人間の歯と似ているため、イヌのエナメル質もテトラサイクリンによって着色される。したがって、若いイヌにテトラサイクリンが処方される場合、その危険性を説明しなければならない。また、人間同様エナメル質形成不全が発生する可能性もある[96][98]。ネズミは切歯の舌側面や臼歯の咬頭頂にはエナメル質を持たず、また、ウサギやモルモットでも切歯の舌側面にエナメル質が存在しない[36]。ウマでは、エナメル質と象牙質がかみ合っているが、これは強さを高め、摩耗を減らす働きがある[99]。
哺乳類以外で後生動物の中で歯にエナメル質を持つ生物としては、硬骨魚類、両生類、爬虫類が存在する(軟骨魚類はエナメロイド)。爬虫類や魚類の多くはエナメル質の構造が哺乳類と異なり、小柱構造を持たない類エナメル質と呼ばれることもある[36]。また、エナメル質を持たないサワラやヒラメや、歯の発生において象牙質より先にエナメル質が作られる鯛のようなものも魚類の中に存在する[36]。
脚注[編集]
- ^ a b c d Ross et al. (2002), p. 441
- ^ a b c d 久米川、前田 (1990) p.10
- ^ 藤田尚男、藤田恒夫 (2001) p.94
- ^ 栁澤 (1996) pp.11-12
- ^ a b c d Johnson (1999)
- ^ a b Cate (1998), p. 1:日本語版p. 3,p. 273
- ^ a b c Cate (1998), p. 219
- ^ 後藤(2014)
- ^ a b “浮谷先生コラム 第14弾~ウキウキ散歩⁉~歯科用語放浪記~”. 柔道整復学科ブログ|柔道整復師・鍼灸師の日本医学柔整鍼灸専門学校 (2021年11月19日). 2024年3月24日閲覧。
- ^ a b c d Cate (1998), p. 224
- ^ a b 横瀬, p.8
- ^ Cate (1998), p. 221:日本語版p. 277
- ^ 北村ら (2001), p.50
- ^ Cate (1998), p. 230:日本語版p. 290
- ^ 北村ら (2001), pp.50-51
- ^ Cate (1998), p. 76; Ross et al. (2002), p. 441
- ^ a b Cate (1998), 日本語版p. 286
- ^ 藤田恒太郎ら (2000) p.18
- ^ 藤田恒太郎ら (2000) p.19
- ^ Oral Studio歯科辞書 セメント - エナメル境
- ^ a b 栁澤 (1996)p.19
- ^ 栁澤 (1996)p.11
- ^ 栁澤 (1996)p.14
- ^ 栁澤 (1996)p.12
- ^ 大塚ら (1996) p. 304
- ^ 覚道ら (2000) pp.240-241
- ^ 大塚ら (1996) pp. 304-305
- ^ a b Cate (1998), p. 218:日本語版p. 274
- ^ a b 北村ら (2001), p.58
- ^ 藤田尚男、藤田恒夫 (2001) p.84
- ^ Cate (1998), p. 198:日本語版pp. 253-254
- ^ a b 早川ら (2000) p. 87
- ^ a b 早川ら (2000) p. 85
- ^ 和久本 他 (2008) p.11
- ^ a b 岩久ら (2002) pp. 6-7
- ^ a b c d 北村ら (2001), p.48
- ^ a b c Ross et al. (2002), p. 443
- ^ 藤田尚男、藤田恒夫 (2001) p.88
- ^ Cate (1998), p. 197:日本語版p. 249
- ^ a b Ross et al. (2002), p. 445
- ^ Cate (1998), p. 208
- ^ Ross et al. (2002), p. 447
- ^ Ross et al., p. 448
- ^ Ross et al. (2002), p. 3
- ^ 花田 (2008)
- ^ American Dental Hygienists' Association (2007)
- ^ a b Summitt et al. (2001), p. 2
- ^ Ash and Nelson (2003), p. 54
- ^ a b c 新谷 (2011) p.95
- ^ 下岡ら (1996) p. 105
- ^ a b Ross et al. (2002), p. 453
- ^ a b Gandara and Truelove (1999)
- ^ a b 山口ら (2008)
- ^ 小平ら (2009)
- ^ 韓ら (2008)
- ^ a b 郡司ら (2010)
- ^ 荒川ら (2003) pp. 161-166
- ^ a b 成橋ら (2011)
- ^ a b c 和久本ら (2008) p.15
- ^ う蝕治療ガイドライン (2009) pp.16-22
- ^ 月星 (2009) pp.16-21
- ^ 庄司 (2011) p.68
- ^ モリタ ダイアグノデントペン 製品特徴
- ^ a b 高森ら (2011)
- ^ 青山ら (2009)
- ^ Summitt et al. (2001), p. 273
- ^ Summitt et al. (2001), p. 274
- ^ Summitt et al. (2001), p. 7
- ^ 川原ら (1986) p. 74
- ^ Summitt et al. (2001), p. 191.
- ^ a b c Summitt et al. (2001), p. 193
- ^ a b 和久本 他 (2008) p.141-142
- ^ Cate (1998), p. 235:日本語版p. 294
- ^ a b American Dental Association (2007)
- ^ Summitt et al. (2001), p. 402
- ^ American Dental Association (2007) notes the intrinsic change; Summitt et al. (2001), p. 403 list the two most common agents
- ^ 岩久ら (2002) p. 312
- ^ 岩谷ら (2009)
- ^ Summitt et al., p. 404
- ^ Summitt et al. (2001), p. 420
- ^ 中原 (2009), pp.46-59
- ^ 中原 (2009), pp.59-63
- ^ a b c 新谷 (2011) p.110
- ^ a b Harris (2002), p. 7: see section titled "X-Linked Inheritance"
- ^ 二階ら (1999) pp. 26-27
- ^ 米津 他(2010)
- ^ 佐々 (2004)
- ^ eMedicine: Kernicterus
- ^ eMedicine: Erythropoietic Porphyria
- ^ 藤井 (2001) p.80
- ^ 三宅 (1997) p.404
- ^ 木村ら (2001)
- ^ Frandson and Spurgeon (1992), p. 305
- ^ 藤田尚男、藤田恒夫 (2001) p.95
- ^ a b 藤田桂一 (2008)
- ^ a b Pinney (1991), p. 187
- ^ 林ら (2010)
- ^ Pinney (1991), p. 186
- ^ Martin (2007); Randall-Bowman (2004)
参考文献[編集]
- American Dental Association (2007年). “Oral Health Topics A-Z: Tooth whitening treatments” (English). pp. Online FAQ. 2007年10月7日閲覧。
- American Dental Hygienists' Association (2007年). “Oral Health Information]” (English). 2007年10月7日閲覧。
- Ash, Major M., Jr. and Nelson, S.J. (2003) (English). Dental anatomy, physiology, and occlusion (8th ed. ed.). Philadelphia: W.B. Saunders. ISBN 0-7216-9382-2
- Blackwell, Bonnie (1996) "Why Teeth Fossilize Better Than Bone", Dinosaur mailing list, accessed 7 October 2007
- British Nutrition Foundation (2004年). “Dental Health” (English). 2007年10月7日閲覧。
- Brown, Theodore L. (2003). Chemistry : the central science (9th ed. ed.). Upper Saddle River, N.J. ; [Great Britain]: Prentice Hall. ISBN 0-13-049140-3 (pbk); ISBN 0-13-047038-4 (Access code card); ISBN 0-13-038165-9 (CD-ROM)
- Cate, A.R. Ten (1998). Oral Histology: development, structure, and function (5th ed. ed.). St. Louis, Mo. ; London: Mosby. ISBN 0-8151-2952-1
- A.R. Ten Cate『tenCate 口腔組織学』川崎堅三ほか訳(第5版)、医歯薬出版、2001年3月20日(原著1998年)。ISBN 4-263-45515-0。
- eMedicine (2007年). “Homepage” (English). 2007年10月7日閲覧。
- Frandson, R.D. and Spurgeon, T.L. (1992) (English). Anatomy and Physiology of Farm Animals (5th ed. ed.). Philadelphia: Lea & Febiger. ISBN 0-8121-1435-3
- Gandara, B.K. and Truelove, E.L. (November 1999). “Diagnosis and Management of Dental Erosion”. Journal of Contemporary Dental Practice 1 (1): 16-23. PMID 12167897.
- Harris, Edward F. (2002) Craniofacial Growth and Development
- Hebel, Jeanette L. and Poh-Fitxpatrick, M.B. (2006年). “Erythropoietic Porphyria”. eMedicen online. 2007年10月7日閲覧。
- Johnson, Clarke (1999年). “Biology of the Human Dentition”. Online course notes. Univ. Illinois at Chicago. 2007年10月7日閲覧。
- Martin, Chris (2007) Teeth, Encarta online encyclopedia, accessed 7 October 2007
- Ernest Newbrun, ed (April 1986) (English). Fluorides and Dental Caries: Contemporary Concepts for Practitioners and Students (3rd ed. ed.). Springfield, Illinois: Charles C Thomas Pub Ltd. ISBN 0-398-05196-8
- Chris C. Pinney (December 1991) (English). Illustrated Veterinary Guide for Dogs, Cats, Birds, and Exotic Pets. Sandra G. Pinson (Illustrator) (1st ed. ed.). Blue Ridge Summit, PA: Tab Books. ISBN 0-8306-1986-0
- Randall-Bowman, [n.i.] (2004) Gummed Out: Young Horses Lose Many Teeth, Vet Says, archived webpage, accessed 8 October 2007]
- Ross, Michael H., Kaye, G.I. and Pawlina, W. (2002-10-15) (English). Histology: a text and atlas (Fourth Edition ed.). Philadelphia; London: Lippincott Williams & Wilkins. ISBN 0-683-30242-6
- Springer, Shelley C. and Annibale, D.J. (2006) Kernicterus, eMedicine online, accessed 7 October 2007
- Summitt, James B. and Robbins, J. William and Schwartz, Richard S., ed (2001-01-15) (English). Fundamentals of Operative Dentistry: A Contemporary Approach (2nd Edition ed.). Chicago, Ill.: Quintessence Publishing. ISBN 978-0867153828
- 日本歯科保存学会 う蝕治療ガイドライン作成委員会 編『MI (Minimal Intervention) を理念としたエビデンス(根拠)とコンセンサス(合意)に基づくう蝕治療ガイドライン』(PDF)(第1版第1刷)永末書店、京都市上京区、2009年10月29日。ISBN 978-4-8160-1209-9。2011年4月10日閲覧。
- 青山剛大、中野健二郎、成橋昌剛、佐藤かおり、冨士谷盛興、千田彰「DIAGNOdent penの隣接面う蝕検出能に関するin vitro研究」(PDF)『日本歯科保存学会学術大会プログラムおよび講演抄録集』第131巻、日本歯科保存学会、東京都豊島区、2009年10月、web only、J-GLOBAL ID 201002242069522382 日本歯科保存学会平成21年度秋季学術大会(第131回)口演A14、2011年4月29日閲覧。
- 編著 荒川浩久、神原正樹、安井利一『スタンダード口腔保健学』(第1版)学建書院、2003年3月30日。ISBN 4-7624-0634-1。
- 岩谷いずみ、向井義晴、寺中敏夫「エナメル質漂白に対する再石灰化処理の影響」『日本歯科保存学雑誌』第52巻第1号、特定非営利活動法人日本歯科保存学会、2009年2月、pp. 1-11、ISSN 0387-2343、NAID 110007228035。
- 監修岩久正明、河野篤、千田彰、田上順次『改訂版保存修復学21』永末書店、2002年3月30日。ISBN 4-8160-1114-5。
- 編集大塚吉兵衛、榊鉄也他『スタンダード口腔生化学』(第1版)学建書院、1996年3月25日。ISBN 4-7624-0595-7。
- 小平真美、山口大、徳永理利、山口喜弘、斉藤佳代、葛西一貴「矯正治療前後におけるエナメルクラック発生の比較検討」『歯科審美』第22巻第1号、日本歯科審美学会、東京都豊島区、2009年9月、pp.48-54、ISSN 0916-1945、NAID 10026405324。
- 後藤仁敏「琺瑯質かエナメル質か、間葉性エナメル質かエナメロイドか」『鶴見大学紀要. 第3部, 保育・歯科衛生編』第51巻第1号、鶴見大学、2014年3月、pp. 71-86、ISSN 03898024、NAID 120006549053。
- 覚道幸男、吉田洋、杉村忠敬、西川泰央「III 口腔生理学/口腔器官の機能」『図説歯学生理学』(第2版第6刷)学建書院、2000年3月24日。ISBN 4-7624-0517-5。
- 監修川原春幸、中村正明『デンタルマテリアル』(第2版)医歯薬出版、1986年7月10日。ISBN 4-263-40370-3。
- 相山誉夫、今井倭武、織田正豊、北村博則、鈴木和夫、寺木良巳、戸田善久、東義景 著、北村博則、織田正豊 編『人体口腔組織図譜』(第4版第8刷)医歯薬出版、2001年1月20日。ISBN 978-4-263-40145-3。
- 編集 木村利美、国分秀也、嶋田美樹、島田慈彦 改訂 小林昌宏 (2001年9月25日). “-妊婦・胎児の薬物動態に関する適正使用情報II-” (PDF). Clin Kinetics Mews. 北里大学病院薬剤部. pp. No.13. 2010年12月5日閲覧。
- 久米川正好、前田憲彦 著「第1章 総論」、赤井三千男 編『歯の解剖学入門』(第1版)医歯薬出版、1990年5月31日、pp. 1-27頁。ISBN 4-263-40572-2。
- 郡司明彦、田村幸彦、平尾功治、町田光、秋田季子、小林奈緒美、藤井彰「う蝕予防のためのフッ化物応用に関する最近の知見 ―フッ化物洗口を中心に―」『歯科薬物療法』第29巻第1号、日本歯科薬物療法学会、東京都江東区、2010年、1-8頁、ISSN 0288-1012、NAID 10026132607、ONLINE ISSN 1884-4928。
- 佐々龍二「低出生体重児の歯、歯列および顎顔面頭蓋の特徴 その1 歯の特徴」『小児歯科臨床』第9巻第11号、東京臨床出版/全国小児歯科開業医会、東京都豊島区、2004年11月、71-75頁、ISSN 1341-1748。
- 編集下岡正八他『新小児歯科学』(第1版)クインテッセンス出版、1996年2月10日。ISBN 4-87417-501-5。
- 庄司茂『機能的な歯内治療 痛みの防止と残した歯の価値を高めるために』(第1版第1刷)デンタルダイヤモンド社、東京都千代田区、2011年4月1日。ISBN 978-4-88510-226-4。
- 新谷誠康 著「各論 小児歯科臨床-87のヒント 05.小児う蝕 乳歯歯質と永久歯歯質の違い/06.口腔領域の異常 歯質の異常」、吉田昊哲、嘉ノ海龍三、山﨑要一 編『小児歯科は成育医療へ ―今を知れば未来がわかる』デンタルダイヤモンド社、東京都千代田区〈DENTAL DIAMOND 増刊号〉、2011年4月1日、p.95/p.110頁。ISBN 978-4-88510-227-1。ISSN 0386-2305 第36巻第6号 通巻520号。
- 高森一乗、田中裕子、白川哲夫 著「各論 小児歯科臨床-87のヒント 05..小児う蝕 DIAGNOdent penを応用したう蝕の診査・診断」、吉田昊哲、嘉ノ海龍三、山﨑要一 編『小児歯科は成育医療へ ―今を知れば未来がわかる』デンタルダイヤモンド社、東京都千代田区〈DENTAL DIAMOND 増刊号〉、2011年4月1日、103頁。ISBN 978-4-88510-227-1。ISSN 0386-2305 第36巻第6号 通巻520号。
- 月星光博『外傷歯の診断と治療 増補新版』(第2版第1刷)クインテッセンス出版〈シリーズMIに基づく歯科臨床〉、2009年8月10日。ISBN 978-4-7812-0090-3。
- 中原泉「3 人種とエナメル質の様相」『歯の人類学』(第1版第4刷)医歯薬出版、東京都文京区、2009年2月20日、46-63頁。ISBN 978-4-263-45561-6。NCID BA62230794。
- 成橋昌剛、冨士谷盛興、山田三良、千田彰「レーザーはここまできた! practive &Evidence 3 齲蝕治療にレーザーを活用する!」『歯界展望』第117巻第4号、医歯薬出版、東京都文京区、2011年4月、656-660頁、ISSN 0011-8702。
- 編集二階宏昌他『歯学生のための病理学 口腔病理編』(第2版)医歯薬出版、1999年5月10日。ISBN 4-263-45438-3。
- 花田信弘 著「第I部 総論 第1章 う蝕のライフサイクルと予防 1.ライフサイクルとう蝕」、田上順次、花田信弘、桃井保子 編『う蝕学 - チェアサイドの予防と回復のプログラム -』(第1版第1刷)永末書店、京都市上京区、2008年3月5日、pp. 8-13頁。ISBN 978-4-8160-1192-4。
- 早川太郎、須田立雄、木崎治俊『口腔生化学』(第3版)医歯薬出版、2000年9月20日。ISBN 4-263-45485-5。
- 林一彦、渡邉佳恵、大村雅、木場秀夫「介助犬の臼歯破折」『日本補助犬科学研究』第4巻第1号、日本身体障害者補助犬学会、東京都渋谷区、2010年、40-43頁、doi:10.3373/jssdr.4.40、ISSN 1881-8978、NAID 40017412237、ONLINE ISSN 1882-3084。
- 韓臨麟、砂田賢、岡本明、福島正義、興地隆史「エナメル質亀裂の発生状況と関連症状に関する臨床調査」『日本歯科保存学雑誌』第51巻第6号、特定非営利活動法人日本歯科保存学会、2008年12月、pp. 614-621、ISSN 0387-2343、NAID 110007026967。
- 藤田桂一「小動物歯科診療の歴史ならびに現状と展望(II)」『日本獣医師会雑誌』第58巻第5号、日本獣医師会、2008年5月、pp. 298-300、ISSN 0446-6454、NAID 10015712705。
- 藤井彰『歯科薬理学サイドリーダー』(第2版第1刷)学建書院、2001年6月10日。ISBN 4-7624-1142-6。
- 原著藤田恒太郎、改訂桐野忠大、山下靖雄『歯の解剖学』(第22版第6刷)金原出版、2000年1月30日。ISBN 4-307-45007-8。
- 藤田尚男、藤田恒夫「III.消化器系 B.歯」『標準組織学 各論』(第3版第10刷)医学書院、2001年3月1日、pp. 83-104頁。ISBN 4-260-10053-X。
- 三宅洋一郎 著「19章 病原微生物に作用する化学療法薬 B 各論」、石田甫、大浦清、斎藤喜八、土肥敏博 編『歯科薬理学』(第4版)医歯薬出版、1997年6月13日、pp. 399-409頁。ISBN 4-263-45370-0。
- 栁澤孝彰 著「第1章 保存修復学総論 B 歯の構造と機能 2 歯の構造」、石川達也、藤井弁次、勝山茂 編『標準保存修復学』(第3版第1刷)医学書院、1996年7月15日、pp.11-20頁。ISBN 4-260-13724-7。
- 山口喜弘、山口大、葛西一貴「Q&A エナメルクラックに用いる充填剤」『デンタルダイヤモンド』第33巻第2号、デンタルダイヤモンド社、東京都千代田区、2008年2月、pp.100-101、ISSN 0386-2305。
- 横瀬敏志 著「第1章 保存修復学概説 3 歯・周囲組織の構造と口腔の機能 A.歯の構造」、平井義人、寺中敏夫、寺下正道、千田彰 編『保存修復学』(第5版第2刷)医歯薬出版、東京都文京区、2008年5月25日、6-14頁。ISBN 978-4-263-45606-4。NCID BA81788568。
- 米津卓郎、新谷誠康 (2010年9月). “リレーミニレクチャー エナメル質の形成障害と小児歯科臨床における対応” (PDF). 東京歯科大学千葉病院医療連携NEWS デンタルドットコム. 東京歯科大学千葉病院医療連携室. pp. 4. 2011年4月30日閲覧。
- 和久本貞雄、久光久、伊藤和雄『最新 保存修復』(第2版第14刷)医歯薬出版、東京都文京区、2008年1月20日。ISBN 978-4-263-40408-9。
- “【Oral Studio歯科辞書】”. Oral Studio. デンタルアロー. 2011年1月22日閲覧。
- “光学式う蝕検出装置 ダイアグノデントペン 製品特長”. 歯科情報ポータルサイト デンタルプラザ. モリタ. 2011年4月29日閲覧。
関連項目[編集]
外部リンク[編集]