局所麻酔薬

局所麻酔薬(きょくしょますいやく、略称: 局麻、局麻薬: 英: local anesthetic)とは、痛みの感覚をなくす局所麻酔のための医薬品である。局所麻酔薬は、主に神経細胞膜のナトリウム特異的イオンチャネル、特にいわゆる電位依存性ナトリウムチャネルを介したナトリウムの流入を阻害する。ナトリウムの流入が阻害されると、活動電位が発生できなくなる。その結果、神経を介した、感覚や運動の伝導・伝達が遮断される。ドイツ医学の影響を強く受けた日本の医療現場では古くから、「ロカール」と「カ」の部分にアクセントを置いて呼ばれることが多かった。これはドイツ語の局所麻酔薬(独: Lokalanästhetikum)の発音に由来する[1]。
手術の場合、全身麻酔のための全身麻酔薬とは異なり、局所麻酔薬は意識を失うことなく、体の特定の場所に痛みのない状態を作り出す。また、特定の神経経路に使用する場合(神経ブロック)、運動麻痺(筋力の低下)を得ることも可能である。
概要[編集]
臨床用局麻は、アミド型およびエステル型局所麻酔薬の2つの型に分類される。合成局麻は、構造的にコカインに関連している。コカインとの違いは、乱用の可能性が非常に低く、高血圧(少数の例外を除いて)や血管収縮を引き起こさないことである。力価により下記の通りに分類される[2]。
| 低力価 | 中力価 | 高力価 |
|---|---|---|
| プロカイン | メピバカイン | テトラカイン |
これらの薬剤は、以下のような様々な局所麻酔に使用されている。
- 表面麻酔クリーム、ゲル、軟膏、液体、スプレーなどの局所投与で、麻酔薬をジメチルスルホキシドやその他の溶媒/基剤に溶解し、より深く吸収させる。
- 浸潤麻酔
- 腕神経叢ブロック
- 硬膜外麻酔
- 脊髄くも膜下麻酔
- イオントフォレーシス
これらの薬剤名の末尾にある「-caine」は、かつてコカインが局所麻酔薬として使用されていたことから、コカイン(cocaine)にちなんで命名されたものである。
作用機序[編集]
局所麻酔薬は、主に神経細胞膜のナトリウム特異的イオンチャネル、特にいわゆる電位依存性ナトリウムチャネルを介したナトリウムの流入を阻害することにより作用する[3]。ナトリウムの流入が阻害されると、活動電位が発生できなくなり、信号伝導が阻害される。
塩基型とイオン型[編集]

局所麻酔薬の共通の構造として、脂溶性の高い芳香基(ベンゼン環)と、水素イオンを得て電離すると水溶性となる3級アミンの双方を持っている点が特徴である[4]。分子全体としての脂溶性が高いほど局所麻酔の作用(力価)は強くなる[2]。局麻薬は弱塩基性であり、通常、水溶性にするために塩酸塩として製剤化される。このため水溶液中では、塩基型(B)とイオン型(BH+)の平衡状態にある(右図参照)[5]。塩基型のみが脂質で構成される細胞膜を容易に拡散する。細胞内に入ると、局所麻酔薬は平衡状態になり、再度イオン型が形成され、細胞外に容易に戻ることはない。これは、「イオントラップ」と呼ばれている。イオン型の状態で、局所麻酔薬は神経繊維の電位依存性ナトリウムチャネル内部の細胞質端に近い特異的結合部位に結合する[3]。ほとんどの局所麻酔薬は、膜の内表面で作用する。薬物は細胞膜を透過する必要があり、これは塩基型で最もよく達成される。このことは、永久的にイオン化された局所麻酔薬であるRAC 421-IIが、細胞膜を横切って拡散することはできないが、神経線維の細胞質に注入された場合、NaKATPase遮断と麻酔効果を誘発することができることを例証している。局所麻酔薬は、電離していない塩基型(B)の状態で細胞膜を通過した後に、イオン型(BH+)に変わり細胞質側から電位依存性ナトリウムチャネルをブロックして、神経の信号伝達を阻害することにより作用を発揮する。創傷部の炎症によるアシドーシスは、局麻薬の作用を一部低下させる。これは、麻酔薬の大部分がイオン化しているため、細胞膜を通過して細胞質に面したナトリウムチャネルに作用する部位に到達できないことが一因である[6]。
局所麻酔薬の効き方[編集]
すべての神経線維は局麻薬に感受性があるが、直径と髄鞘の組み合わせにより、局麻薬遮断に対する線維の感受性は異なり、これを分離遮断と呼んでいる。B線維(交感神経緊張)が最も感度が高く、次いでC線維(痛み)、Aδ(温度)、Aγ(固有感覚)、Aβ(触覚、圧覚)、Aα(運動)である。B線維はC線維より太いが、有髄であるため、有髄でない細いC型線維より先に遮断される 。一般に細い神経から順に麻酔されてゆく。順序としては、血管運動神経、温痛覚、触覚、圧覚、運動の順番である。臨床現場では麻酔効果の判定は主に冷たさを感じるかで行う(コールドサインテスト)。
アミド型とエステル型[編集]
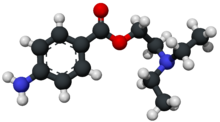
アミド型とエステル型とは、局所麻酔薬の分類であり、その名称は、脂溶性芳香族環と親水性アミノ基の中間鎖の化学構造にちなむ。アミド型はアミド結合であり、エステル型はエステル結合である[7][8]。アミド型の英語名は「アミノアミド(英: amino amides)」、エステル型の英語名は「アミノエステル(英: amino esters)」であるが、日本ではこの呼称はあまり普及していない。
化学構造[編集]


構造的には、局所麻酔薬は3つの分子成分から構成されている[7]。
脂溶性部分と中間鎖の化学結合には、アミド型とエステル型があり、現在の局所麻酔薬の分類の一般的な基礎となっている[7]。
薬理[編集]
エステル型局所麻酔薬は、血漿中でブチリルコリンエステラーゼ(偽コリンエステラーゼ)によりパラアミノ安息香酸誘導体に速やかに代謝され、尿中に排泄される[9]。このことから、半減期が非常に短いことが示唆されている[10]。アミド型よりエステル型でアレルギーを起こしやすいと言われているが、アレルギー反応に関与しているのはエステル結合そのものでは無く、エステル型局所麻酔薬の分解産物であるパラアミノ安息香酸[11]とその誘導体である[7]。アミド型は肝代謝型であり、チトクロームP450関連酵素により分解される[8]。主に肝臓で緩徐に分解されるため、作用時間が長い傾向にある。長く麻酔薬が残存するため、ブピバカインなどの毒性が強い麻酔薬で有害作用が発生した場合は治療上の問題となる[12]。これは、肝不全患者における薬剤選択の要因となりうるが[13]、偽コリンエステラーゼは肝臓で産生されるため、生理的(例:新生児・乳児または超高齢の個人)または病理的(例:肝硬変)にも肝代謝障害はエステル型を用いる場合も考慮せねばならない。
| エステル型 | アミド型 | 天然物由来 |
|---|---|---|
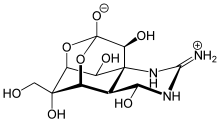
メントール、オイゲノール、コカインを除くほとんどの天然物由来局所麻酔薬は神経毒であり、その名称には-toxinという接尾語がついている。コカインはナトリウムチャネルの細胞内側に結合し、サキシトキシン、ネオサキシトキシン、テトロドトキシンはナトリウムチャネルの細胞外側に結合する。
組成[編集]

注射用局所麻酔液は、通常、以下のもので構成されている:[14]
- 局所麻酔薬そのもの
- 通常、水性または単なる滅菌水である溶媒
- 血管収縮薬(必須ではない。本節で後述)
- 還元剤(抗酸化剤)、例えばエピネフリンが使用される場合、還元剤としてメタ重亜硫酸ナトリウムが使用される。
- 防腐剤、例:メチルパラベン
- 緩衝液
時には、局麻が組み合わされることもある。例:
- リドカイン/プリロカイン(EMLA, Eutectic Mixture of Local Anesthetic: 局麻薬共融混合物)
- リドカイン/テトラカイン(Rapydan)
- テトラカイン/アドレナリン/コカイン合剤(TAC)
注射用局麻液は、血管を収縮させることで局所麻酔の持続時間を長くし、それによって麻酔薬を安全に長時間濃度を維持するとともに、出血を抑えるために血管収縮剤(合剤)と混合されることがある[15]。血管収縮剤は、全身循環が注射部位から局所麻酔薬を除去する速度を一時的に低下させるため、血管収縮剤と組み合わせた場合の局麻の最大投与量は血管収縮剤のない同じ局麻と比較して高くなる。時折、この目的のためにコカインが投与されることがある。例としては、以下のようなものがある。
- 塩酸プリロカインとエピネフリン(商品名シタネストフォルテ)
- リドカイン、ブピバカイン、およびエピネフリン(推奨最終濃度はそれぞれ0.5、0.25、および0.5%)
- リドカインとエピネフリンで構成されるイオントカイン
- セプトカイン(商品名セプトドント)、アーティカインとエピネフリンとの配合剤
このタイプの組み合わせ製品の1つは、表面麻酔のために局所的に使用されるTAC(5-12%テトラカイン、1/2000(0.05%、500ppm、1/2パーミル)アドレナリン、4または10%コカイン)である。
局所血管収縮薬の添加[編集]
一部の局所麻酔薬はアドレナリンなどを添加して用いられる。これは麻酔薬を使用した部位の血管が収縮するため、麻酔薬が血流などの影響で濃度低下する時間が遅くなるため作用時間が長くなったり、局所に麻酔薬が留まり血中濃度が上昇し難いようにするなどの効果を期待するものである。しかし、糖尿病、甲状腺機能亢進症、高血圧といった全身性疾患を持っている場合は、添付文書上は禁忌とされている[16]。局所麻酔薬へのアドレナリンなどの添加は主にリドカインで行われ、製剤時に添加済みの薬剤も使用されている[16]。
血管収縮剤を使用した局麻薬は、終動脈に灌流されている部位でも安全である[注釈 1]。血管収縮剤入り局麻薬が鼻、耳、指、足指などの四肢に壊死を起こす(終動脈の収縮による)という通説には、1948年のエピネフリン入り市販リドカインの導入以来、壊死の例が報告されていないため根拠がないという反論がある[17]。
光学異性体[編集]
光学異性体とは、分子を構成する原子の組成および結合状態は同一であるが、立体構造が異なる分子を言う。メピバカイン、ブピバカイン、ロピバカインには光学異性体が存在する。従来の局所麻酔薬はR体(右旋性)とS体 (左旋性) を等量含んだラセミ体として使用されてきたものの、光学異性体の間で麻酔の効果や心毒性に差が見られることが分かってきた。市販されているロピバカイン製剤であるアナペインは、局所麻酔作用が強く、心血管系への作用が少ないS体のみを製剤化し安全性を高めている。同様に、S体のブピバカインのみを製剤化したものがレボブピバカインである。レボブピバカインは、ラセミ体のブピバカインと比べ効力は同等であるのに対して、心毒性は弱い。
副作用[編集]
局所麻酔薬中毒[編集]
過量投与により、主として中枢神経系と心血管系に様々な症状が現れる。これは症状が多彩なため、アレルギー反応と間違われやすい[18]。近年は用語が多義的で誤解を招きやすい中毒よりも局所麻酔薬の全身毒性(英: local anesthetic systemic toxicity: LAST)と表記されることが増えてきている[19][20]。
中枢神経系[編集]
局所麻酔薬の組織内濃度に応じて、中枢神経系に興奮性または抑制性の作用が生じることがある。
全身毒性の初期症状には、耳鳴り、口の中の金属味、口のしびれまたは麻痺、めまいおよび/または見当識障害がある。
高濃度では、抑制性ニューロンの比較的選択的な抑制により脳が興奮し、末梢の運動痙攣に続いてけいれん発作を起こすなど、より高度な症状を引き起こすことがある。ブピバカイン、特にクロロプロカインとの併用で発作が起こりやすいと報告されている[21]。
さらに高濃度では脳機能の深部抑制が起こり、昏睡、呼吸停止、死亡に至ることがある[22]。このような組織濃度は、高用量の静脈内注入によるものである可能性がある。
心血管系[編集]
心臓毒性は、薬剤の血管への不適切な注入により生じることがある。適切な投与を行っても、患者の予見できない解剖学的特異性により、投与部位から体内に薬剤が拡散することは避けられない[21]。このため、神経系に影響を及ぼしたり、薬剤が全身循環に移行することがある。しかし、感染が伝播することは非常にまれである。
局所麻酔薬の血管内注射の過量投与に伴う心臓毒性は、低血圧、房室伝導遅延、心室固有調律、および最終的な心血管系虚脱によって特徴づけられる。すべての局所麻酔薬は心筋の不応期を短縮する可能性があるが、ブピバカインは心筋のナトリウムチャネルを遮断するため、致死的不整脈を誘発する可能性が最も高い。心血管系の副作用を改善するために開発されたレボブピバカインとロピバカイン(単一光学異性体誘導体)でさえ、心機能を破綻させる可能性を持つ[23]。麻酔薬の組み合わせによる毒性は相加的である[21]。
内分泌系[編集]
内分泌系と代謝系にはわずかな副作用しかなく、ほとんどの場合、臨床的な反応はない[21]。
LASTの治療
下記の治療法が提唱されている[20]。
- 局所麻酔薬の投与をやめる/応援を求める
- 気道確保
- ベンゾジアゼピンによる痙攣抑制
- 必要に応じて心肺蘇生
- 20%脂質エマルジョン1.5mL/kg(2~3分以上かけてボーラス投与)(リピッドレスキューの項を参照)
リピッドレスキュー[編集]
この中毒治療の方法は、1998年にガイ・ワインバーグ博士によって考案されたが、2006年に初めて救命の成功例が発表されるまで、広く使用されるには至らなかった。一般に市販されている脂肪乳剤であるイントラリピッドが、局所麻酔薬の過量投与に続発する重度の心毒性の治療に有効であることを示す証拠があり、この方法での使用(リピッドレスキュー)に成功したヒトの症例報告もある[24][25][26]。しかし現時点ではまだエビデンスは限られている[27]。
現在までのほとんどの報告では、一般に入手可能な静脈内脂質乳剤であるイントラリピッドを使用しているが、リポシンおよびメディアリピッドのような他の乳剤も有効であることが示されている。
動物実験による十分なエビデンス[28][29]やヒトの症例報告では、この方法での使用が成功している[25][26]。英国では、この使用をより広く公表する努力がなされ[24]、リピッドレスキューは現在英国・アイルランド麻酔科医協会により治療法として公式に推進されている[30]。ブプロピオン及びラモトリギンの過量投与における難治性心停止の治療に脂質乳剤が成功したという1例の報告が発表されている[31]。
「自家製の」リピッドレスキューキットの組成も発表されている[32]。
リピッドレスキューの作用機序は完全に理解されていないが、血流中の添加脂質はシンクとして作用し、患部組織から親油性毒素を除去することができるのかもしれない。この理論は、ウサギのクロミプラミン毒性に対するリピッドレスキューに関する2つの研究[33][34]、モキシデクチンの子犬を治療するためにリピッドレスキューを使用するという獣医学の臨床報告[35]と一致するものであった。
免疫学的アレルギー(アナフィラキシー)[編集]
局所麻酔薬(特にエステル型)に対する有害反応は珍しくないが、厳密な意味でのアレルギーやアナフィラキシーは非常にまれである[18]。エステルに対するアレルギー反応は通常、その代謝物であるパラアミノ安息香酸に対する過敏性に起因し、アミド型に対する交差アレルギーには至らない[36]。そのため、アミド型局麻はそのような患者の代替品として使用することができる。非アレルギー性反応(例えばLAST)は、その症状においてアレルギーに類似している場合がある。場合によっては、アレルギーの診断を確立するために、皮膚テストおよびチャレンジ試験が必要となることがある。また、局所麻酔薬に防腐剤として添加されることの多いパラベン誘導体に対するアレルギーの症例もある。
メトヘモグロビン血症[編集]
メトヘモグロビン血症は、ヘモグロビン中の鉄が変化して酸素運搬能力が低下し、チアノーゼや低酸素症の症状が現れるものである。ベンゾカイン、リドカイン、プリロカインなどのアニリン系化学物質にさらされるとこの作用が現れ、特にベンゾカインが顕著である[36]。プリロカインの全身毒性は比較的低いが、その代謝物のo-トルイジンはメトヘモグロビン血症を引き起こすことが知られている。
世代間の影響[編集]
体外受精における卵子摘出時に局所麻酔薬を使用することについては、議論がある。卵胞液中に薬理学的濃度の麻酔薬が検出されている[21]。臨床試験では、妊婦への影響については結論が出ていない。しかし、ラットにおけるリドカインの子孫への行動上の影響については懸念されている[21]。
妊娠中、局所麻酔薬が胎児に何らかの悪影響を及ぼすことは一般的ではありないこれにもかかわらず、妊娠中は局所麻酔薬のタンパク非結合分画が増加し、生理的変化によって中枢神経系への局所麻酔薬の移行が増加するため、毒性のリスクが高くなる可能性がある[21]。したがって、妊婦は、潜在的合併症を減らすために低用量の局所麻酔薬を使用することが推奨されている[37]。
脚注[編集]
注釈[編集]
- ^ 2023年現在の日本では定説がない。
出典[編集]
- ^ Forvoチーム. “Lokalanästhetikum の発音: Lokalanästhetikum の ドイツ語 の発音”. Forvo.com. 2023年2月23日閲覧。
- ^ a b Gropper 2020, p. 868.
- ^ a b Gropper 2020, p. 873.
- ^ Miller 2007, p. 453.
- ^ Gropper 2020, p. 866.
- ^ Miller 2007, p. 455.
- ^ a b c d Becker, Daniel E; Reed, Kenneth L (2012). “Local Anesthetics: Review of Pharmacological Considerations”. Anesthesia Progress 59 (2): 90–102. doi:10.2344/0003-3006-59.2.90. ISSN 0003-3006. PMC 3403589. PMID 22822998.
- ^ a b Gropper 2020, p. 865.
- ^ “Procaine”. go.drugbank.com. 2023年2月23日閲覧。
- ^ Drasner, Kenneth (2017), Katzung, Bertram G., ed., Local Anesthetics (14 ed.), McGraw-Hill Education 2023年2月23日閲覧。
- ^ Gropper 2020, p. 875.
- ^ Vijay, Bhavani S.; Mitra, Subhro; Jamil, Shahin N. (2013). “Refractory cardiac arrest due to inadvertent intravenous injection of 0.25% bupivacaine used for local infiltration anesthesia”. Anesthesia, Essays and Researches 7 (1): 130–132. doi:10.4103/0259-1162.114020. ISSN 0259-1162. PMC 4173496. PMID 25885735.
- ^ Pharmacology: PreTest self-assessment and review. New York: McGraw-Hill, Medical Pub. Division. (2002). ISBN 978-0-07-136704-2
- ^ “Allergic Reactions”. Cleveland Clinic. 2014年4月11日閲覧。
- ^ “Vasoconstrictor agents for local anesthesia”. Anesthesia Progress 42 (3–4): 116–120. (1995). PMC 2148913. PMID 8934977.
- ^ a b “キシロカイン注射液「0.5%」エピレナミン(1:100,000)含有/ キシロカイン注射液「1%」エピレナミン(1:100,000)含有/ キシロカイン注射液「2%」エピレナミン(1:80,000)含有”. www.info.pmda.go.jp. 2023年6月29日閲覧。
- ^ “[Local anaesthesia with vasoconstrictor is safe to use in areas with end-arteries in fingers, toes, noses and ears]”. Ugeskrift for Laeger 176 (44): 44. (October 2014). PMID 25354008.
- ^ a b Bina, Babak; Hersh, Elliot V.; Hilario, Micael; Alvarez, Kenia; McLaughlin, Bradford (2018-06-01). “True Allergy to Amide Local Anesthetics: A Review and Case Presentation” (英語). Anesthesia Progress 65 (2): 119–123. doi:10.2344/anpr-65-03-06. ISSN 0003-3006. PMC PMC6022794. PMID 29952645.
- ^ El-Boghdadly, Kariem; Pawa, Amit; Chin, Ki Jinn (2018). “Local anesthetic systemic toxicity: current perspectives”. Local and Regional Anesthesia 11: 35–44. doi:10.2147/LRA.S154512. ISSN 1178-7112. PMC 6087022. PMID 30122981.
- ^ a b “局所麻酔薬中毒 (LAST) 再訪:発展のパラダイム”. Anesthesia Patient Safety Foundation. 2023年2月25日閲覧。
- ^ a b c d e f g (英語) Meyler's Side Effects of Drugs Used in Anesthesia. Elsevier. (2008-10-07). ISBN 9780444532701
- ^ “Systemic toxicity and cardiotoxicity from local anesthetics: incidence and preventive measures”. Regional Anesthesia and Pain Medicine 27 (6): 556–561. (2002). doi:10.1053/rapm.2002.37127. PMID 12430104.
- ^ “Intralipid Treatment Of Bupicavaine Toxicity”. Anesthesia Patient Safety Foundation 24 (1). (Spring 2009) 2013年6月12日閲覧。.
- ^ a b “Lipid emulsion to treat overdose of local anaesthetic: the gift of the glob”. Anaesthesia 61 (2): 107–109. (February 2006). doi:10.1111/j.1365-2044.2005.04494.x. PMID 16430560.
- ^ a b “Successful use of a 20% lipid emulsion to resuscitate a patient after a presumed bupivacaine-related cardiac arrest”. Anesthesiology 105 (1): 217–218. (July 2006). doi:10.1097/00000542-200607000-00033. PMID 16810015.
- ^ a b “Successful resuscitation of a patient with ropivacaine-induced asystole after axillary plexus block using lipid infusion”. Anaesthesia 61 (8): 800–801. (August 2006). doi:10.1111/j.1365-2044.2006.04740.x. PMID 16867094.
- ^ “Intravenous lipid emulsion as antidote beyond local anesthetic toxicity: a systematic review”. Academic Emergency Medicine 16 (9): 815–824. (September 2009). doi:10.1111/j.1553-2712.2009.00499.x. PMID 19845549.
- ^ “Pretreatment or resuscitation with a lipid infusion shifts the dose-response to bupivacaine-induced asystole in rats”. Anesthesiology 88 (4): 1071–1075. (April 1998). doi:10.1097/00000542-199804000-00028. PMID 9579517.
- ^ “Lipid emulsion infusion rescues dogs from bupivacaine-induced cardiac toxicity”. Regional Anesthesia and Pain Medicine 28 (3): 198–202. (2003). doi:10.1053/rapm.2003.50041. PMID 12772136.
- ^ “Association of Anesthesists of Great Britain and Ireland home page”.[リンク切れ]
- ^ “Use of lipid emulsion in the resuscitation of a patient with prolonged cardiovascular collapse after overdose of bupropion and lamotrigine”. Annals of Emergency Medicine 51 (4): 412–5, 415.e1. (April 2008). doi:10.1016/j.annemergmed.2007.06.004. PMID 177660096
- ^ “lipidrescue - Sample LipidRescue Kit”. lipidrescue.squarespace.com. 2022年12月4日閲覧。
- ^ “Intralipid outperforms sodium bicarbonate in a rabbit model of clomipramine toxicity”. Annals of Emergency Medicine 49 (2): 178–85, 185.e1–4. (February 2007). doi:10.1016/j.annemergmed.2006.07.016. PMID 17098328.
- ^ “Correlation of plasma and peritoneal diasylate clomipramine concentration with hemodynamic recovery after intralipid infusion in rabbits”. Academic Emergency Medicine 16 (2): 151–156. (February 2009). doi:10.1111/j.1553-2712.2008.00313.x. PMID 19133855.
- ^ “Moxidectin toxicosis in a puppy successfully treated with intravenous lipids”. Journal of Veterinary Emergency and Critical Care 19 (2): 181–186. (April 2009). doi:10.1111/j.1476-4431.2009.00402.x. PMID 19691569.
- ^ a b Facial plastic, reconstructive, and trauma surgery. Marcel Dekker. (2003-10-17). ISBN 978-0-8247-4595-0
- ^ 正尚, 横山 (2007). “硬膜外麻酔に用いる局所麻酔薬の特徴”. 日本臨床麻酔学会誌 27 (5): 445–455. doi:10.2199/jjsca.27.445.
参考文献[編集]
- Miller, Ronald 著、武田純三 訳『ミラー麻酔科学』メディカルサイエンスインターナショナル、2007年4月1日。ISBN 9784895924658。
- Gropper, Michael A. (2020) (英語). Miller's anesthesia (Ninth ed.). Philadelphia: Elsevier. ISBN 9780323612647. OCLC 1124935549
関連項目[編集]
外部リンク[編集]
- 日本区域麻酔学会
- The American Society of Regional Anesthesia 米国区域麻酔学会(英語)
- Regional Anesthesia and Pain & Medicine 学術誌: 区域麻酔と疼痛医学(英語)
