ラモトリギン
 | |
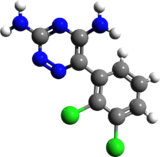 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 |
|
| 法的規制 | |
| 投与経路 | 経口投与 |
| 薬物動態データ | |
| 生物学的利用能 | 98% |
| 代謝 | 肝臓 |
| 半減期 | 31-38時間 |
| 排泄 | 尿中94% 糞便中2% |
| 識別 | |
| CAS番号 | 84057-84-1 |
| ATCコード | N03AX09 (WHO) |
| PubChem | CID: 3878 CID 3878 |
| DrugBank | DB00555 |
| KEGG | D00354 |
| 化学的データ | |
| 化学式 | C9H7Cl2N5 |
| 分子量 | 256.091g/mol |
ラモトリギン(Lamotrigine)は、抗てんかん薬の一つである[1]。また、双極性障害の気分安定薬としても処方される。日本では2008年よりグラクソ・スミスクラインより商品名ラミクタールで販売され、適応は抗てんかん薬として、また双極性障害の気分エピソードの抑制である。
薬機法による劇薬および処方箋医薬品である。副作用として重篤な薬疹による皮膚症状があり[2]、2015年2月には皮膚障害による死亡例を受けて厚生労働省から安全性速報が出された[3](詳細は#副作用を参照)。
医療用途
[編集]てんかん
[編集]- てんかん患者での、部分発作(二次性全般化発作を含む)、強直間代発作、定型欠神発作対する単剤療法
- 他の抗てんかん薬で十分な効果が認められないてんかん患者に対する他の抗てんかん薬との併用療法
- 部分発作(二次性全般化発作を含む)、強直間代発作、Lennox-Gastaut症候群における全般発作
英国国立医療技術評価機構(NICE)ガイドラインでは、児童青年および成人のてんかん初回発症について、カルバマゼピンとならび第一選択薬として推奨している[1]。
双極性障害
[編集]- 双極性障害における気分エピソードの再発・再燃抑制
海外では、双極性障害に対して一時は第一選択薬であったが、2008年の出版バイアスの調査[4]により、急性のエピソードやラピッド・サイクルに有効性が見られなかった[5]。急性期に対する有効性や安全性は確立されていない[6]。
日本での使用上の注意には、双極性障害の急性期の有効性と安全性は確立されていないと記載されている。日本うつ病学会による双極性障害の診療ガイドラインは、スティーブンス・ジョンソン症候群など皮膚症候群に注意し、少量からの漸増の推奨に言及している[7]。うつ病エピソードでは、リチウム、クエチアピン、オランザピンと同じく「推奨される」に分類され、ラモトリギンには有効と無効の報告があり、無効の報告を解析すると重症では有効であった[8]。維持期では「最も推奨される」リチウムに続いて、いくつかの「推奨される」薬剤の1つである[8]。双極II型障害の維持期では証拠が少なく、薬物療法が考慮されるのは頻回かつ重症のうつ病やI型の家族歴などが考えられケースによる[9]。
適用外処方
[編集]適応外使用として神経痛に対して処方されることもあるが、英国国立医療技術評価機構 (NICE) は専門医の指導下でなければ行ってはならないと勧告している[10]。
作用機序
[編集]Na+チャネルを抑制することにより、神経膜を安定させ、グルタミン酸などの興奮性神経伝達物質の遊離を抑え、抗痙攣作用を示すと考えられている。なお、双極性障害に対して効果を示す機序は明らかになっていない。
痙攣動物モデルにおいて抗痙攣作用が示されている。抗痙攣作用はフェニトインやジアゼパムに比べ高いとされる。
用法・用量
[編集]

グラクソ・スミスクライン株式会社より販売されている。日本では、100mgと25mg、小児用に5mgと2mgが販売されている。
ラモトリギンはグルクロン酸抱合を受け代謝されるため、バルプロ酸ナトリウムなどこの代謝の阻害作用のある医薬品と併用された場合には用量は変わってくる[11]。その他抗てんかん薬との併用により、投薬量、漸増量が異なる。医師の指示の下で服薬する。血中濃度を保つ必要があるため、定期的に服薬する必要がある。
急激な増量を行うと重篤な副作用を起こしやすいとされているため、徐々に増量することが好ましい。
副作用
[編集]重篤な副作用として薬疹による皮膚障害があり、皮膚粘膜眼症候群(スティーブンス・ジョンソン症候群)、中毒性表皮壊死症(ライエル症候群)、薬剤性過敏症症候群が起こることがある。
注意喚起
[編集]2012年1月には医薬品医療機器総合機構(PMDA)より、用量の多い場合に皮膚障害の副作用が発症しやすくなるため、用量遵守についての注意喚起がなされた[2]。日本での統計では皮膚症状の発生頻度は、服用量を遵守した場合に2.9%、承認された用量より多い場合には10.4%であった[2]。
死亡例
[編集]バルプロ酸またはフルボキサミン使用例にラモトリギンを追加投与する際、添付文書上は25mg/隔日または25mg/日と定められているが、50mg/日から開始したために、薬剤性過敏症症候群を来し死亡した症例が報告されている[12]。
2014年内にラモトリギンを服用していた4人が、重度の皮膚障害を発症した後に死亡したことが判明した。適正量を超えて医療機関から処方された薬を服用したとみられており、皮膚障害が出た後も投薬が続けられていた[13]。
2015年2月4日には皮膚障害による死亡例を受けて厚生労働省から安全性速報が出され[3]、用量遵守の警告を含むよう添付文書が改定された[3]。
2015年4月20日、日本うつ病学会、日本神経精神薬理学会、日本臨床精神神経薬理学会の理事長は連名で声明を行い、医師に対して、ラモトリギンの効果と安全性、特に皮膚症状について患者に説明し同意を得て(インフォームド・コンセント)、用量と投与間隔、併用薬を確認するようお願いしている[11]。
なお、用量が守られなかった場合には、PMDAによる医薬品副作用被害救済制度は適用されない[11]。
併用注意
[編集]薬物相互作用を起こす医薬品も多く、併用により重篤な副作用が出やすくなるため注意が必要である。
- バルプロ酸ナトリウム
- ラモトリギンの消失半減期が約2倍に延長するとの報告がある。
- グルクロン酸胞合を誘導する薬剤
- フェニトイン・カルバマゼピン・フェノバルビタール・プリミドン・リファンピシン・ロピナビル・リトナビル配合剤など
- 血中濃度の低下。
- アタザナビル/リトナビル
- 血中濃度の低下。
- カルバマゼピン
- 眩暈、失調、複視、霧視、嘔吐などの副作用が発生。
- リスペリドン
- 傾眠の副作用上昇傾向あり。
- 経口避妊薬(卵胞ホルモン・黄体ホルモン配合剤)
- 血中濃度の低下。
主な副作用
[編集]重篤な副作用
[編集]- 発熱、目充血、顔面の浮腫み、皮膚・粘膜のびらん、水泡、紅斑、咽頭痛、瘙痒、全身倦怠感。
- 市販後調査により日本ではラミクタールによるスティーブンス・ジョンソン症候群は55,000名に処方されたうち10名に発症している。米国0.08%、すなわち1200~1300人にラミクタールによるSJSが発症していると報告された。これらはいずれもラミクタールによりSJS発症頻度が薬剤として最も高いことを示している。
- 薬剤性過敏症症候群(発疹、発熱、リンパ節症、顔面の浮腫み、血液障害、肝障害など)(頻度不明)
- 再生不良性貧血(頻度不明)
- 汎血球減少(頻度不明)
- 無顆粒球症(頻度不明)
- 肝炎・肝機能障害および黄疸(頻度不明)
- 無菌性髄膜炎
その他副作用
[編集]- 5%未満
- 発疹、眩暈、傾眠、肝機能検査値異常
- 1~5%未満
- 頭痛、不眠、失調、易刺激性、不安・焦燥・興奮、てんかん発作の増加、胃腸障害(吐気、嘔吐、下痢など)、食欲不振、白血球減少、貧血、好中球減少、血小板減少、複視
高齢者では、生理機能が低下しているため慎重投与が必要である。
2008年、アメリカ食品医薬品局(FDA)は、199の二重盲検試験を分析し、データに用いられた24週間では、抗てんかん薬服用時の自殺念慮や自殺企図が2倍(てんかん用途では3.5倍、精神科では1.5倍)に高まることを警告した(それ以上の期間は単に未調査)[14]。2009年4月23日以降、認可されたすべての抗てんかん薬に警告表示が追加された[15]。日本でも、自殺企図の既往や自殺念慮を有する場合に注意書きがある[6]。
妊婦、授乳婦への投与
[編集]妊娠中の投与に関する安全性が認められていない。海外での調査において妊婦の服用により、大奇形発現リスクの増加は認められてはいないが、慎重投与が必要である。授乳中の婦人には、投薬中は授乳を避けること。
関連項目
[編集]出典
[編集]- ^ a b CG137: Epilepsies: diagnosis and management (Report). 英国国立医療技術評価機構. January 2012. Chapt.1.4.
- ^ a b c ラミクタール錠(ラモトリギン)の重篤皮膚障害と用法・用量 遵守、早期発見について (PMDAからの医薬品適正使用のお願いNo6) (pdf) (Report). 医薬品医療機器総合機構. January 2012. 2013年1月1日閲覧。
- ^ a b c “抗てんかん薬、双極性障害治療薬「ラミクタール錠」投与患者における重篤な皮膚障害に関する注意喚起について”. 厚生労働省 (2015年2月4日). 2015年10月1日閲覧。
- ^ Nassir Ghaemi S, Shirzadi AA, Filkowski M (2008). “Publication bias and the pharmaceutical industry: the case of lamotrigine in bipolar disorder”. Medscape J Med 10 (9): 211. PMC 2580079. PMID 19008973.
- ^ 黒木俊秀「抗うつ薬時代の憂うつ」『現代うつ病の臨床』187~211頁。
- ^ a b “ラミクタール錠小児用2mg/ラミクタール錠小児用5mg/ラミクタール錠25mg/ラミクタール錠100mg 添付文書” (2015年9月). 2016年11月6日閲覧。
- ^ 日本うつ病学会 2012, p. 8, 17.
- ^ a b 日本うつ病学会 2012, p. 18.
- ^ 日本うつ病学会 2012, p. 14.
- ^ CG173: Neuropathic pain in adults: pharmacological management in non-specialist settings (Report). 英国国立医療技術評価機構. November 2013. Chapt.1.1.
- ^ a b c 日本うつ病学会理事長・尾崎紀夫、日本神経精神薬理学会理事長・石郷岡純、日本臨床精神神経薬理学会理事長・大谷浩一『ラモトリギンに関する連名ステートメント』(pdf)(レポート)2015年4月20日。
- ^ “GSKの抗てんかん薬・ラミクタール 皮膚障害で死亡例 用法・用量の遵守喚起” (2015年1月14日). 2015年1月14日閲覧。
- ^ 抗てんかん薬:4人死亡…適正用量超え服用
- ^ “Postmarket Drug Safety Information for Patients and Providers > Information for Healthcare Professionals: Suicidal Behavior and Ideation and Antiepileptic Drugs”. U.S. Food and Drug Administration (FDA) (2008年1月31日). 2013年1月15日閲覧。
- ^ “Postmarket Drug Safety Information for Patients and Providers > Suicidal Behavior and Ideation and Antiepileptic Drugs”. U.S. Food and Drug Administration (FDA) (2009年5月5日). 2013年1月15日閲覧。
参考文献
[編集]- グラクソ・スミスクライン株式会社 ラミクタール 添付文書
- 日本うつ病学会; 気分障害の治療ガイドライン作成委員会 (16 June 2020). 日本うつ病学会治療ガイドライン I.双極性障害 2020 (pdf) (Report) (第4回改訂 ed.). 日本うつ病学会. 2023年12月6日閲覧。
