アインスタイニウム
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 外見 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
銀白色
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 一般特性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 名称, 記号, 番号 | アインスタイニウム, Es, 99 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 分類 | アクチノイド | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 族, 周期, ブロック | n/a, 7, f | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子量 | [252] | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子配置 | [Rn] 5f11 7s2 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子殻 | 2, 8, 18, 32, 29, 8, 2(画像) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理特性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 相 | 固体 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度(室温付近) | 8.84 g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 融点 | 1133 K, 860 °C, 1580 °F | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子特性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 酸化数 | 2, 3, 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 電気陰性度 | 1.3(ポーリングの値) | |||||||||||||||||||||||||||||||||||||||||||||||||||
| イオン化エネルギー | 1st: 619 kJ/mol | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 共有結合半径 | 165 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||
| その他 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 結晶構造 | 六方最密充填構造 (α-Es)
面心立方格子 (β-Es) 〔300℃で相転移〕 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 磁性 | 常磁性 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS登録番号 | 7429-92-7 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| 主な同位体 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細はアインスタイニウムの同位体を参照 | ||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||
アインスタイニウム (英: einsteinium [aɪnˈstaɪniəm]) は原子番号99の元素。元素記号はEs。人工放射性元素であり、アクチノイド系列の元素の1つであり、7番目の超ウラン元素である。
名称[編集]
元素名は、アルベルト・アインシュタインに由来する。
概要[編集]
1952年の最初の水爆の爆発による破片の一部として発見された。最も一般的な同位体であるアインスタイニウム253(半減期20.47日)は、年間1ミリグラム程度の総収量で、いくつかの専用高出力原子炉におけるカリホルニウム253の崩壊から人工的に生成される。原子炉での合成に続いて、アインスタイニウム253を他のアクチノイドおよびそれらの崩壊生成物から分離する複雑な工程がある。他の同位体は、重いアクチノイド元素に軽いイオンを衝突させることで、さまざまな実験室で合成されているものの、アインスタイニウム253に比べてはるかに少量である。生成されるアインスタイニウムが少量であり、最も簡単に生成される同位体の半減期が短いため、現在のところ実用的な用途はほとんどなく、もっぱら基礎的な科学研究に用いられる。特に、アインスタイニウムは、1955年に初めて新元素メンデレビウムの17個の原子を合成するために使用された。
アインスタイニウムは柔らかく銀色の常磁性の金属である。化学的性質はアクチノイド系列後半の典型であり、+3の酸化状態が優勢である。+2酸化状態も(特に固体で)とることができる。アインスタイニウム253の高い放射能は、可視光の輝きを生み出し、1グラムあたり約1000ワットの熱を放出しその結晶性金属格子を急速に損傷する。1日で約3%のアインスタイニウム253が崩壊してバークリウム249に、そこからさらにカリホルニウム249になるため、特性を研究するのが難しい。半減期が最も長いアインスタイニウムの同位体であるアインスタイニウム252(半減期471.7日)は、物理的性質の研究に適しているが、製造がかなり難しいことが分かっており、微量でしか入手できず、大量一括には手に入らない[1]。純粋な形で巨視的な量で観察される最大の原子番号を持つ元素であり、これは一般的な短寿命の同位体アインスタイニウム253でなされた[2]。
すべての人工超ウラン元素と同様に、アインスタイニウムの同位体は非常に放射性が高く、摂取すると健康に非常に危険であると考えられている[3]。
歴史[編集]

アインスタイニウムは1952年12月、カリフォルニア大学バークレー校のアルバート・ギオルソとその共同研究者によりアルゴンヌとロスアラモス国立研究所との共同研究でアイビー・マイク核実験の放射性降下物の中から初めて同定された。この実験は1952年11月1日に太平洋のエニウェトク環礁で実施され、水爆実験としては初の成功を収めた[4]。爆発の破片を最初調べたところプルトニウムの新たな同位体244
94Puが生成されていることが分かったが、これはウラン238の原子核が6個の中性子を吸収したのち2回のベータ崩壊を経て生成されたと考えられている。
当時、複数の中性子吸収は極めて珍しい現象と考えられていたが、244
94Puが同定されたことでウランの原子核にさらに多くの中性子が取り込まれカリホルニウムより重い新元素が生成される可能性が示唆された[4]。

ギオルソと共同研究者らは、ろ紙を備えた飛行機に爆発雲の中を飛ばせ、得られたろ紙を分析した(244
94Puの発見に使われたのと同じサンプリング技術)[5]。後には、より大量の放射性物質が環礁のサンゴの残骸から分離され、アメリカに運ばれた[4]。未知の元素の可能性がある物質の分離は、弱酸性媒質(pH ≈ 3.5)中のクエン酸/アンモニウム緩衝液の存在下で高温でのイオン交換を用いて行われた。最終的に回収されたアインスタイニウムの原子数は200以下であった[6]。しかし、元素99(アインスタイニウム)、すなわちその253Esの同位体は6.6 MeVの特徴的な高エネルギーアルファ崩壊によって検出された[4]。これはウラン238核による15個の中性子の捕獲とそれに続く7度のベータ崩壊により生成され、半減期は20.5日であった。このような複数の中性子吸収は爆発中の高い中性子束密度により可能になったため、新たに生成された重い同位体は軽い元素に分解する前に吸収できる中性子が十分多くあった。中性子捕獲により最初核種の原子番号を変えずに質量数を上げ、付随して起こるベータ崩壊により原子番号が徐々に増加する[4]。
ただし一部の238U原子はさらに2個の中性子を吸収し(合計17個)、255Esと別の新たな元素フェルミウムの255Fm同位体を生成することがある[7]。新たな元素の発見と複数の中性子捕獲に関する関連する新たなデータは当初、冷戦の緊張と核技術におけるソ連との競争により1955年まで米軍の命令により秘密にされていた[4][8][9]。しかし、非常に多くの中性子の急速な捕獲は、ベータ崩壊前に超新星爆発における特定の重い化学元素(ニッケルより重い)の宇宙元素合成(生成)を説明するために必要ないわゆるr過程複数中性子吸収の必須な直接的な実験的確認を提供する。このような過程は宇宙における多くの安定した元素の存在を説明するために必要である[10]。
一方、元素99(および新たな元素100フェルミウム)の同位体はバークレーおよびアルゴンヌ研究所で窒素14とウラン238の間の核反応で生成され[11]、その後、プルトニウムかカリホルニウムの強い強い中性子照射により生成された。
これらの結果は1954年にいくつかの論文において、この元素について実施された最初の研究ではないという声明つきで発表された[12][13][14][15][16]。また、バークレーのチームはアインスタイニウムとフェルミウムの化学的性質に関するいくつかの結果を報告した[17][18]。アイビー・マイクの結果は機密指定ではなくなり、1955年に公開された[8]。

元素99と100の発見で、アメリカのチームはスウェーデンのストックホルムにあるノーベル物理学研究所のグループと争った。1953年後半から1954年初めにかけてスウェーデンのグループはウランに酸素原子核を衝突させることで元素100の軽い同位体、特に250Fmの合成に成功した。これらの結果は1954年にも発表された[19]。それにもかかわらず、バークレーのチームの発表がスウェーデンの論文よりも先であったため、バークレーのチームが先であることが承認された。バークレーの発表は1952年の熱核爆発のこれまで開示されていなかった結果に基づいていた。したがって、バークレーのチームに新たな元素に名前を付ける特権が与えられた。アイビー・マイクの設計につながった取り組みがプロジェクトPANDA[20]というコードネームであったため、元素99はジョークで「パンダモニウム」と呼ばれていた[21]。しかし、正式名はバークレーのグループにより2人の著名な科学者アルベルト・アインシュタインとエンリコ・フェルミに由来するものが提案された。「われわれは原子番号99の元素の名前にはアルベルト・アインシュタインにちなんでアインスタイニウム(記号E)と名付け、原子番号100の元素の名前にはエンリコ・フェルミにちなんでフェルミウム(記号Fm)と名付けた」[8]アインシュタインとフェルミはともに名称が最初に提案されたときから命名が公式に発表されるまでに死去している。これらの新たな元素の発見は、1955年8月8-20日に開催された最初のジュネーブ原子会議でアルバート・ギオルソにより発表された[4]。元素記号は当初Eであったが、後にIUPACによりEsに変更された[22][23]。
特徴[編集]
物理的性質[編集]

アインスタイニウムは人工の、銀白色の放射性金属である。周期表ではアクチノイドのカリホルニウムの右、アクチノイドのフェルミウムの左、ランタノイドのホルミウムの下に配置されており、ホルミウムとは多くの類似した物理的および化学的特性を共有する。密度8.84 g/cm3はカリホルニウムの密度(15.1 g/cm3)より低く、ホルミウムの密度(8.79 g/cm3)とほぼ同じであるが、アインスタイニウム原子はホルミウムよりもずっと重い。融点も比較的低く(860 °C)、カリホルニウム(900 °C)、フェルミウム(1527 °C)、ホルミウム(1461 °C)よりも低い[3][25]。軟質金属であり体積弾性率はわずか15GPaであり、この値は非アルカリ金属の中で最も低いものの1つである[26]。
周囲条件で二重六方構造で結晶化するより軽いアクチノイド、カリホルニウム、バークリウム、キュリウム、アメリシウムとは対照的にアインスタイニウムは空間群Fm3m、格子定数a = 575 pmの面心立方(fcc)対称性を持っていると考えられている。しかし、a=398pm、c=650pmの室温の六方アインスタイニウム金属の報告があり、300℃に加熱するとfcc相に変換される[27]。
アインスタイニウムの放射能により引き起こされる自己損傷は非常に強いため、結晶格子は急速に破壊され[28]、この過程で253Es1グラム当たり1000ワットのエネルギーを放出し、可視光の輝きを放つ[2]。これらの過程はアインスタイニウムの密度と融点が比較的低い原因である可能性がある[29]。さらに、使うことができる試料の大きさが小さいため、電子顕微鏡内で加熱されている試料を観察することにより融点がしばしば推定された[30]。したがって小さな試料の表面効果により融点の値が低くなる可能性がある。
この金属は2価であり、著しく高い揮発性を持っている[31]。自己放射線による損傷を減らすために、固体のアインスタイニウムとその化合物を測定するときはほとんどそれらを熱アニーリングした直後に行われる[32]。また、一部の化合物は還元ガスの雰囲気下で研究される。例えば、EsOClの場合はH2O+HClであるため、分解中に試料が部分的に再成長する[33]。
固体のアインスタイニウムとその化合物の自己破壊とは別に、この元素を研究する上での本質的な困難には希少性(最も一般的な253Es同位体は1ミリグラム未満の量で1年に1,2回しか使用することができない)と自己汚染(1日当たり約3.3%の割合でアインスタイニウムからバークリウム、そしてカリホルニウムに急速に変化する)が含まれる[34][35][36]。
よって、ほとんどのアインスタイニウムの試料は汚染されており、それらの固有の特性は時間の経過とともに蓄積された実験データを外挿することで推定されることがしばしばある。汚染の問題を回避する他の実験的手法には、発光特性の研究などで波長可変レーザーによるアインスタイニウムイオンの選択的光励起などがある[37]。
アインスタイニウム金属やその酸化物およびフッ化物の磁気特性が研究されてきた。3つの材料全てが液体ヘリウムから室温まででキュリー・ワイス常磁性の挙動を示した。有効磁気モーメントはEs2O3では10.4±0.3 µBであり、EsF3では11.4±0.3 µBであり、これらの値はアクチノイドの中で最も高い値であり、対応するキュリー温度は53および37Kである[38][39]。
化学的性質[編集]
すべてのアクチノイド同様、アインスタイニウムは高い反応性を持つ。3価の酸化状態は固体や水溶液中で最も安定であり、その状態で淡いピンク色となる[40]。2価のアインスタイニウムの存在が特に固相ではしっかりと確立されており、このような+2状態はプロトアクチニウム、ウラン、ネプツニウム、プルトニウム、キュリウム、バークリウムなどの他の多くのアクチノイドでは観察されていない。アインスタイニウム(II)化合物は例えばアインスタイニウム(III)を塩化サマリウム(II)で還元することにより得られる[41]。酸化状態+4は蒸気の研究から推定されているが、未だ不明である[42]。
同位体[編集]
アインスタイニウムには19個の同位体と3個の核異性体があり、質量数は240から257の範囲である。すべて放射性であり、最も安定した核種である252Esは半減期が471.7日である[43]。次に安定の同位体は254Es(半減期275.5日)[44]、255Es(39.8日)、253Es(20.47日)である。残りの同位体はすべて半減期が40時間未満であり、ほとんどの同位体が30分以内に崩壊する。3つの核異性体のうち、最も安定なのは254mEsであり半減期は39.3時間である[45]。
核分裂[編集]
アインスタイニウムは核分裂率が高く、結果として持続的な核連鎖反応の臨界質量が低くなる。この質量は254Es同位体の裸球(bare sphere)の場合は9.89kgであり、厚さ30cmの鋼製中性子反射体を加えることで2.9kgに、水から作った厚さ20cmの反射体を使用することで2.26kgに下げることができる。しかし、この小さい臨界質量でさえこれまでに分離されたアインスタイニウムの総量、特に希少な254Es同位体の総量を大幅に超えている[46]。
自然発生[編集]
アインスタイニウムのすべての同位体の半減期は短いため、原始アインスタイニウム、つまり地球が形成されている間に地球上に存在していた可能性のあるアインスタイニウムは崩壊してから長い時間が経っている。地殻で自然に天然に存在するアクチノイドのウランとトリウムからアインスタイニウムを合成するには、複数の中性子捕獲が必要であるがこれは極めて起こることのなさそうな事象である。したがってすべての地球上のアインスタイニウムは、科学実験室、高出力原子炉または核実験で生成され、合成したときから数年以内にのみ存在する[6]。
アインスタイニウム含むアメリシウムからフェルミウムまでの超ウラン元素はオクロの天然原子炉で自然に発生したが、現在は発生していない[47]。
2008年にはプシビルスキ星でアインスタイニウムが観測された[48]。
合成・抽出[編集]

アインスタイニウムは専用の高速原子炉で軽いアクチノイドに対して中性子を照射することで微量生成される。世界の主要な照射源は米国テネシー州のオークリッジ国立研究所にある85メガワットの高中性子束同位体生産炉(HFIR)[50]とロシア、ディミトロフグラードの原子炉科学技術研究所(Research Institute of Atomic Reactors, NIIAR)にあるSM-2ループ型原子炉[51]であり、どちらもキュリウム以上(Z > 96)の元素の生産に特化したものである。これらの施設はパワーと束レベルが似ており、NIIARで生産される量は広く報告されていないがキュリウム以上の元素の生産能力は同等であると期待されている[52]。オークリッジでの"typical processing campaign"では数十グラムのキュリウムが照射され、デシグラム量のカリホルニウム、ミリグラム量のバークリウム(249Bk)とアインスタイニウム、ピコグラム量のフェルミウムが生成される[53][54]。
253Esの最初の微視的試料は約10ナノグラムで、1961年にHFIRで調製された。重量を推定するために特別な磁気天秤が設計された[3][55]。その後、数キログラムのプルトニウムから始まり1967年から1970年には0.48ミリグラム(ほとんどが253Es)、1971年から1973年には3.2ミリグラムの大量のバッチが生産され、その後1974年から1978年まで安定して年間約3ミリグラムが生産された[56]。ただしこれらの量は照射直後のターゲットの積分量を指す。その後の分離手順により同位体的に純粋なアインスタイニウムは約10分の1に減少した[52]。
実験室での合成[編集]
プルトニウムの重中性子照射によりアインスタイニウムの4つの主要な同位体が得られる。4つとは253Es(半減期が20.47日で自発核分裂半減期が7×105年のα放射体)、254mEs(半減期が39.3時間のβ放射体)、254Es(半減期が約276日のα放射体)、255Es(半減期が39.8日のβ放射体)である[57][58]。別のルートは高強度の窒素または酸素イオンビームによるウラン238の衝突を含む[59]。
アインスタイニウム247(半減期4.55分)はアメリシウム241に炭素イオンをもしくはウラン238に窒素イオンを照射することにより生成された[60]。後者の反応は1967年にロシアのドゥブナで最初に実現し、関係した科学者にはLenin Komsomol Prizeが授与された[61]。
同位体248Esは重水素イオンを249Cfに照射することで生成された。248Esは主に電子の放出により248Cfに半減期25±5分で崩壊するが、6.87 MeVのエネルギーのα粒子を放出する(電子とα粒子の比は約400である)[62]。
重い同位体249Es、250Es、251Es、252Esは249Bkにα粒子を衝突させることで得られた。この過程で1つから4つの中性子が解放され、1回の反応で4つの異なる同位体を形成できる[63]。
アインスタイニウム253は0.1–0.2ミリグラムの252Cfターゲットに(2–5)×1014 中性子·cm−2·s−1の熱中性子束を500–900時間照射することで生成された[64]。
核爆発における合成[編集]

10メガトンのアイビー・マイク核実験のデブリの分析は、長期プロジェクトの一環であった。この目的の1つは高出力核爆発における超ウラン元素の生産効率の研究であった。これらの実験の動機はウランから超ウラン元素を合成するためには中性子を何度も捕獲する必要があるということであった。このような事象が発生する確率は中性子束とともに高くなるが、核爆発は最も強力な人工中性子源であり、マイクロ秒以内に1023中性子/cm2オーダーの密度、すなわち約1029中性子/(cm2·s)を供給する。これに比べ、HFIR原子炉の中性子束は5×1015 中性子/(cm2·s)である。デブリの試料が米国本土に届くまでにいくつかの同位体が崩壊する可能性があるため、予備分析のための専用の実験室がエニウェトク環礁に設置された。実験室は、実験後に環礁の上空を飛行する紙フィルターを備えた飛行機から分析用の試料をできるだけ早く受け取っていた。フェルミウムより重い新たな化学元素を発見することが望まれていたが、1954年から1956年の間に環礁で一連のメガトン爆発が行われた後にもこれらが発見されることはなかった[5]。
閉ざされた空間で起こる強力な爆発により収量が向上し同位体が重くなることが期待されていたため、大気での結果は1960年代にネバダ核実験場で蓄積された地下での実験データにより補われた。従来のウランチャージとは別に、ウランとアメリシウムおよびトリウムの組み合わせ、およびプルトニウムとネプツニウムの混合チャージが試みられたが収量の点ではあまりうまくいかず、これは重元素チャージの核分裂率が上がったことで重同位体の損失が大きくなったのが原因であった。爆発が周囲の岩を300-600メートルの深さで溶かして蒸発させてデブリを撒き広げているため、生成物の分離には問題があった。生成物を抽出するためにそのような深さまで掘削することは収集する量という点で遅く非効率な方法であった[5][65]。
1962年から1969年まで行われた9回の地下実験のうち[66][67]、最後の実験は最も強力であり、超ウラン元素の収量が最も高かった。高出力の原子炉で通常1年間照射して作られるミリグラムのアインスタイニウムが、マイクロ秒以内に生成された[65]。しかし、全体の提案の主な現実的問題は強力な爆風により分散した放射性のデブリを集めることであった。航空機のフィルターは全量の約4×10−14しか吸着せず、エニウェトク環礁のサンゴ数トン集めることでこの割合を2桁のみ上げることができた。Hutch爆発から60日後に約500kgの地下岩を抽出しても総チャージの約1×10−7しか取り戻せなかった。この500kgのバッチ中の超ウラン元素の量は実験の7日後に採取した0.4kgの岩に含まれていたもののたった30倍であり、回収した放射性岩石の量に対する超ウラン元素の収量の非常に非線形な依存性が示された[68]。爆発後の試料回収を早くするために実験前にその場所でシャフトを掘削した。これにより爆発により震源からシャフトを介して放射性物質が放出され、表面近くで多くの物質が回収された。この方法は2つの実験で試され、すぐに数百キログラムの材料が提供されたが、アクチノイド濃度は掘削後に得られた試料の3分の1であった。このような方法は短命の同位体の科学的研究では効率的であったかもしれないが、生成されたアクチノイドの全体的な収集効率を改善することはできなかった[69]。
核実験のデブリからは新たな元素(アインスタイニウムとフェルミウムを除く)を検出できず、超ウラン元素の総収量は残念なほど低かったが、これらの実験ではそれより前に実験室で得ることができたものよりもはるかに大量の希少な重同位体が得られた[70]。
分離[編集]
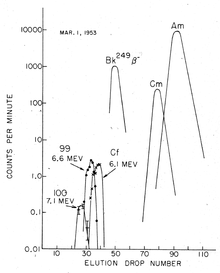
アインスタイニウムの分離手順は合成方法により異なる。サイクロトロン内の軽イオン衝突の場合、重イオンターゲットは薄い箔に取り付けられ、生成されたアインスタイニウムは照射後に箔から簡単に洗い流せる。しかし、そのような実験での生成量は比較的少ない[71]。原子炉での照射の場合は収量がずっと高くなるが、生成物はさまざまなアクチノイド同位体の混合物であるだけでなく核分裂崩壊で生成されるランタノイドも含まれる。この場合、アインスタイニウムを単離するには高温高圧での陽イオン交換とクロマトグラフィーの何度かの反復手順を含む面倒な手順をしなくてはならない。原子炉で最も一般的に生成されるアインスタイニウムの同位体である253Esは半減期わずか20日(ほとんどの実験のタイムスケールでは早い)で249Bkに崩壊するためバークリウムからの分離が重要である。このような分離はバークリウムが固体の+4状態に容易に参加して沈殿するのに対し、アインスタイニウム含む他のアクチノイドは溶液中で+3状態のままであるという事実に依存して行われる[72]。
ランタノイド核分裂生成物からの3価アクチノイドの分離は、溶離液として塩酸(HCl)で飽和した90%水/10%エタノール溶液を使用する陽イオン交換樹脂カラムで行うことができる。その後、溶離液として6モル濃度のHClを使用する陰イオン交換クロマトグラフィーを行う。次にアンモニウム塩で処理された陽イオン交換樹脂カラム(Dowex-50交換カラム)を使用して、元素99、元素100、元素101を含む断片を分離する。これらの元素は例えば溶離液としてα-ヒドロキシイソ酪酸溶液(α-HIB)を使用して、溶離位置/時間に基づいて簡単に識別できる[73]。
3+アクチノイドの分離は、ビス-(2-エチルヘキシル)リン酸(HDEHPと略される)を固定有機相として、硝酸を移動水相として使用する溶媒抽出クロマトグラフィーによっても実現できる。アクチノイド溶離のシーケンスは陽イオン交換樹脂カラムの溶離のシーケンスと逆になる。この方法で分離されたアインスタイニウムは、樹脂カラムを使用した分離と比較して有機錯化剤を含まないという利点がある[73]。
金属の調製[編集]
アインスタイニウムは反応性が高いため、その化合物から純粋な金属を得るには強力な還元剤が必要である[74]。これは金属リチウムによるフッ化アインスタイニウム(III)の還元により達成できる。
- EsF3 + 3 Li → Es + 3 LiF
しかし、融点が低く自己放射線による損傷が高いため、蒸気圧が高くフッ化リチウムよりも蒸気圧が高い。これによりこの還元反応はかなり非効率になる。これは初期に試されたが、ランタン金属による酸化アインスタイニウム(III)の還元が支持されるとすぐに放棄された[27][29][75]。
- Es2O3 + 2 La → 2 Es + La2O3
化合物[編集]
| 化合物 | 色 | 対称性 | 空間群 | No | ピアソン記号 | a (pm) | b (pm) | c (pm) |
|---|---|---|---|---|---|---|---|---|
| Es2O3 | 無色 | 立方[35] | Ia3 | 206 | cI80 | 1076.6 | ||
| Es2O3 | 無色 | 単斜[76] | C2/m | 12 | mS30 | 1411 | 359 | 880 |
| Es2O3 | 無色 | 六方[76] | P3m1 | 164 | hP5 | 370 | 600 | |
| EsF3 | 六方[34] | |||||||
| EsF4 | 単斜[77] | C2/c | 15 | mS60 | ||||
| EsCl3 | 橙色 | 六方[78][79] | C63/m | hP8 | 727 | 410 | ||
| EsBr3 | 黄色 | 単斜[80] | C2/m | 12 | mS16 | 727 | 1259 | 681 |
| EsI3 | 琥珀色 | 六方[81][82] | R3 | 148 | hR24 | 753 | 2084 | |
| EsOCl | 正方[81][83] | P4/nmm | 394.8 | 670.2 |
酸化物[編集]
酸化アインスタイニウム(III)(Es2O3)は硝酸アインスタイニウム(III)を燃焼させることにより得られた。これは無色の立方晶を形成し、最初に大きさが約30ナノメートルのマイクログラムの試料から特徴づけられた[28][35]。この酸化物には他に単斜晶系や六方晶系の2つの相が知られている。特定のEs2O3相の形成は調製技術と試料の来歴に依存し、明確な相図はない。自己照射または自己発熱の結果として3つの相の間で相互変換が自然発生する可能性がある[84]。六方相は酸化ランタン(III)とアイソタイプであり、Es3+イオンがO2−イオンの6配位群で囲まれている[76][81]。
ハロゲン化物[編集]

アインスタイニウムのハロゲン化物は、酸化状態+2および+3で知られている[83][85]。最も安定した状態はフッ化物からヨウ化物までのすべてのハロゲン化物で+3である。
フッ化アインスタイニウム(III)(EsF3)はフッ化物イオンとの反応により塩化アインスタイニウム(III)溶液から沈殿する。代わりの調製手段は酸化アインスタイニウム(III)を1-2気圧、300-400℃の温度で三フッ化塩素(ClF3)もしくはF2ガスにさらすことである。EsF3結晶構造は六方晶系であり、フッ化カリホルニウム(III)(CfF3)のようにEs3+イオンが二面冠(bicapped)三角柱配置でフッ素イオンが8個配位されている[34][86][87]。
塩化アインスタイニウム(III)(EsCl3)は、約500℃で約20分間、乾燥塩化水素蒸気の雰囲気中で酸化アインスタイニウム(III)をアニーリングすることで調製できる。約425℃に冷却すると結晶化し、UCl3タイプの六方構造を持つ橙色の固体になる。ここではアインスタイニウム原子は三面冠(tricapped)三角柱形状で塩素原子が9個配位している[79][86][88]。臭化アインスタイニウム(III)(EsBr3)は、AlCl3タイプの単斜構造を持つ淡黄色の固体であり、アインスタイニウム原子は臭素が八面体的に配位している(配位数6)[82][86]。
アインスタイニウムの2価化合物は、3価ハロゲン化物を水素で還元することにより得られる[89]。
- 2 EsX3 + H2 → 2 EsX2 + 2 HX, X = F, Cl, Br, I
塩化アインスタイニウム(II)(EsCl2)[90]、臭化アインスタイニウム(II)(EsBr2)[91]、ヨウ化アインスタイニウム(II)(EsI2)[83]は光吸収により生成され特徴づけられているが、構造に関する情報はまだ知られていない[82]。
既知のアインスタイニウムのオキシハロゲン化物にはEsOCl[83]、EsOBr[89]、EsOIがある[83]。これらは水と対応するハロゲン化水素の蒸気混合物で三ハロゲン化物を処理することで合成される。例えばEsOClを得るためのEsCl3 + H2O/HCl[33]
有機アインスタイニウム化合物[編集]
アインスタイニウムの高い放射能は放射線療法での潜在的な用途があり、有機金属錯体はアインスタイニウム原子を体内の適切な臓器に届けるために合成されている。クエン酸アインスタイニウム(およびフェルミウム化合物)を犬に注射する実験が行われている[2]。アインスタイニウム(III)もベータジケトンキレート錯体に組み込まれたが、これはランタノイドと類似の錯体が以前有機金属化合物の中で最も強いUV励起発光を示したためである。アインスタイニウム錯体を調製するとき、Es3+イオンはGd3+イオンで1000倍に希釈され、これにより測定に必要な20分間に化合物が崩壊しないように放射線による損傷を減らすことができた。結果生じたEs3+からの発光は非常に弱く、検出することができなかった。このことはキレートマトリックスからEs3+イオンへの効率的なエネルギー移動を妨げる化合物の個々の構成要素の好ましくない相対エネルギーにより説明された。他のアクチノイドのアメリシウム、バークリウム、およびフェルミウムについても同様の結論が出された[92]。
しかし、Es3+イオンの発光は無機塩酸溶液やジ(2-エチルヘキシル)オルトリン酸を含む有機溶液で観察された。これは約1064nm(約100nmの半値幅)に広いピークを示し、緑色光(波長約495nm)により共鳴的に励起される。発光の寿命は数マイクロ秒で量子収率は0.1%未満である。ランタノイドと比較してEs3+の非放射減衰率は比較的高く、f電子と内部Es3+電子の相互作用が強いことに関連していた[93]。
用途[編集]
アインスタイニウムより上の超ウラン元素や超アクチノイド元素の生成を目的とした基礎科学研究以外では、アインスタイニウムの同位体はほとんど使用されていない[94]。
1955年、メンデレビウムはバークレー研究所の60インチサイクロトロンで253Esの約109個の原子からなるターゲットを照射することで合成された。結果生じる253Es(α,n)256Md反応により原子番号101の新たな元素の原子が17個生成された[95]。
希少な同位体アインスタイニウム254は質量が大きく、半減期が270日と比較的長く、数マイクログラムと多くの量を手に入れられることから超重元素を生成するのに好まれている[96]。アインスタイニウム254は1985年にカリフォルニア州バークレーにあるsuperHILAC線形加速器で行われたカルシウム48イオンを衝突させることによりウンウンエンニウム(元素119)の合成する試みのターゲットとして使用された。原子は確認されず、この反応の断面積の上限は300ナノバーンに設定された[97]。
アインスタイニウム254は月探査機サーベイヤー5号の化学分析分光計(「アルファ散乱表面分析器」)の較正マーカーとして使用された。この同位体の大きな質量により、マーカーからの信号と月面で調査された軽い元素の間のスペクトルの重なりが減少した[98]。
安全性[編集]
入手できるアインスタイニウムの毒性データのほとんどは動物の研究に基づいている。ラットが摂取すると血流にとどまるのは約0.01%だけである。血流から約65%は骨に行き、およそ50年間そこに残る。25%は肺に行き(生物学的半減期は約20年であるがこれはアインスタイニウムの同位体の短い半減期とは無関係である)、0.035%が睾丸にまたは0.01%が卵巣に行きアインスタイニウムがずっと留まる。摂取量の約10%は排泄される。骨表面におけるアインスタイニウムの分布は均一であり、プルトニウムの分布と同様である[99]。
出典[編集]
- ^ Einsteinium. periodic.lanl.gov
- ^ a b c Haire, p. 1579
- ^ a b c Hammond C. R. "The elements" in Lide, D. R., ed. (2005), CRC Handbook of Chemistry and Physics (86th ed.), Boca Raton (FL): CRC Press, ISBN 0-8493-0486-5
- ^ a b c d e f g Ghiorso, Albert (2003). “Einsteinium and Fermium”. Chemical and Engineering News 81 (36): 174–175. doi:10.1021/cen-v081n036.p174.
- ^ a b c Seaborg, p. 39
- ^ a b John Emsley Nature's building blocks: an A-Z guide to the elements, Oxford University Press, 2003, ISBN 0-19-850340-7 pp. 133–135
- ^ 254Es, 254Fm and 253Fm would not be produced because of lack of beta decay in 254Cf and 253Es
- ^ a b c Ghiorso, A.; Thompson, S.; Higgins, G.; Seaborg, G.; Studier, M.; Fields, P.; Fried, S.; Diamond, H. et al. (1955). “New Elements Einsteinium and Fermium, Atomic Numbers 99 and 100”. Phys. Rev. 99 (3): 1048–1049. Bibcode: 1955PhRv...99.1048G. doi:10.1103/PhysRev.99.1048. Google Books
- ^ Fields, P.; Studier, M.; Diamond, H.; Mech, J.; Inghram, M.; Pyle, G.; Stevens, C.; Fried, S. et al. (1956). “Transplutonium Elements in Thermonuclear Test Debris”. Physical Review 102 (1): 180–182. Bibcode: 1956PhRv..102..180F. doi:10.1103/PhysRev.102.180. Google Books
- ^ Byrne, J. Neutrons, Nuclei, and Matter, Dover Publications, Mineola, NY, 2011, ISBN 978-0-486-48238-5 (pbk.) pp. 267.
- ^ Ghiorso, Albert; Rossi, G. Bernard; Harvey, Bernard G.; Thompson, Stanley G. (1954). “Reactions of U-238 with Cyclotron-Produced Nitrogen Ions”. Physical Review 93 (1): 257. Bibcode: 1954PhRv...93..257G. doi:10.1103/PhysRev.93.257.
- ^ Thompson, S. G.; Ghiorso, A.; Harvey, B. G.; Choppin, G. R. (1954). “Transcurium Isotopes Produced in the Neutron Irradiation of Plutonium”. Physical Review 93 (4): 908. Bibcode: 1954PhRv...93..908T. doi:10.1103/PhysRev.93.908.
- ^ Harvey, Bernard; Thompson, Stanley; Ghiorso, Albert; Choppin, Gregory (1954). “Further Production of Transcurium Nuclides by Neutron Irradiation”. Physical Review 93 (5): 1129. Bibcode: 1954PhRv...93.1129H. doi:10.1103/PhysRev.93.1129.
- ^ Studier, M.; Fields, P.; Diamond, H.; Mech, J.; Friedman, A.; Sellers, P.; Pyle, G.; Stevens, C. et al. (1954). “Elements 99 and 100 from Pile-Irradiated Plutonium”. Physical Review 93 (6): 1428. Bibcode: 1954PhRv...93.1428S. doi:10.1103/PhysRev.93.1428.
- ^ Choppin, G. R.; Thompson, S. G.; Ghiorso, A.; Harvey, B. G. (1954). “Nuclear Properties of Some Isotopes of Californium, Elements 99 and 100”. Physical Review 94 (4): 1080–1081. Bibcode: 1954PhRv...94.1080C. doi:10.1103/PhysRev.94.1080.
- ^ Fields, P.; Studier, M.; Mech, J.; Diamond, H.; Friedman, A.; Magnusson, L.; Huizenga, J. (1954). “Additional Properties of Isotopes of Elements 99 and 100”. Physical Review 94 (1): 209–210. Bibcode: 1954PhRv...94..209F. doi:10.1103/PhysRev.94.209.
- ^ Seaborg, G. T.; Thompson, S.G.; Harvey, B.G. and Choppin, G.R. (July 23, 1954) "Chemical Properties of Elements 99 and 100", Radiation Laboratory, University of California, Berkeley, UCRL-2591
- ^ Thompson, S. G.; Harvey, B. G.; Choppin, G. R.; Seaborg, G. T. (1954). “Chemical Properties of Elements 99 and 100”. Journal of the American Chemical Society 76 (24): 6229–6236. doi:10.1021/ja01653a004.
- ^ Atterling, Hugo; Forsling, Wilhelm; Holm, Lennart; Melander, Lars; Åström, Björn (1954). “Element 100 Produced by Means of Cyclotron-Accelerated Oxygen Ions”. Physical Review 95 (2): 585–586. Bibcode: 1954PhRv...95..585A. doi:10.1103/PhysRev.95.585.2.
- ^ Richard Lee Miller (1991). Under the cloud: the decades of nuclear testing. Two-Sixty Press. p. 115. ISBN 978-1-881043-05-8
- ^ John McPhee (1980). The Curve of Binding Energy. Farrar, Straus & Giroux Inc.. p. 116. ISBN 978-0-374-51598-0
- ^ Haire, p. 1577
- ^ Seaborg, G.T. (1994) Modern alchemy: selected papers of Glenn T. Seaborg, World Scientific, p. 6, ISBN 981-02-1440-5.
- ^ Haire, p. 1580
- ^ Haire, R. G. (1990) "Properties of the Transplutonium Metals (Am-Fm)", in: Metals Handbook, Vol. 2, 10th edition, (ASM International, Materials Park, Ohio), pp. 1198–1201.
- ^ Haire, p. 1591
- ^ a b Haire, R. (1986). “Preparation, properties, and some recent studies of the actinide metals”. Journal of the Less Common Metals 121: 379–398. doi:10.1016/0022-5088(86)90554-0.
- ^ a b Greenwood, p. 1268
- ^ a b Haire, R. G.; Baybarz, R. D. (1979). “Studies of einsteinium metal”. Le Journal de Physique 40: C4–101. doi:10.1051/jphyscol:1979431. draft manuscript
- ^ Seaborg, p. 61
- ^ Kleinschmidt, Phillip D.; Ward, John W.; Matlack, George M.; Haire, Richard G. (1984). “Henry's Law vaporization studies and thermodynamics of einsteinium-253 metal dissolved in ytterbium”. The Journal of Chemical Physics 81 (1): 473–477. Bibcode: 1984JChPh..81..473K. doi:10.1063/1.447328.
- ^ Seaborg, p. 52
- ^ a b Seaborg, p. 60
- ^ a b c Ensor, D. D.; Peterson, J. R.; Haire, R. G.; Young, J. P. (1981). “Absorption spectrophotometric study of 253EsF3 and its decay products in the bulk-phase solid state”. Journal of Inorganic and Nuclear Chemistry 43 (10): 2425–2427. doi:10.1016/0022-1902(81)80274-6.
- ^ a b c Haire, R. G.; Baybarz, R. D. (1973). “Identification and analysis of einsteinium sesquioxide by electron diffraction”. Journal of Inorganic and Nuclear Chemistry 35 (2): 489–496. doi:10.1016/0022-1902(73)80561-5.
- ^ Seaborg, p. 55
- ^ Seaborg, p. 76
- ^ Huray, P.; Nave, S.; Haire, R. (1983). “Magnetism of the heavy 5f elements”. Journal of the Less Common Metals 93 (2): 293–300. doi:10.1016/0022-5088(83)90175-3.
- ^ Huray, Paul G.; Nave, S. E.; Haire, R. G.; Moore, J. R. (1984). “Magnetic Properties of Es2O3 and EsF3”. Inorganica Chimica Acta 94 (1–3): 120–122. doi:10.1016/S0020-1693(00)94587-0.
- ^ Holleman, p. 1956
- ^ Seaborg, p. 53
- ^ Haire, p. 1578
- ^ Ahmad, I.; Wagner, Frank (1977). “Half-life of the longest-lived einsteinium isotope-252Es”. Journal of Inorganic and Nuclear Chemistry 39 (9): 1509–1511. doi:10.1016/0022-1902(77)80089-4.
- ^ McHarris, William; Stephens, F.; Asaro, F.; Perlman, I. (1966). “Decay Scheme of Einsteinium-254”. Physical Review 144 (3): 1031–1045. Bibcode: 1966PhRv..144.1031M. doi:10.1103/PhysRev.144.1031.
- ^ Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). “The NUBASE2016 evaluation of nuclear properties”. Chinese Physics C 41 (3): 030001. Bibcode: 2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ^ Institut de Radioprotection et de Sûreté Nucléaire, "Evaluation of nuclear criticality safety data and limits for actinides in transport", p. 16.
- ^ Emsley, John (2011). Nature's Building Blocks: An A-Z Guide to the Elements (New ed.). New York, NY: Oxford University Press. ISBN 978-0-19-960563-7
- ^ Gopka, V. F.; Yushchenko, A. V.; Yushchenko, V. A.; Panov, I. V.; Kim, Ch. (2008). “Identification of absorption lines of short half-life actinides in the spectrum of Przybylski's star (HD 101065)”. Kinematics and Physics of Celestial Bodies 24 (2): 89–98. Bibcode: 2008KPCB...24...89G. doi:10.3103/S0884591308020049.
- ^ Seaborg, p. 51
- ^ “High Flux Isotope Reactor”. Oak Ridge National Laboratory. 2010年9月23日閲覧。
- ^ “ru:Радионуклидные источники и препараты” (Russian). Research Institute of Atomic Reactors. 2010年9月26日閲覧。
- ^ a b Haire, p. 1582
- ^ Greenwood, p. 1262
- ^ Porter, C. E.; Riley, F. D., Jr.; Vandergrift, R. D.; Felker, L. K. (1997). “Fermium Purification Using Teva Resin Extraction Chromatography”. Sep. Sci. Technol. 32 (1–4): 83–92. doi:10.1080/01496399708003188.
- ^ Hoffman, Darleane C.; Ghiorso, Albert and Seaborg, Glenn Theodore (2000) The Transuranium People: The Inside Story, Imperial College Press, pp. 190–191, ISBN 978-1-86094-087-3.
- ^ Seaborg, pp. 36–37
- ^ Jones, M.; Schuman, R.; Butler, J.; Cowper, G.; Eastwood, T.; Jackson, H. (1956). “Isotopes of Einsteinium and Fermium Produced by Neutron Irradiation of Plutonium”. Physical Review 102 (1): 203–207. Bibcode: 1956PhRv..102..203J. doi:10.1103/PhysRev.102.203.
- ^ Audi, G.; Kondev, F. G.; Wang, M.; Huang, W. J.; Naimi, S. (2017). “The NUBASE2016 evaluation of nuclear properties”. Chinese Physics C 41 (3): 030001. Bibcode: 2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- ^ Guseva, L.; Filippova, K.; Gerlit, Y.; Druin, V.; Myasoedov, B.; Tarantin, N. (1956). “Experiments on the production of einsteinium and fermium with a cyclotron”. Journal of Nuclear Energy (1954) 3 (4): 341–346. doi:10.1016/0891-3919(56)90064-X.
- ^ Harry H. Binder: Lexikon der chemischen Elemente, S. Hirzel Verlag, Stuttgart 1999, ISBN 3-7776-0736-3, pp. 18–23.
- ^ Эйнштейний (in Russian, a popular article by one of the involved scientists)
- ^ Chetham-Strode, A.; Holm, L. (1956). “New Isotope Einsteinium-248”. Physical Review 104 (5): 1314. Bibcode: 1956PhRv..104.1314C. doi:10.1103/PhysRev.104.1314.
- ^ Harvey, Bernard; Chetham-Strode, Alfred; Ghiorso, Albert; Choppin, Gregory; Thompson, Stanley (1956). “New Isotopes of Einsteinium”. Physical Review 104 (5): 1315–1319. Bibcode: 1956PhRv..104.1315H. doi:10.1103/PhysRev.104.1315.
- ^ Kulyukhin, S.; Auerman, L. N.; Novichenko, V. L.; Mikheev, N. B.; Rumer, I. A.; Kamenskaya, A. N.; Goncharov, L. A.; Smirnov, A. I. (1985). “Production of microgram quantities of einsteinium-253 by the reactor irradiation of californium”. Inorganica Chimica Acta 110: 25–26. doi:10.1016/S0020-1693(00)81347-X.
- ^ a b c Seaborg, p. 40
- ^ These were codenamed: "Anacostia" (5.2 kilotons, 1962), "Kennebec" (<5 kilotons, 1963), "Par" (38 kilotons, 1964), "Barbel" (<20 kilotons, 1964), "Tweed" (<20 kilotons, 1965), "Cyclamen" (13 kilotons, 1966), "Kankakee" (20-200 kilotons, 1966), "Vulcan" (25 kilotons, 1966) and "Hutch" (20-200 kilotons, 1969)
- ^ United States Nuclear Tests July 1945 through September 1992 Archived June 15, 2010, at the Wayback Machine., DOE/NV--209-REV 15, December 2000.
- ^ Seaborg, p. 43
- ^ Seaborg, p. 44
- ^ Seaborg, p. 47
- ^ Haire, p. 1583
- ^ Haire, pp. 1584–1585
- ^ a b Hall, Nina (2000). The new chemistry. Cambridge University Press. pp. 9–11. ISBN 978-0-521-45224-3
- ^ Haire, p. 1588
- ^ Haire, p. 1590
- ^ a b c Haire, R. G.; Eyring, L. (1994). “Lanthanides and Actinides Chemistry”. In K.A. Gscheidner, Jr.. Handbook on the Physics and Chemistry of Rare Earths. 18. North-Holland, New York. pp. 414–505. ISBN 978-0-444-81724-2
- ^ Kleinschmidt, P. (1994). “Thermochemistry of the actinides”. Journal of Alloys and Compounds 213–214: 169–172. doi:10.1016/0925-8388(94)90898-2.
- ^ Fujita, D.; Cunningham, B. B.; Parsons, T. C. (1969). “Crystal structures and lattice parameters of einsteinium trichloride and einsteinium oxychloride”. Inorganic and Nuclear Chemistry Letters 5 (4): 307–313. doi:10.1016/0020-1650(69)80203-5.
- ^ a b Miasoedov, B. F. Analytical chemistry of transplutonium elements, Wiley, 1974 (Original from the University of California), ISBN 0-470-62715-8, p. 99
- ^ Fellows, R.; Peterson, J. R.; Noé, M.; Young, J. P.; Haire, R. G. (1975). “X-ray diffraction and spectroscopic studies of crystalline einsteinium(III) bromide, 253EsBr3”. Inorganic and Nuclear Chemistry Letters 11 (11): 737–742. doi:10.1016/0020-1650(75)80090-0.
- ^ a b c Haire, pp. 1595–1596
- ^ a b c Seaborg, p. 62
- ^ a b c d e Young, J. P.; Haire, R. G.; Peterson, J. R.; Ensor, D. D.; Fellow, R. L. (1981). “Chemical consequences of radioactive decay. 2. Spectrophotometric study of the ingrowth of berkelium-249 and californium-249 into halides of einsteinium-253”. Inorganic Chemistry 20 (11): 3979–3983. doi:10.1021/ic50225a076.
- ^ Haire, p. 1598
- ^ Holleman, p. 1969
- ^ a b c Greenwood, p. 1270
- ^ Young, J. P.; Haire, R. G.; Fellows, R. L.; Peterson, J. R. (1978). “Spectrophotometric studies of transcurium element halides and oxyhalides in the solid state”. Journal of Radioanalytical Chemistry 43 (2): 479–488. doi:10.1007/BF02519508.
- ^ Fujita, D.; Cunningham, B. B.; Parsons, T. C.; Peterson, J. R. (1969). “The solution absorption spectrum of Es3+”. Inorganic and Nuclear Chemistry Letters 5 (4): 245–250. doi:10.1016/0020-1650(69)80192-3.
- ^ a b Peterson, J.R. (1979). “Preparation, characterization, and decay of einsteinium(II) in the solid state”. Le Journal de Physique 40 (4): C4–111. doi:10.1051/jphyscol:1979435. manuscript draft
- ^ Fellows, R.L.; Young, J.P.; Haire, R.G. and Peterson J.R. (1977) in: GJ McCarthy and JJ Rhyne (eds) The Rare Earths in Modern Science and Technology, Plenum Press, New York, pp. 493–499.
- ^ Young, J.P.; Haire R.G., Fellows, R.L.; Noe, M. and Peterson, J.R. (1976) "Spectroscopic and X-Ray Diffraction Studies of the Bromides of Californium-249 and Einsteinium-253", in: W. Müller and R. Lindner (eds.) Plutonium 1975, North Holland, Amsterdam, pp. 227–234.
- ^ Nugent, Leonard J.; Burnett, J. L.; Baybarz, R. D.; Werner, George Knoll; Tanner, S. P.; Tarrant, J. R.; Keller, O. L. (1969). “Intramolecular energy transfer and sensitized luminescence in actinide(III) .beta.-diketone chelates”. The Journal of Physical Chemistry 73 (5): 1540–1549. doi:10.1021/j100725a060.
- ^ Beitz, J.; Wester, D.; Williams, C. (1983). “5f state interaction with inner coordination sphere ligands: Es3+ ion fluorescence in aqueous and organic phases”. Journal of the Less Common Metals 93 (2): 331–338. doi:10.1016/0022-5088(83)90178-9.
- ^ It's Elemental – The Element Einsteinium. Retrieved 2 December 2007.
- ^ Ghiorso, A.; Harvey, B.; Choppin, G.; Thompson, S.; Seaborg, G. (1955). “New Element Mendelevium, Atomic Number 101”. Physical Review 98 (5): 1518–1519. Bibcode: 1955PhRv...98.1518G. doi:10.1103/PhysRev.98.1518. ISBN 978-981-02-1440-1.
- ^ Schadel, M.; Bruchle, W.; Brugger, M.; Gaggeler, H.; Moody, K.; Schardt, D.; Summerer, K.; Hulet, E. et al. (1986). “Heavy isotope production by multinucleon transfer reactions with 254Es”. Journal of the Less Common Metals 122: 411–417. doi:10.1016/0022-5088(86)90435-2.
- ^ Lougheed, R. W.; Landrum, J. H.; Hulet, E. K.; Wild, J. F.; Dougan, R. J.; Dougan, A. D.; Gäggeler, H.; Schädel, M. et al. (1985). “Search for superheavy elements using 48Ca + 254Esg reaction”. Physical Review C 32 (5): 1760–1763. Bibcode: 1985PhRvC..32.1760L. doi:10.1103/PhysRevC.32.1760. PMID 9953034.
- ^ Turkevich, A. L.; Franzgrote, E. J.; Patterson, J. H. (1967). “Chemical Analysis of the Moon at the Surveyor V Landing Site”. Science 158 (3801): 635–637. Bibcode: 1967Sci...158..635T. doi:10.1126/science.158.3801.635. PMID 17732956.
- ^ International Commission on Radiological Protection (1988). Limits for intakes of radionuclides by workers, Part 4. 19. Elsevier Health Sciences. pp. 18–19. ISBN 978-0-08-036886-3
関連文献[編集]
- Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth–Heinemann. ISBN 978-0080379418
- Haire, Richard G. (2006). “Einsteinium”. In Morss, Lester R.; Edelstein, Norman M.; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements. 3 (3rd ed.). Dordrecht, the Netherlands: Springer. pp. 1577–1620. doi:10.1007/1-4020-3598-5_12. ISBN 978-1-4020-3555-5. オリジナルの2010-07-17時点におけるアーカイブ。
- Holleman, Arnold F.; Wiberg, Nils (2007). Textbook of Inorganic Chemistry (102nd ed.). Berlin: de Gruyter. ISBN 978-3-11-017770-1
- Seaborg, G.T., ed (23 January 1978). Proceedings of the Symposium Commemorating the 25th Anniversary of Elements 99 and 100. Report LBL-7701
外部リンク[編集]
- Einsteinium at The Periodic Table of Videos (University of Nottingham)
- Age-related factors in radionuclide metabolism and dosimetry: Proceedings – contains several health related studies of einsteinium
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| |||||||||||||||||||||||||||||||||


![{\displaystyle {\ce {^{238}_{92}U->[{\ce {+6(n,\gamma )}}][-2\ \beta ^{-}]{}_{94}^{244}Pu}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/adc5607f4aa66702f7f8331613b838b19e5fbccc)
![{\displaystyle {\ce {^{238}_{92}U ->[{\ce {+15n}}][6 \beta^-] ^{253}_{98}Cf ->[\beta^-] ^{253}_{99}Es}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/54c4fccdd01ebda8ab75c3aac855a348c6f5ea2c)
![{\displaystyle {\ce {^{252}_{98}Cf ->[{\ce {(n,\gamma)}}] ^{253}_{98}Cf ->[\beta^-][17.81 {\ce {d}}] ^{253}_{99}Es ->[{\ce {(n,\gamma)}}] ^{254}_{99}Es ->[\beta^-] ^{254}_{100}Fm}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/63f13874738d0dfe8637d3dd71bef4ba0cbc6b14)
![{\displaystyle {\ce {^{253}_{99}Es ->[\alpha][20 {\ce {d}}] ^{249}_{97}Bk ->[\beta^-][314 {\ce {d}}] ^{249}_{98}Cf}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/864c693290ca15763e10e38145d86820f7ebe7d3)
![{\displaystyle {\ce {^{249}_{98}Cf + ^{2}_{1}D -> ^{248}_{99}Es + 3^{1}_{0}n}}\quad \left({\ce {^{248}_{99}Es ->[\epsilon][27 {\ce {min}}] ^{248}_{98}Cf}}\right)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/b42bfcc37be3fe9bc6251a1bb1dd647e564b664b)
![{\displaystyle {\ce {^{249}_{97}Bk ->[+\alpha] ^{249,250,251,252}_{99}Es}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/46af865ac0b1463965f1790285f36a01d24eb318)
![{\displaystyle {\ce {^{252}_{98}Cf ->[{\ce {(n,\gamma)}}] ^{253}_{98}Cf ->[\beta^-][17.81 {\ce {d}}] ^{253}_{99}Es}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/45d75d0f0badaf920ba511372718f8dc284b9587)
