マクロライド系抗菌薬
マクロライド系抗菌薬(マクロライドけいこうきんやく)とは、マクロライドの定義に従った構造を有した、抗菌薬として用いられる薬物群の総称である。
マクロライド系抗菌薬の作用点は細菌のリボソームであるため、細胞壁を持たない細菌に対しても効果を発揮する。殊にリケッチア、クラミジアなどの細胞内寄生菌や、マイコプラズマの感染症に対しては、第1選択薬として用いられる。抗菌薬の中では比較的有害作用が少なく、また比較的多くの細菌に有効であるため、小児から老人まで広く処方されてきた頻用薬の1つだが、その汎用性が一因でマクロライド系抗菌薬に耐性を示す細菌が増加しており、医療上の問題になっている。また、他にも薬物を併用している際には、薬物相互作用が問題となる場合もある。
マクロライドの構造上の定義[編集]
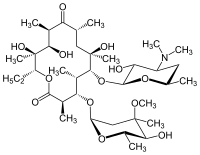
マクロライド(macrolide)とは、アグリコンとして大員環のラクトンをもつ配糖体を指す[1]。そのため、波数1720〜1730 cm−1付近の赤外線領域にラクトンに起因する特徴的な吸光帯を有する。
なお、このラクトン環は、12、14、15、ないし16員環であり得る[注釈 1]。また、一口に糖とは言っても、ヒドロキシ基が外れたデオキシ糖が多く見られ、他にもアミノ糖やメチル化糖であったりと、様々な糖がラクトン環に結合している[注釈 2]。さらに、結合している糖の数も1つ以上であって、何個の糖が結合しているのかは決まっていない。その上、糖がラクトン環のどの位置に結合しているのかも決まっておらず、複数の糖が連なっている場合もある。
歴史[編集]
最初に実用化されたマクロライド系抗菌薬はエリスロマイシンである。イーライリリー社のマクガイア(J. M. McGuire)らによって、フィリピンの土壌中から分離された放線菌の1種、Saccharopolyspora erythraea(旧名Streptomyces erythraeus)から分離された。すなわち、最初のマクロライド系抗菌薬は抗生物質であった[注釈 3]。1952年にはアメリカ合衆国で、エリスロマイシン産生菌を採取したイロイロ州の「Ilo」を冠して、Ilosoneという商品名で発売された。
これ以降、その他のマクロライド系抗菌薬を産生する細菌の発見および、それを化学修飾することによる半合成抗菌薬の開発などによって、マクロライド系抗菌薬に分類される化合物群は増えていった。
比較的副作用が少なく、広範な菌種に作用する抗菌薬として、マクロライド系抗菌薬は感染症治療に頻用されていった。さらに、畜産業においては家畜に抗菌薬を投与することにより肥育効率が向上するとされ、例えばスピラマイシンなども、家畜の肥育目的で使用されてきた[2]。これらの結果、マクロライド系抗菌薬に耐性を有した細菌が数多く報告されてきた。加えて交差耐性と呼ばれる、細菌がある1つのマクロライド系抗菌薬に耐性を獲得すると同時に、他の抗菌薬にも耐性を獲得する例も知られてきた。マクロライド系抗菌薬に対する耐性の獲得と同時に、その他のマクロライド系抗菌薬ばかりか、構造が全く異なるリンコサマイド系抗菌薬(リンコマイシン系抗菌薬)のリンコマイシンやクリンダマイシンに対する耐性も獲得されるという例も多く知られる[3]。また、耐性により効果が失われるだけでなく、菌交代現象によりかえって悪影響をおよぼすケースも知られてきた。
マクロライド系抗菌薬を含め、抗菌薬の不適切な使用による耐性菌出現の誘発などの問題は、21世紀初頭においても依然未解決の問題である。
産生菌による生合成経路・精製法・人工的な化学修飾[編集]
この節の加筆が望まれています。 |
薬理作用[編集]
マクロライド系抗菌薬の活性は、化学構造上のマクロライド環に由来する。その大きさからグラム陰性菌が有する外膜を通過しづらく、グラム陽性菌と比してグラム陰性菌には効き難い傾向が見られる[4]。
作用機序[編集]
14員環から16員環のマクロライド系抗菌薬の作用機序は、真正細菌が有する70Sリボゾームのサブユニットの1つ、50Sサブユニットを構成する23S rRNAに親和性を有する事が関係している[1]。23S rRNAはリボザイムとしてペプチジルトランスファーゼ反応[注釈 4]を触媒するが[5]、ここにマクロライド系抗菌薬の分子が干渉することにより、ペプチジルトランスファーゼ反応が阻害され、一時的にタンパク質合成が妨げられる[1]。こうして、マクロライド系抗菌薬は基本的に静菌的に作用する[1]。すなわち、マクロライド系抗菌薬は細菌の増殖速度を低下させ、細菌に感染されてしまった側の真核生物が有する免疫系による細菌の排除速度の方が高くなることで感染が終息する。
なお、真核生物ドメインのリボゾームは、真正細菌ドメインのリボゾームとは構造が異なるため、ヒトを含め真核生物のタンパク質合成は阻害されない[注釈 5]。この結果、マクロライド系抗菌薬を真核生物に投与しても、選択毒性を発揮し、抗菌薬として使用できる。
ところで、抗菌薬を実際に感染症の治療に用いる場合には、その作用が「時間依存性か、濃度依存性か」が本質的に重要である。マクロライド系抗菌薬は、基本的に時間依存性の薬物と考えられている。つまり、最小発育阻止濃度よりも高い濃度を、長い時間にわたって保てば保つほど効果を発揮する。一方で、マクロライド系抗菌薬は基本的に静菌的に作用するため、最小発育阻止濃度以上に濃度を上げても効果が増すことはない一方、被投与者への悪影響が出易くなる。
逆に、最小発育阻止濃度を下回れば細菌の増殖は防げず、被投与者に全く悪影響が出ないとは言い切れないうえ、耐性菌出現の問題もある。よって、適切な用量を、適切な間隔で、適切な期間、使用しなければならない。
薬物動態[編集]
一般的にマクロライド系抗菌薬はヒトでの代謝や排泄が比較的速く、例えば、エリスロマイシンなどを経口投与で使用する場合には、頻回投与しなければ充分な効果を発揮しない。この欠点を補うため、一部のマクロライド系抗菌薬には徐放製剤も実用化された[注釈 6]。
なお、ケトライドはヒトでの代謝や排泄は比較的遅く、テリスロマイシンの半減期が約10時間程度である。さらに、アザライドはヒトでの代謝や排泄が遅く、アジスロマイシンの半減期は60時間を超える。
また、マクロライド系抗菌薬は真核細胞内への浸透性が高いため、細胞内部に寄生する病原体に対しても有効である。
適応菌種[編集]
マクロライド系抗菌薬は、例えばペニシリンに比べて幅広い抗菌スペクトラムを持ち、呼吸器や軟部組織などの多くの細菌感染症に対して適応されてきた。例として、連鎖球菌、肺炎球菌、ブドウ球菌、そして腸球菌といった、グラム陽性菌による感染症が挙げられる[注釈 7]。
ただし、マクロライド系抗菌薬に対して、かなり耐性化が進んでいる菌種も見られる。さらに効果の面で考えても、殺菌的に作用するペニシリンやセファロスポリンなどの使用が優先される菌種もあり、それらに対してはペニシリンアレルギーなどの場合に代替的に処方されることがある。
一方で、マクロライド系抗菌薬にも「得意な」細菌が存在する。例えば、リケッチアやクラミジアといった細胞内寄生菌に対しては、マクロライド系抗菌薬が真核生物の細胞内に入り込み易いために、比較的効果を発揮し易い[注釈 8]。また、マクロライド系抗菌薬の作用点が細胞壁ではないため、細胞壁を有さないマイコプラズマにも、効果を発揮する。加えて、細菌が細胞壁の材料として用いているペプチドグリカンへの依存が低い細胞壁を有した抗酸菌、殊に非定型抗酸菌に対しても、マクロライド系抗菌薬は効果を発揮する。
なお、ウイルスや真菌には無効であり、原則としてマクロライドを含む抗菌薬は処方されない。
その他の適応[編集]
抗菌作用を狙う以外に、14員環マクロライド系抗菌薬のエリスロマイシンやクラリスロマイシンは、びまん性汎細気管支炎(DPB)に対して特効的な治療効果を有すると明らかされた。
問題点[編集]
副作用[編集]
マクロライド系抗菌薬が引き起こす副作用は、頻度も多くはなく、比較的安全な薬物とされる。元来は、真核生物の細胞に入り込み易いために、アレルギーも誘発し易かったマクロライド系抗菌薬だが、そのような薬物は、実用化前に排除されてきた結果である。それでも、医薬品一般の問題として、予測の難しいアレルギーが発生しうるという点については、心に留めておく必要がある。
マクロライド系抗菌薬の主な副作用としては、下痢、悪心(吐き気)、嘔吐などの消化器症状が挙げられる。最初に実用化されたマクロライド系抗菌薬であるエリスロマイシンでは、特に消化器症状が出る副作用の頻度が高い。この消化器症状は、マクロライド系抗菌薬が胃酸によって分解された際に生じる、ヘミケタルと言う物質が、消化管の蠕動運動を亢進するため発生するとされる。これが発生する理由は、消化管ホルモンの1つであるモティリンの代わりに作用し、すなわち、モティリン受容体を刺激して、結果として胃の運動を促進すると判明した[6]。そこで、この副作用を軽減するには、トリメブチンを併用すると効果を示す場合もある。なお、消化器症状については、胃酸によって分解されないように、腸溶性コーティングを施すといった製剤の工夫で軽減される。また、クラリスロマイシンなどのように、化学修飾をして胃酸で分解され難いようしたマクロライド系抗菌薬では、改善された。
また、稀ではあるものの、マクロライド系抗菌薬には代表的な副作用として、心臓に異常を来たす事が挙げられる。この結果は、心電図におけるQT時間の延長として観察される。特に、併用薬や基礎疾患が存在する場合には、死亡の可能性が有る。
薬物相互作用[編集]
多くのマクロライド系抗菌薬はCYP3A4で代謝される上に、代謝物のニトロソアルカン化合物がCYP3A4の活性中心であるヘム鉄に共有結合するとされる。この結果、CYP3A4の作用を阻害する。そのため、マクロライド系抗菌薬自体の副作用よりも、同じCYP3A4で代謝される 他の複数の薬物との薬物相互作用の問題が出る場合が有る。15員環や16員環と比べて、特に14員環のマクロライド系抗菌薬では、CYP3A4の阻害作用が強く出る傾向にある[7]。CYP3A4が阻害された事によって問題を起こす薬物は数多い。そもそもスボレキサントのように、CYP3A4に対する強い阻害作用を有した薬物との併用が禁忌と定められている薬物も存在する。また例えば、気管支喘息の治療薬として知られるテオフィリンは、有効血中濃度と中毒域が近く、CYP3A4が阻害された事でテオフィリンの代謝が阻害されて血中濃度上昇し、テオフィリンの中毒に陥る危険が有る。さらに、カルシウム拮抗薬に於いても血中濃度が上昇し、危険なレベルの低血圧性ショックを引き起こす可能性が有るとの報告が存在する[8] [9]。
また、QT時間延長の副作用もある。したがって、QT時間延長作用のある別の薬剤と併用すると、この副作用が増悪し、場合によっては致死的な不整脈を引き起こす。この種の薬物の代表は第2世代抗ヒスタミン薬のテルフェナジンであり、この薬物は代謝拮抗作用も併せ持つため、併用は禁忌である。
細菌による耐性の獲得[編集]
マクロライド系抗菌薬に対する薬剤耐性獲得は比較的起こり易く、臨床上の重大な問題になっている。細菌の耐性化には以下のような機序が考えられている。
- リボゾームの、マクロライド系抗菌薬が結合する部位が変異により構造変化する。
- マクロライド系抗菌薬の透過性を低下させる。
- マクロライド系抗菌薬を細胞外に排出する仕組みを獲得する。
- マクロライド系抗菌薬のラクトン部位を分解して不活化する酵素の産生能を獲得する。
一度獲得された耐性はプラスミドを介し細菌から細菌へと伝達されることが問題を深刻にする。さらに、1種類のマクロライド系抗菌薬に耐性を獲得する際、他のマクロライド系抗菌薬や、他の系統の抗菌薬にも同時に耐性を獲得する、交差耐性と呼ばれる現象もある。
かつてマクロライド系抗菌薬は市中肺炎に対して有効であったものの、2007年現在、市中肺炎の起因菌の8割がマクロライド系抗菌薬に耐性を持つに至っている。このような状態でマクロライド系抗菌薬を使用すれば、かえって症状を悪化させることもある。そのため、マクロライド系抗菌薬を使える菌種は、マイコプラズマ、クラミジア、非定型抗酸菌、ヘリコバクターピロリ、カンピロバクターなど少なくなった。
菌交代現象[編集]
これはマクロライド系抗菌薬に限らず、抗菌薬全般に言える話だが、抗菌薬を使用すると、その抗菌薬が効く微生物が死ぬ一方で、その抗菌薬が効かない微生物が、増殖可能な場所と栄養分を独占して一気に増殖する場合がある。この現象は耐性菌だけでなく、そもそもマクロライド系抗菌薬が効き難い緑膿菌などの細菌や、細菌ではない真菌などでも起こる。
薬剤費・苦味の問題[編集]
マクロライド系抗菌薬の実地臨床上の重要な弱点は、耐性の問題の以外に、抗菌薬の中では比較的高価である事が挙げられる。マクロライド系抗菌薬は化学構造が複雑なため人工合成が難しく、微生物に抗菌薬を生合成させてから分離精製する手間が必要があったり、特性を改善するため分離精製後に化学修飾を行う必要がある事が関係している。
また一般に軽視されがちな「マクロライド系抗菌薬は一般に苦味が強い」という点も、乳幼児に経口投与する際には重大な問題になる。抗菌薬は不規則な服薬をすると耐性菌の発生を助長する可能性が高く、また苦味によって患者が投与をためらうと不規則な服薬に繋がる。このため、医師や薬剤師は服薬コンプライアンスの維持に注意を払い、また味が良くないせいで患者が薬を飲まなくなることを避けるために製剤を工夫してきた。例えば、裸錠ではなくフィルムコーティングを錠剤に施すことで、噛み砕いたり、口の中で溶かしたりしなければ苦味はほとんど問題にならなくなる。カプセル剤として製剤しても同様である。ただ、散剤などの剤形ではどうしても苦味が感知されやすい。そこで、散剤でも甘味のコーティングを工夫したり、苦味を抑える添加物を加えるといった改良が行われてきており、以前よりも苦味に対する問題は少なくなりつつある。一方で、この製剤の工夫により薬剤費がさらに高くなる。14員環マクロライド系抗菌薬に比べて16員環マクロライド系抗菌薬は苦味が少ないため、この点では有利である。
なお経口服用が出来ない場合、注射薬や他の抗菌薬への変更を考慮する場合もある。
種類[編集]
代表的なマクロライド系抗菌薬を以下に示す。なおカッコ内は略称を記載した。
- 14員環
- 15員環
- アジスロマイシン(AZM) - マクロライド系抗菌薬だがラクトン環に窒素を含むため「アザライド」として分類する場合もある。薬物動態も異なり、半減期が長い。
- 16員環
- その他のマクロライド系抗菌薬
- ケトライド系抗菌薬
- 抗細菌薬以外でマクロライドの構造を有する薬物
使用例[編集]
- 市中肺炎
- 近年では、起炎菌である肺炎球菌がペニシリン耐性肺炎球菌(PRSP)である場合が多いため、第3世代セフェムを単独で用いる他にも、マクロライド系薬剤 + βラクタム薬を用いる場合もある。
- 非定型肺炎(異型肺炎)
- マイコプラズマ肺炎やクラミドフィラ・ニューモニエ肺炎などでは、マクロライド系・テトラサイクリン系・ニューキノロン系抗菌薬が用いられる場合が多い。
- 百日咳
- 急性の百日咳では、マクロライド系抗菌薬が用いられる場合が多い。
- 性行為感染症
- クラミジア感染・淋菌感染や、骨盤内炎症性疾患でのクラミジア重感染を疑い、アジスロマイシン1000 mgを1日1回投与などが行われる場合がある。
- ネコ引っかき病
- ほとんどは重篤化せず軽度の腫れでは治療の必要は無い。抗菌薬が使われる場合には、マクロライド系・テトラサイクリン系・ニューキノロン系抗菌薬が第1選択とされる。ただし、クラリスロマイシンは有効でないとする報告も存在する。
- 非定型抗酸菌
- クラリスロマイシンは非定型抗酸菌の治療にエタンブトールと併用する場合がある。
- ヘリコバクター・ピロリ除去
- 胃に持続感染するヘリコバクター・ピロリの除去のためには、幾通りかの薬物の組み合わせが用いられる。例えば、プロトンポンプ阻害薬+アモキシシリン+クラリスロマイシンの併用、ボノプラザン+アモキシシリン+クラリスロマイシンの併用、プロトンポンプ阻害薬+アモキシシリン+メトロニダゾールの併用、ボノプラザン+アモキシシリン+メトロニダゾールの併用である。
脚注[編集]
注釈[編集]
- ^ ただし、15員環のアジスロマイシンは、14員環に窒素を人工的に導入して開発された経緯からアザライド(azalide)に分類する場合もある。
- ^ 通常はクラジノースかデソサミンが結合している。
- ^ 抗生物質と抗菌薬は、厳密には異なる。抗生物質とは、人工合成の化合物ではなく、微生物が産生する天然物であり、他の微生物の発育を妨げる化合物群である。参考までに、抗生物質に当たる化合物群を、医薬品の分類で見ると、抗菌薬、抗真菌薬、抗ガン剤などに跨る。これに対して、抗菌薬とは、天然物・半合成・人工合成に関わらず、細菌に対して毒性を有しており、細菌の活動を抑えたり、細菌を殺す化合物群である。したがって、それぞれの化合物群の集合は、必要条件も充分条件も満たさず、イコールで結べない。
- ^ リボソームでタンパク質を合成するためにアミノ酸を運んできたtRNAが、リボソーム上で合成されつつあるタンパク質と一時的に結合した、ペプチジルtRNAが合成される反応
- ^ ただし、古細菌ドメインのリボソームも阻害されないため、古細菌には無効である。他に、真核生物である、真菌のリボソームも阻害されないため、真菌にも無効である。また、そもそも感染した生物の細胞が有するリボソームを乗っ取って利用するウィルスなどにも無効である。
- ^ 徐放製剤とは、消化管内で薬物を時間をかけて錠剤などから溶出させる方法で、その薬物が長時間にわたって消化管内へと供給されるようにデザインされた製剤である。このため、その薬物が腸管の広い範囲で吸収可能な薬物であった場合には、次々と体内へと吸収されて、体内への薬物の供給が続く。これにより、先に体内へと吸収された薬物が、代謝によって失活したり、排泄によって消失したりしても、新たに薬物が吸収されてくるので、結果として、長時間にわたって薬物が作用する。マクロライド系抗菌薬の徐放製剤の例として、日本では認可されていないものの、クラリスロマイシンに、そのような製剤が開発された。
- ^ グラム陽性菌とは、細菌に対してグラム染色を行った際に、染まる細菌を指す。対義語はグラム陰性菌である。
- ^ 真核生物の細胞内に入り込み易いという、マクロライド系抗菌薬と同様な長所を持つテトラサイクリンは、カルシウムとの複合体を形成し易い。このため、特に成長期にテトラサイクリンを投与すると、骨や歯の形成に対する悪影響を与える。また、歯の形成中にテトラサイクリンを投与すると、歯牙黄染と呼ばれる特徴的な副作用も出る。このため、テトラサイクリンは、殊に妊婦や乳幼児に対しては、可能な限り使用しない事が求められる。
- ^ キタサマイシンは、ロイコマイシン類混合物なので、このように「LM」の略称が使用される。ただし、キタサマイシンは全てのロイコマイシン類を含有しているわけではない。
出典[編集]
- ^ a b c d 微生物薬品化学 2003, p. 215.
- ^ 微生物薬品化学 2003, p. 141.
- ^ 微生物薬品化学 2003, p. 177,222.
- ^ 微生物薬品化学 2003, p. 179.
- ^ 微生物薬品化学 2003, p. 51.
- ^ 重信 弘毅・石井 邦雄(編集)『パートナー薬理学』 p.310 南江堂 2007年4月15日発行 ISBN 978-4-524-40223-6
- ^ 微生物薬品化学 2003, p. 188.
- ^ 一部の抗生物質とカルシウム拮抗薬の併用は低血圧をもたらす いきいき健康 NIKKEI NET:閲覧 2011.2.21
- ^ Those taking calcium channel blockers showed raised risk for dangerously low blood pressure Canadian Medical Association Journal(CMAJ)
- ^ Methymycin (CID:5282034)
- ^ Neomethymycin (CID:5282033)
参考文献[編集]
- 上野 芳夫・大村 智 監修、田中 晴雄・土屋 友房 編集『微生物薬品化学』(改訂第4版)南江堂、2003年4月15日。ISBN 4-524-40179-2。
- マクロライド系抗菌薬 MSDマニュアル家庭版
- 砂塚敏明、マクロライド系薬の新作用と創薬 日本化学療法学会雑誌 2004年 52巻 7号 p.367-370, doi:10.11250/chemotherapy1995.52.367
