ラクトン
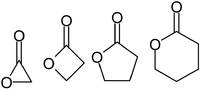
α-アセトラクトン
β-プロピオラクトン
γ-ブチロラクトン
δ-バレロラクトン



ラクトン (lactone) は、環状エステルのことで[1]、同分子内のヒドロキシ基(-OH)とカルボキシ基(-COOH)が脱水縮合することにより生成する。炭素原子が2個以上、酸素原子が1個からなる複素環式化合物で、環を形成する酸素原子に隣接した炭素原子にカルボニル基(=O)が置換した構造をとる。
存在[編集]
5–6員環のラクトン構造はテルペン類などの天然物に多く存在し、香気成分やフェロモンなどによく見られる。例えば麝香臭を持つ香料として著名なエキサルトリド (exaltolide) は16員環のラクトンである。
- 例
- ε-カプロラクトン
- γ-ノナラクトン - モモ、アンズなど
- ウイスキーラクトン
- γ-デカラクトン
- γ-ウンデカラクトン - モモなど
- シクロペンタデカノリド
- シクロヘキサデカノリド
- アンブレットリド
- エチレンブラシレート (Musk T)
- グルコノラクトン - 蜂蜜など
- クマリン - サクラの葉
- ワインラクトン
- カヴァラクトン
- セスキテルペンラクトン
- エラグ酸 - イチゴ、ラズベリー、クランベリー、ブドウなど
命名[編集]
ラクトンは一般に、前駆体となるカルボン酸分子の名称(アセト- = 2炭素、プロピオ- = 3、ブチロ- = 4、バレロ- = 5、カプロ = 6、…)の末尾に-ラクトン(-lactone)をつけ、複素環を構成する炭素数をギリシア文字で表し、それを前に置いて命名する。前に置くギリシア文字は、三員環のものはα-、四員環のものはβ-、五員環のものはγ-のようになる。
その他、ラクトンであることを表す末尾には -オリド、-オライド (-olide) がある。例えば、ブテノライド、マクロライド、カルデノライドおよびブファジエノライドなどがある。
12員環以上の大環状ラクトンをマクロライドと総称する。抗菌作用や抗腫瘍作用など強い生理活性を示すものが多く、抗生物質 エリスロマイシン、抗真菌剤 アムホテリシン、免疫抑制剤 タクロリムスなどが医薬として実用に供されている。
合成[編集]
合成法は主に、ヒドロキシ基とカルボキシル基を持つ分子(ヒドロキシカルボン酸)の分子内脱水縮合による。環化を起こしやすい5,6員環ラクトンの形成は容易で、相当するヒドロキシカルボン酸あるいはそのエステルを酸触媒で反応させるだけでラクトンが得られることが多い。7員環以上の中・大員環ラクトンは高度希釈法を用いるなど合成に工夫を要し、山口ラクトン化反応や椎名ラクトン化反応、およびオレフィンメタセシスによる方法が近年多く用いられている。
反応[編集]
水酸化ナトリウム水溶液などで加水分解すると、脱水縮合前のヒドロキシカルボン酸に戻る。反応性や機構はラクトンの環の大きさにより変わる。5員環以上のラクトンの加水分解は、カルボニル炭素への OH−イオンの付加から始まる付加脱離機構で、立体的なひずみを持つ 4員環ラクトンでは、OH−イオンが4位の炭素を攻撃する SN2機構で進行する。
若い女性特有体臭成分と加齢による減少[編集]
ロート製薬の研究によると、γ-デカラクトン(ラクトンC10)とγ-ウンデカラクトン(ラクトンC11)はともに若い女性特有の体臭を構成している。γ-デカラクトンは20代から急激に、γ-ウンデカラクトンは30代から大幅に減少することが明らかになった。若い女性の体臭にのみ含まれ、若い女性特有の良い匂いの原因となる。濃度は10代後半をピークに減少する。含有の香料をつけることで加齢後も嗅覚で女性らしさや若々しい印象を向上させる[2][3]。
出典[編集]
- ^ March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure Michael B. Smith, Jerry March Wiley-Interscience, 5th edition, 2001, ISBN 0-471-58589-0
- ^ “ロート製薬の「DEOCO」が男性に「バカ売れ」女子の匂い?”. ライブドアニュース. 2019年5月30日閲覧。
- ^ “若い女性特有の「いい匂い」は10代後半がピーク 維持する方法”. yomiDr. / ヨミドクター(読売新聞). 2019年5月30日閲覧。
