ヨウ素131
| ヨウ素131 | |
|---|---|
| 概要 | |
| 名称、記号 | ヨウ素131,放射性ヨウ素,131I |
| 中性子 | 78 |
| 陽子 | 53 |
| 核種情報 | |
| 半減期 |
8.0197日 物理的半減期:8.04日 生物学的半減期 120-138日(非結合ヨウ素) 生体内での実効半減期 7.6日 (非結合ヨウ素) |
| 同位体質量 | 130.9061246(12) u |
| 余剰エネルギー | 971 keV |
ヨウ素131(英: iodine-131, 131
53I)は、ヨウ素の放射性同位体のうちの一つで、質量数が131のものを指す。半減期は約8日である。主に医療や製薬の用途がある。また、核分裂生成物のうち放射能汚染の原因となる主要三核種のひとつである。
概要[編集]
主に医療や製薬の用途がある。また、核分裂生成物のうち放射能汚染の原因となる主要な存在[1] として、1950年代の野外核実験やチェルノブイリ原子力発電所事故だけでなく、今日の日本の原子力事故に至るまで健康に多大な影響をもたらす存在として認知されている。主要なウラン、プルトニウム、間接的にトリウムのそれぞれの核分裂生成物でもあるため、全ての核分裂生成物の合計重量の3 %近くを占める。
ベータ崩壊による作用として、透過する細胞と最高数ミリメートル離れて突然変異および細胞死を引き起こす。このため、高線量の放射線は時に低線量のものよりも危険性が少ない。それゆえ甲状腺の組織を破壊する傾向があり、結果としてがんの原因となる。例として、甲状腺腫の治療に中程度の線量のヨウ素131を用いられた小児には甲状腺癌の増大が見られたが、はるかに高線量で治療を受けた小児はそうならなかった。同様にバセドウ病の治療に非常に高線量のヨウ素131を用いる多くの研究では、中程度の線量のヨウ素131吸収で甲状腺癌のリスクが直線的に増加するにもかかわらず、甲状腺癌の増加は見られない[2]。したがって、小さい線量のヨウ素131は医療用として、特に小児にはますます用いられなくなり、目的の組織を破壊する方法としてますます最大限量でのみ用いられる。これは「治療上の用法」として知られている。
エネルギーと放射線量の約10 %がガンマ線を介しているので、それが治療に用いられるとシンチグラフィのイメージング(画像化)技術(すなわちガンマカメラ)で「見る」ことができる。しかし、他の90 %の放射線(ベータ線)は組織の損傷を引き起こすだけで、見たり画像化には寄与することはないため、核イメージングのみが必要な場合は他の害の少ないヨウ素の放射性同位体が好まれる。それでも、ヨウ素131は他のヨウ素の放射性同位体に比べて低費用のため、時折純粋に画像診断に使用されている。医療用の画像処理に用いられた非常に少ない線量のヨウ素131によって、甲状腺癌の増加は示されていない。ヨウ素131のコストの低さという有用性は、原子炉内でテルルに対する中性子照射によりヨウ素131を作成し、様々な単純な方法(すなわち揮発性の同位体を加熱して飛散させる)でヨウ素131を分離させる相対的な容易さによる。これとは対照的に、他のヨウ素の放射性同位体は通常加圧キセノンガスの高価なカプセルの原子炉照射から始まる遥かに高価な技術によって作成される。
生成[編集]
ヨウ素131のほとんどは自然テルル目標の中性子照射をした原子炉から生成される。最も軽いテルルの同位体からより重い安定同位体や他の安定ヨウ素やキセノンになるため、自然テルルの照射はほぼ完全に、数時間以上の半減期を持つ放射性同位体のみのヨウ素131を生成する。しかし、自然発生した最も重い天然テルルの核種、テルル130(天然テルルの34 %)は中性子を吸着させてテルル131になり、それは25分間の半減期を通してベータ崩壊によりヨウ素131となる。
テルル化合物はイオン交換カラムに酸化物として拘束されている状態で照射することができ、ヨウ素131を放出した後アルカリ溶液に溶出する[3]。通例として、粉末状のテルル元素を照射した後、はるかに低い蒸気圧を持っているヨウ素の乾燥蒸留によりヨウ素131を分離させる。成分は、標準的な方法で弱アルカリ性溶液に溶解し、ヨウ素131と次亜ヨウ素酸エステル(すぐにヨウ化物に還元される)を生成する[4]。
ヨウ素131は、ウラン235が核分裂する際に 2.878 % の確率で核分裂生成物として生成される。[5]自然界に存在するウラン235は極めてわずかの確率(2.0x10−9)で自発核分裂を起こし、ヨウ素131を生成するが、それとて8日の半減期で急速に減少するので、自発核分裂由来のヨウ素131は検出限界を下回る量しか存在しえない。核燃料中であれ、放射能汚染の現場であれ、自然界であれ、いかなる場所にであれ存在し、検出されたヨウ素131は、その時点から長くとも数ヶ月以内の時点で、原子炉や核実験などで人工的に生成されたものであるとみなせる。
なお、半減期が15.7×106年と比較的長いヨウ素129は、自発核分裂由来のものが自然界で検出されることがある。
放射性崩壊[編集]
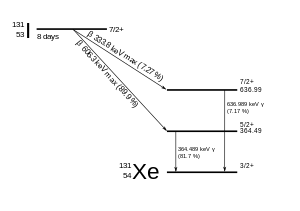
安定同位体のヨウ素127に含まれる中性子数は74であるが、放射性同位体のヨウ素131は78個の中性子を含む。ヨウ素131の半減期は 8.02 日で、大部分(89 %)がベータ崩壊およびガンマ崩壊が起こり、キセノン131(安定同位体)へと推移する。第一段階はベータ崩壊によって励起状態のキセノン131に変化し、これが直ちにガンマ崩壊を起こして安定状態のキセノン131となる。このときに放出されるエネルギーの総量は 971 keV である。
+ 606 keV
+ 364 keV
第一段階で生じる崩壊エネルギーは 248 - 807 keV と幅広いが、最多は 606 keV である(崩壊比 89 %)。[6] ベータ崩壊に伴って同時に生じる反ニュートリノがエネルギーを運び去るため、この場合のベータ線の平均エネルギーは 190 keV となる。[7]
ベータ線は高いエネルギーを持つため、人体へ照射されると 0.6 – 2mm 体内へ進入する。[8]
人体への影響[編集]
食品中のヨウ素はほとんどが甲状腺に蓄積される。これは甲状腺が機能維持のためにヨウ素を必要とするためである。ヨウ素131が放射性降下物として環境中に高濃度で存在する場合、摂取する食品を経由して甲状腺に蓄積される可能性が高まり、これが崩壊することで甲状腺にダメージを与える。高濃度のヨウ素131を取り込んだ場合の危険性は、主に放射線がもたらす遅発性の甲状腺癌であるが、良性腫瘍や甲状腺肥大の可能性も指摘されている[9]。
甲状腺癌のリスクはヨウ素剤の服用で低減できる。これは体内のヨウ素濃度を上げることで放射性ヨウ素の吸収と蓄積が相対的に下がるからである。チェルノブイリ原子力発電所事故の際にはポーランドで児童にヨウ素剤が配布された反面、チェルノブイリ周辺では配布されず、被害の拡大につながった。[10]
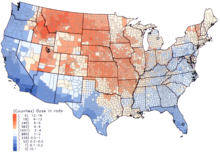
米国内では、1950年代から1960年代初頭の児童にヨウ素131の蓄積が顕著に見られるが、これはその期間に実施された地上核実験の結果、放射能汚染された牧草を食べた牛からの牛乳の摂取によるものである。[11] アメリカ国立癌研究所により、放射性降下物として直接人体に作用したヨウ素131の影響も公表されているが、これは米国内の3070の行政区域で行われた、1971年以前に生まれた人への個別調査と、[12] ネバダ核実験場からの降下物のデータの総計から算出されたものである。[13]
治療と予防[編集]
ヨウ素131の体内への取り込みを防ぐには、安定同位体のヨウ素127をヨウ化塩の形で体内で飽和させる。通常はヨウ化カリウムが用いられる。純粋なヨウ素はこの目的で用いてはならない。単体のヨウ素は強い酸化作用を示すため、飽和に必要な量を摂取すると人体にとって有毒だからである。安定同位体のヨウ素で人体によるヨウ素吸収を飽和すれば、後からやってきたヨウ素131の吸収はほとんど行われず、放射線障害を低減できる。予防には成人には一日あたり 130 mg のヨウ化カリウムが一回または 65 mg ずつ二回に分けて投与される。ヨウ化カリウム 130 mg 中にはヨウ素が 100 mg 含まれるが、これは一日の必須量である 0.15 mg の 700倍に相当する。
医学・薬学的使用[編集]
ヨウ素131は治療(放射線療法)として核医学で用いられ、そして用いられた場合は診断用スキャナで可視化できる。ヨウ素131をヨウ化塩として用いるのには、甲状腺の正常な細胞のヨウ素吸収のメカニズムを利用している。放射線治療での使用の例は、組織がヨウ素を吸収してしまい組織の破壊が望ましい場合である。
ヨウ素131の主要な用途は、甲状腺中毒症(甲状腺機能亢進症)と、ヨウ素を吸収する一部の甲状腺癌の治療が挙げられる。従ってヨウ素131は、直接の放射性同位体療法として、バセドウ病による甲状腺機能亢進症と、時に活動過多の甲状腺結節(悪性でない異常活性の甲状腺組織)を治療するために用いられる。バセドウ病由来である甲状腺機能亢進症を治療するための放射性ヨウ素の治療上における使用は、1941年にSaul Hertz(英語版)によって最初に報告された。
治療目的で意図的にヨウ素131を投与する際には、数億 - 数十億ベクレルを投与する。これによって甲状腺に照射される放射線量は、数十シーベルト(ミリもマイクロもつかないことに留意)にもなる。
ヨウ素131同位体はまた、例えば褐色細胞腫や神経芽細胞腫の画像診断と治療のためのヨウ素131-メタヨードベンジルグアニジン(ヨウ素131-MIBG、131I-MIBG、[I-131]MIBG。2021年1月28日、「MIBGシンチグラフィ陽性の褐色細胞腫・パラガングリオーマ」の適応で承認申請された[14])のような、治療に使用することができる特定の放射性医薬品に対して、放射性の標識として使用することができる。これら全ての治療上の使用において、ヨウ素131は狭い範囲へのベータ線放射により細胞組織を破壊する。細胞組織に対する放射線損傷のおよそ90 %はベータ線により、残余はガンマ線による(放射性同位体から、より長い距離まで到達する)。ヨウ素131はガンマ放出体でもあるため、治療での使用後、診断用スキャナで可視化できる。
甲状腺における少量のベータ放射線による発ガン性のため、ヨウ素131は主として(あるいは純粋に)診断の用途に使用されることは滅多にない。とはいえ、過去にはその生産の容易さと低価格のためにこれはより一般的ではあった。その代わりに、より純粋にガンマ線を放射する放射性ヨウ素であるヨウ素123が、診断上の検査(甲状腺の核医学走査)では使用される。ヨウ素125もまた、診断により長い半減期を持つ放射性ヨウ素が必要な場合や、近接照射療法治療(同位体は小さな種子のような形体の金属カプセルに封じられる)で時折使用される(ベータ線の混じらない低エネルギーのガンマ線を放射するヨウ素125が有用であるので)。ヨウ素のその他の放射性同位体は、近接照射療法では決して使用されない。
日常的に輸送される下水汚泥がカナダ=アメリカ国境で通過を拒否されたことがあり、これは医療用同位体としてのヨウ素131の使用が原因とされている[15]。上記の物質は、医療用の施設から直接、あるいは治療を受けた患者が排泄することにより下水道に入り込む可能性がある。
治療後の隔離[編集]
ヨウ素131による治療を受けた患者は、その後一ヶ月(量によってはそれ以下)性交を避けなければならない。また6ヶ月間は妊娠しないようにする必要がある。「これは、たとえ保有される放射能の総計がわずかかもしれず、放射性ヨウ素治療における実際の危険性の医学的な証拠はないとしても、成長している胎児に対する理論上の危険性が存在するためである。このような予防策は、放射能への直接の胎児の被曝を本質的に排除し、また放射性ヨウ素からの被曝によって理論上は損傷を受けたかもしれない精子による受胎の可能性を明らかに引き下げる。」[16] これらのガイドラインは病院ごとに異なり、また受けた放射線の量にもよる。放射線量が高い間は子どもを抱かないほうが良い、また他人と1 - 2メートル距離をとった方が良いという主張もある[17]。
ヨウ素131は放射性崩壊により人体からなくなる。崩壊する間、さらに少量は汗や排泄(排尿)でなくなる。このため、治療を受けた患者が使用するトイレ・流し台・ベッドのシーツ・衣服をいつも綺麗にしておくことが推奨される。これにより家族、特に子どもが偶然被曝することを最小限にできる。放射性ヨウ素専用の浄化剤を使うことが望ましい。
現在、多くの空港で核兵器製造に使われかねない放射性物質の密輸を見つけるため放射線検出器を置いている。患者は航空機を使用する場合、治療でヨウ素131の使用後最大95日間、放射線検出器を作動させてしまう可能性があることに注意が必要である[18]。
放射性トレーサーとしての産業利用[編集]
1951年にドイツのミュンヘンで飲料水供給システムの漏水箇所を特定するために初めて使用され、ヨウ素131は同位体水文学および漏水検出で最も一般的に使用されるガンマ線放出産業用放射性トレーサーの1つになった[19][20][21][22]。
1940年代後半以降、石油産業では放射性トレーサーが使用されてきた。地上でタグ付けされた水は、適切なガンマ検出器を使用してダウンホールで追跡され、流れを決定し、地下の漏れを検出する。I-131は、ヨウ化ナトリウム水溶液をタグ付けするのに最も広く使用されている同位体である[23][24][25]。水圧破砕法において、流体の注入の状況とできた亀裂の位置を特定するために利用される[26][27][28]。
出典[編集]
- ヨウ素-131の甲状腺沈着割合と有効半減期 保健物理 Vol.7 (1972) No.4 P213-219
- 悪性褐色細胞腫の131I-MIBGによる放射線内照射療法 放射線利用技術データベース
- 地球環境の放射性物質による汚染 水質汚濁研究 Vol.11 (1988) No.3 P143-147
- 甲状腺癌の放射性ヨード (放射性ヨウ素) 131I内用療法 RADIOISOTOPES Vol.56 (2007) No.3 P141-152
関連項目[編集]
脚注[編集]
- ^ セシウム137、セシウム134とともに主要三核種と呼ばれる。これは軽いため飛び散りやすく、また水溶性であるため人体に摂取されやすいためである。(高田純『放射線防護の基礎知識』イーグルパブリシング、2011年、pp.102-103)
- ^ The Management of Graves’ Disease in Children, with Special Emphasis on Radioiodine Treatment. Scott A. Rivkees, Charles Sklar and Michael Freemark J. Clin. Endocrinol. Metab. 1998 83: 3767-3776, doi: 10.1210/jc.83.11.3767. For full text see: [1]. Quote:
The increased risk of thyroid cancer after thyroid irradiation in childhood has been recognized for nearly 50 yr (119).
Thus, a major concern of iodine-131 therapy relates to the risks of thyroid and nonthyroid cancers. Not surprisingly, this issue has been the focus of several long term follow-up studies involving more than 60,000 patients (56, 120–123). Studies of the effects of external radiation, diagnostic iodine- 131 use, and environmental radioiodine and g-ray exposure have also provided important insights regarding the risks of radiation exposure and thyroid carcinomas (26, 28, 124–128). These studies show that the risk of thyroid cancer is increased with exposure to low or moderate levels of external radiation. In contrast, thyroid cancer risks are much lower after high level irradiation that results in thyroid cell death or reduced capacity of cells to divide (128, 129).
[...]
The large scale epidemiological surveys of the CTSG involving 36,050 patients in the United States (56) and the Swedish cohort studies (16, 121, 141) have provided considerable information about the relative cancer risks after iodine-131 therapy. After treatment of Graves’ disease in adults with iodine-131, which exposes the thyroid gland to high levels of radiation, rates of thyroid cancer and thyroid cancer mortality were not increased (56, 121, 141, 160).
Follow-up data involving children in the CTSG showed that thyroid adenomas developed in 30% of the patients treated in one center with low doses of iodine-131 (50 mCi/g) estimated to result in thyroid exposure of 2500 cGy (56, 88). Yet, in the other centers where children were treated with higher doses of iodine-131 (100–200 mCi/g), the incidence of thyroid neoplasms was not increased (56).
- ^ Chattopadhyay, Sankha; Saha Das, Sujata (2010), “Recovery of 131I from alkaline solution of n-irradiated tellurium target using a tiny Dowex-1 column”, Applied Radiation and Isotopes 68 (10): 1967, doi:10.1016/j.apradiso.2010.04.033, PMID 20471848
- ^ “I-131 Fact Sheet”. 2010年10月26日閲覧。[リンク切れ] see this page for modern production technique
- ^ “Nuclear Data for Safeguards, Table C-3, Cumulative Fission Yields”. International Atomic Energy Agency. 2011年3月14日閲覧。 (thermal neutron fission)
- ^ “Nuclide Safety Data Sheet Iodine-131”. 2013年11月23日閲覧。
- ^ “Chart of Nuclides”. National Nuclear Data Center. 2011年11月17日閲覧。
- ^ Mario Skugor (2006), Thyroid Disorders (A Clevland Clinic Guide), Cleveland Clinic Press, pp. 82, ISBN 9781596240216
- ^ 原子力災害時における甲状腺防護剤としての安定ヨウ素、今堀 彰、日本原子力学会誌、Vol.30 (1988) No.2
- ^ http://www.ecolo.org/documents/documents_in_english/Causes.ChernobyJF.doc
- ^ Simon, Steven; Bouville, André; Land, Charles (2006), “Fallout from Nuclear Weapons Tests and Cancer Risks”, American Scientist 94: 48, doi:10.1511/2006.1.48
- ^ “Radioactive I-131 from Fallout”. National Cancer Institute. 2007年11月14日閲覧。
- ^ “Individual Dose and Risk Calculator for Nevada Test Site fallout”. National Cancer Institute (10/01/07). 2007年10月18日時点のオリジナルよりアーカイブ。2007年11月14日閲覧。
- ^ “I-131 MIBG 製造販売承認申請”. 日本核医学会 (2021年1月28日). 2021年2月22日閲覧。
- ^ “Medical isotopes the likely cause of radiation in Ottawa waste”. CBCnews (04/02/09). 2013年11月23日閲覧。
- ^ “Radioiodine Therapy”. AACE (2004年). 2012年7月17日閲覧。
- ^ “Receiving Radioactive Iodine for Thyroid Cancer”. University of Washington Medical Center. 2013年11月23日閲覧。
- ^ Sutton, Jane (2007年1月29日). “Radioactive patients”. reuters 2009年5月15日閲覧。
- ^ Moser, H.; Rauert, W. (2007). “Isotopic Tracers for Obtaining Hydrologic Parameters”. In Aggarwal, Pradeep K.; Gat, Joel R.; Froehlich, Klaus F.. Isotopes in the water cycle : past, present and future of a developing science. Dordrecht: Springer. p. 11. ISBN 978-1-4020-6671-9 2012年5月6日閲覧。
- ^ Rao, S. M. (2006). “Radioisotopes of hydrological interest”. Practical isotope hydrology. New Delhi: New India Publishing Agency. pp. 12–13. ISBN 978-81-89422-33-2 2012年5月6日閲覧。
- ^ “Investigating leaks in Dams & Reservoirs”. IAEA.org. 2012年5月6日閲覧。
- ^ Araguás, Luis Araguás; Plata Bedmar, Antonio (2002). “Artificial radioactive tracers”. Detection and prevention of leaks from dams. Taylor & Francis. pp. 179–181. ISBN 978-90-5809-355-4 2012年5月6日閲覧。
- ^ Reis, John C. (1976). “Radioactive materials”. Environmental Control in Petroleum Engineering. Gulf Professional Publishers. p. 55. ISBN 978-0-88415-273-6
- ^ McKinley, R. M. (1994). “Radioactive tracer surveys”. Temperature, radioactive tracer, and noise logging for injection well integrity. Washington: U.S. Environmental Protection Agency 2012年5月6日閲覧。
- ^ Schlumberger Ltd. “Radioactive-tracer log”. Schlumberger.com. 2012年5月6日閲覧。
- ^ US patent 5635712, Scott, George L., "Method for monitoring the hydraulic fracturing of a subterranean formation", published 1997-06-03
- ^ US patent 4415805, Fertl, Walter H., "Method and apparatus for evaluating multiple stage fracturing or earth formations surrounding a borehole", published 1983-11-15
- ^ US patent 5441110, Scott, George L., "System and method for monitoring fracture growth during hydraulic fracture treatment", published 1995-08-15
外部リンク[編集]
- ヨウ素-131 原子力資料情報室(CNIC)
- “Iodine:ANL factsheet”. 2013年11月23日閲覧。
- “RadiologyInfo - The radiology information resource for patients: Radioiodine (I -131) Therapy”. 2013年11月23日閲覧。
- “Sensitivity of Personal Homeland Security Radiation Detectors to Medical Radionuclides and Implications for Counseling of Nuclear Medicine Patients”. 2005年12月23日時点のオリジナルよりアーカイブ。2013年11月23日閲覧。
- “NLM Hazardous Substances Databank – Iodine, Radioactive”. 2013年11月23日閲覧。
| 軽量 130I |
ヨウ素131は ヨウ素の同位体である |
重量 132I |
| 131Te (β-) の崩壊生成物 |
ヨウ素131 の崩壊系列 |
131Xe (β-) へ崩壊 |


