心室中隔欠損
| 心室中隔欠損症 | |
|---|---|
 | |
| 心室中隔欠損のシェーマ。 | |
| 概要 | |
| 診療科 | 遺伝医学 |
| 分類および外部参照情報 | |
| ICD-10 | Q21.0 |
| ICD-9-CM | 745.4 |
| DiseasesDB | 13808 |
| eMedicine | med/3517 |
心室中隔欠損(しんしつちゅうかくけっそん; VSD: Ventricular septal defect)は、先天性心疾患[1]の一つ。心室中隔に欠損孔が開き、シャントが生じている状態を指す。
概論[編集]
心室中隔欠損は、小児の先天性心疾患としては最多頻度のもので先天性心疾患の30%を占め[2]、新生児全体では1000人に3人の割合で出生し、うち約半数は生後1年以内に自然閉鎖することが知られている[3]、最終的には70~75%は欠損孔が最終的に自然閉鎖するが2歳を過ぎると閉鎖する確率が低下して10%ほどになる[2]。 また、逆に欠損孔が大きい場合は心房中隔欠損などと異なり乳児期に心不全を起こす可能性が大きい[4]ので、成人においては、先天性心疾患入院例の15%を占めるのみである。
構造上、他の先天性心疾患の内ファロー四徴症、両大血管右室起始症、総動脈幹症[5]などは原則的に心室中隔欠損を併発し、原則ではないものの心内膜床欠損症や右旋性大血管転位などでも併発例があるがこれらの心室中隔欠損については各自の記事を参照。
本症は欠損孔の部位によって分類され、一般的にKirklinの分類が使用される[6]。
- Kirklin-I型
- 高位欠損、漏斗部欠損、Soto分類における右室流出路欠損、Anderson分類におけるdoubly committed subarterial typeと同義。欠損孔が中隔壁の上方に位置しており、大動脈弁右冠尖に近いことから、弁の逸脱から大動脈弁閉鎖不全症を呈する恐れがある。白人では数%ほどだが、アジア系民族では、全心室中隔欠損症の約30%を占める[2]。
- Kirklin-II型
- 膜様部欠損型。頻度は最多で心室中隔欠損症の2/3を占める[2]。自然閉鎖の傾向が強い。
- Kirklin-III型
- 心内膜床欠損型。頻度は最少であるがダウン症候群では合併する頻度の高い心奇形のひとつ(約40%)である[7]。詳しくは心内膜床欠損症(もしくは房室中核欠損症)の完全型を参照。
- Kirklin-IV型
- 筋性部欠損型。日本人を含むアジア系では3~5%と低いが、白人では10~20%を占める[2]。自然閉鎖例が多い。
病態生理[編集]
血液の短絡量と方向によって症状が変わり、短絡量は欠損孔の大きさと肺血管抵抗によって決定されるので以下のように変化する。なお、重篤な場合(肺高血圧進行時)を除いて 右室に流れ込んだ血液はそのまま肺動脈に流れ込むので右室への容量負荷(拡張)は目立たず、普通は左房・左室・肺動脈が拡張する(逆に心室中隔欠損だけで右室拡張が見られる場合は重篤になっている)[8][9]。
- 欠損孔が小さい場合(大動脈弁輪径の1/3以下)
短絡量が少ないので肺動脈への影響も少なく、血行動態はほぼ正常(ただし短絡する血流の流れが激しくなっているので感染性心内膜炎(IE)を起こす確率は欠損孔が大きいケースと変わらない)。成人例は多くはこのタイプ。 - 欠損孔が中等度(大動脈弁輪径の1/2前後)の場合
圧の高い左室から圧の低い右室への左→右シャントが発生し、肺血流量の増加と左室の容量負荷が生じる。肺動脈圧は正常ないし軽度上昇である。 - 欠損孔が大きい(大動脈弁輪径とほぼ同じ)場合
右室圧は左室圧に等しくなり、肺高血圧を生じる。さらに肺高血圧が進展していくにつれ左右の圧力差が減るので一度は短絡量が減るが、さらに進んで右室側が高圧になるとシャントの方向が逆転して右→左シャントとなり、これをアイゼンメンゲル(Eisenmenger)症候群といいチアノーゼが起きるようになる。アイゼンメンゲル化の頻度はほぼ50パーセントで、この時点で原疾患への手術適応がなくなり[10]、完治には心肺同時移植が必要となる。一方、アイゼンメンゲル化する以前の軽症例のうち、肺体血流比が1.5以上であった場合は手術による治療が可能である。
所見[編集]
臨床所見[編集]
- 自覚症状
- 軽度の欠損孔の場合は、自覚症状はほぼ皆無であるが感染性心内膜炎のリスクがある[4]。
中等度以上の欠損孔の場合は、肺の鬱血により早ければ乳児期から呼吸困難や呼吸器感染症を起こし、時に心不全に陥る[4]。
軽度の易疲労性や動悸が見られるほか、ときに呼吸器感染の反復が見られる場合がある。
高度の欠損孔の場合は、易疲労性などの自覚症状のほか、乳児期から心不全や体重増加不良を認める。
- 聴診
- 聴診においては、胸骨左縁の逆流性収縮期雑音(欠損孔を通過する血液の音)が特徴的である。欠損孔が小さいと勢いを増して流れ込み乱流が激しくなるので雑音が逆に大きくなる[4]。最強点の高さは欠損部位によって変わり、Kirklin-I型においては第2〜3肋間と高いため、肺動脈弁狭窄などとの鑑別が重要である。一方、Kirklin-II〜IV型においては第4肋間と低く、比較的鑑別は容易である。強度は、Levineの6段階分類法で2〜5度である。
また、シャント量の増大でII音の分裂およびIII音の出現、肺高血圧の進展でII音の亢進と拡張期Graham Steell雑音(肺動脈弁閉鎖不全による)の出現がありうるが、アイゼンメンゲル症候群になると右から左への短絡量がさほど多くないので雑音はかえって減弱ないし消失する[4]。 - その他
- 外見上、胸郭において吸気性陥没、頻呼吸が見られる場合がある。
検査所見[編集]
- 胸部X線
- 中等度ないし高度の欠損孔の場合は、左-右短絡に伴う肺血流量増加所見(肺血管陰影の増強、左第4弓の突出、左房・左室拡大)が認められる[11]。アイゼンメンゲル化した場合は、さらに第2弓が突出する。また通常は肺血流量が多くなるので末梢まで肺血管陰影を追えるが、アイゼンメンゲル症候群時は肺野は明るくなり末梢血管陰影が乏しくなる[11][12]。
- 心電図
- 中等度の欠損孔の場合は左室肥大、高度の欠損孔の場合は肺高血圧進展でさらに右室肥大を示す[11]。また、Kirklin-III型(心内膜床欠損型)においては左軸偏位を呈する。アイゼンメンゲル化した場合は左室肥大がなくなり、右室肥大のみが残る[11]。
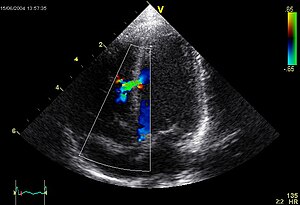
- 心臓超音波検査
- 断層法において、中〜高度欠損孔は心室中隔の孔として観察される。また、カラー・ドプラー法により短絡血流を描出できるほか、肺動脈圧の推定も可能である。
- 心臓カテーテル検査
- 中〜高度欠損孔においては、右室において酸素飽和度のステップアップ[13]、肺血圧の上昇を認める。また、左室造影を行なうことで短絡が造影され、左室の容積と駆出率が求められる。
治療[編集]
経過観察[編集]
心室中隔欠損は自然閉鎖傾向があるので小さくて無症状の場合(成人例の多く)は経過観察で十分となる(特に運動制限もない)。ただし感染性心内膜炎を起こしやすいのでその予防に努める[14]。(年に1~2回の定期検査が推奨される[15]。)
内科的治療[編集]
内科的治療は、本症に合併した心不全や感染性心内膜炎(IE)、呼吸器疾患などに対して行なわれる。左室・左房の容量負荷を除去するための利尿薬が第一選択となり、フロセミド、スピロノラクトンを1〜3mg/kg/日投与する。頻脈がある場合にはジゴキシン、末梢冷感が強く僧帽弁逆流などを合併する場合にはACE阻害薬が併用されうるが、心不全の増悪などについて注意を要する。
また、IE予防のため、抜歯など菌血症のリスクを伴う処置の際には、抗菌剤の予防投与を行う。
なお、アイゼンメンゲル化して外科治療の適応外となった症例に対しては、肺高血圧への対症療法として、酸素投与や亜硝酸剤、カルシウム拮抗薬などが用いられる。
外科的治療[編集]
手術そのものは人工心肺下で右心房を開いて三尖弁側から右心室をのぞき込む形(心室は切開しない)で欠損孔を直接またはパッチを当てて塞ぐ[14]。外科的治療が考慮されるのは以下の場合である。
- 中〜高度欠損孔で肺/体血流比が1.5以上(左-右短絡率が33%以上)で収縮傾向がなく左室拡大を認める場合[14]。
肺高血圧を合併する例では2歳までに手術を済ませる。2歳以上であっても肺血管抵抗8単位以下なら手術適応[15]。 - Kirklin-I型(漏斗部欠損)に大動脈弁逸脱・大動脈弁閉鎖不全症や逆流を認める場合[14]。
この場合、欠損孔が大動脈弁に近い位置(高位)のため、短絡の流れに引き寄せられ、逸脱した大動脈弁に欠損孔が覆われて短絡血流が減少・消失して心室中隔欠損としては改善するが弁が変形して閉鎖不全につながり結局左室の容量負荷による機能低下になることがある。また、成人したのちにこの弁の逸脱が後述のバルサルバ洞動脈瘤になり破裂して急性発症(急性心不全につながる)する危険があるため、注意が必要である[16][17]。 - 小欠損孔においても感染性心内膜炎(IE)を再発する場合[14]。
IEの治癒より6か月が経過して以後に手術を行う。 - バルサルバ(Valsava)洞[18]動脈瘤を合併した場合[16]。
なお、肺高血圧が進展して肺/体血流比が1.5以下となっている場合は、アイゼンメンゲル症候群となっていることから、外科的治療の適応はなくなり[14]、完治には心肺同時移植が必要となる。
脚注[編集]
- ^ 弁置換手術などの術後にも生じることがある
- ^ a b c d e (高橋2015)p.145「概念」
- ^ 心室中隔欠損 - 日本小児外科学会
- ^ a b c d e (高橋2015)p.146-147「症状」
- ^ 大動脈と肺動脈が分離せず、1本の太い動脈が心室から起始する疾患。((高橋2015)p.176「3 総動脈幹症」)
- ^ (医学情報研究所2017)p.149「分類」
- ^ (高橋2015)p.149「C 房室中隔欠損症」
- ^ (高橋2015)p.146「血行動態」
- ^ (医学情報研究所2017)p.150「病態生理」
- ^ 手術すると右→左短絡していた血液の逃げ場がなくなりすでに高かった肺血管抵抗がさらに悪化し右心不全を起こす。((高橋2015)p.145「STEP3 Eisenmenger症候群」)
- ^ a b c d (高橋2015)p.147「検査」
- ^ (医学情報研究所2017)p.151「胸部X線像」
- ^ 右心系(右心房→右心室→肺動脈)は静脈血が流れており、途中に酸素供給もないのでカテーテルを進めて酸素飽和度を測定した場合、通常はずっと低いままであるので途中で上昇がある場合どこからか左心系から動脈血が短絡していることになる。
上昇場所で「右心房→心房中隔欠損」「右心室→心室中隔欠損」「肺動脈→動脈管開存」がそれぞれ疑われる。
((高橋2015)p.63「C 酸素飽和度」) - ^ a b c d e f (高橋2015)p.148「治療」
- ^ a b (医学情報研究所2017)p.152「治療」
- ^ a b (高橋2015)p.148「合併症」
- ^ (医学情報研究所2017)p.150「合併症」
- ^ 大動脈基部の隆起した部位、大動脈洞とも。((医学情報研究所2017)p.9「Valsava洞」)
参考文献[編集]
- 大関武彦, 古川漸, 横田俊一郎『今日の小児治療指針 第14版』医学書院、2006年。ISBN 978-4-260-00090-1。
- 高久史麿, 尾形悦郎, 黒川清, 矢崎義雄『新臨床内科学 第8版』医学書院、2002年。ISBN 978-4-260-10251-3。
- 梅村敏(監) 木村一雄(監) 高橋茂樹『STEP内科5 循環器』海馬書房、2015年、p.145-148「B 心室中隔欠損」 他頁。ISBN 978-4-907921-02-6。
- 医学情報研究所 編集『病気がみえる vol.2 循環器』(4版)株式会社メディックメディア、2017年、p.148-152「心室中隔欠損症(VSD)」(監修:早渕康信) 他頁。ISBN 978-4-89632-643-7。
