塩素酸カリウム
| 塩素酸カリウム | |
|---|---|
| |

| |
別称 塩素(V)酸カリウム | |
| 識別情報 | |
| CAS登録番号 | 3811-04-9 |
| EC番号 | 223-289-7 |
| 国連/北米番号 | 1485 |
| RTECS番号 | FO0350000 |
| 特性 | |
| 化学式 | KClO3 |
| モル質量 | 122.55 g/mol |
| 外観 | 白色の結晶粉末 |
| 密度 | 2.32 g/cm3, 固体 |
| 融点 |
356 °C, 629 K, 673 °F |
| 沸点 |
~400 °C (分解) |
| 水への溶解度 | 7.3 g/100 ml (20 °C) |
| 熱化学 | |
| 標準生成熱 ΔfH |
−397.73 kJ mol−1[1] |
| 標準モルエントロピー S |
141.3 J mol−1K−1 |
| 標準定圧モル比熱, Cp |
100.25 J mol−1K−1 |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 0548 |
| EU分類 | 酸化剤(O) 有害(Xn) 環境への危険性(N) |
| EU Index | 017-004-00-3 |
| NFPA 704 | |
| Rフレーズ | R9, R22, R51/53 |
| Sフレーズ | (S2), S13, S16, S27, S61 |
| 引火点 | なし |
| 関連する物質 | |
| その他の陰イオン | 臭素酸カリウム ヨウ素酸カリウム |
| その他の陽イオン | 塩素酸アンモニウム 塩素酸ナトリウム 塩素酸バリウム |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
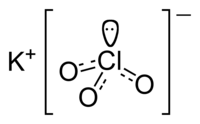
塩素酸カリウム(えんそさんカリウム、potassium chlorate)は化学式 KClO3 と表される、カリウムの塩素酸塩。塩剥(えんぼつ、えんぽつ)ともいう。CAS登録番号は [3811-04-9]。1786年に、クロード・ルイ・ベルトレー (Claude Louis Berthollet) により合成された。
生成方法[編集]
塩化カリウムの濃厚(飽和)水溶液を電気分解してつくられる。アノードにはMMO電極(混合金属酸化物電極)、白金、黒鉛、二酸化鉛などの不溶性電極が使われる。カソードにはチタン、ステンレス鋼、軟鋼などが使われる。アノードの侵食を抑制するためには次の3つの条件が必要。①アノード上での電流密度の上限はMMO電極や白金では200~300mA/cm2、黒鉛では30mA/cm2程度が適切。また、アノード表面での電流密度の偏りを無くすためアノードを取り囲むようにカソードを配置する。②溶液中の塩化物イオン濃度(塩化カリウム濃度)を飽和状態に保ちアノードの侵食を抑える(そのためには塩素酸カリウムを生成したことにより消費した分の塩化カリウムを定期的に補給する)。③アノード周辺の溶液の温度を40℃以下に保つ。
生成する塩素酸カリウムの量は電流に依存し電圧は塩素の過電圧以上であれば無関係。そのため電圧は可能な限り低い値が望ましい(3~5V程度)。
反応は次の通り。
- 全反応 KCl + 3 H2O → KClO3 + 3 H2
- アノード 2Cl- → Cl2 + 2e-
- カソード 2H+ + 2e- → H2 (酸性条件)
2H2O + 2e- → H2 + 2OH- (アルカリ性条件)
アノードで生成された塩素がその場で水や水酸化イオン(水酸化カリウム)と反応し次亜塩素酸HClOや次亜塩素酸イオンClO-を生じる。その後、塩素酸イオンが生成する経路は
■①次亜塩素酸2分子と1個の次亜塩素酸イオンが溶液中で反応(化学的塩素酸塩形成、弱酸性(pH=約6.8)で起きる。 1個の塩素酸イオンを生成するのに6電子が必要。)
■②次亜塩素酸イオンがアノード上で酸化(電気的塩素酸形成、アルカリ性(高いpH)。 1個の塩素酸イオンを生成するのに9電子が必要。)
の2つがある。前者①は高温(約70℃)が必要なのに対して後者②は低温でも起きる。(いずれの場合もアノードの侵食を抑えるためにアノード周辺の溶液は40度以下に保つ。)
■①次亜塩素酸2分子と1個の次亜塩素酸イオンが溶液中で反応(化学的塩素酸塩形成)
アノードで生成した塩素は水と反応して次亜塩素酸HClOと塩酸HCLを生じる。
- Cl2 + H2O ⇋ HClO + H+ + Cl−
この次亜塩素酸の一部が解離して次亜塩素酸イオンClO-を生じる。
- HClO → ClO- + H+
これにより次亜塩素酸HClOと次亜塩素酸イオンClO-が2:1の比率で反応し塩素酸イオンClO3-が生じる。この2:1の比率になるのは弱酸性(pH=約6.8)の時。よって化学的塩素酸塩形成では厳密なpH制御が必要になる。
- 2 HClO + ClO- → ClO3- + 2 Cl− + 2 H+
全反応は次のようになる。
- 3 HClO → ClO3- + 2 Cl- + 3 H+
■②次亜塩素酸イオンがアノード上で酸化(電気的塩素酸形成)
アノードで生成した塩素が溶液の水素イオン濃度に応じて水や水酸化イオン(水酸化カリウム)と反応し次亜塩素酸HClOや次亜塩素酸イオンClO-を生じる。
- Cl2 + H2O ⇋ HClO + H+ + Cl− (酸性条件)
- Cl2 + 2 OH- → ClO- + Cl− + H2O (アルカリ性条件)
生じた次亜塩素酸イオンClO-は3個で塩素酸イオンClO3-1個をアノード表面で生じる。
- 3 ClO− + 3/2 H2O → ClO3- + 3 H+ + 2 Cl− + 3/4 O2 + 3 e-
アノード表面で次亜塩素酸イオンから電子を引き抜かれてラジカルを生じ、このラジカルが水と反応して原子が再配列することにより塩素酸イオンが生成すると考えられる。
- 3 ClO- + 3/2 H2O → 3 ClO• + 3/2 H2O + 3 e-
- 3 ClO• + 3/2 H2O → ClO3- + 3 H+ + 2 Cl- + 3/4 O2
この反応はアルカリ性(高pH)で起こりやすい。①化学的塩素酸塩形成に比べると必要な電子数が5割増(6個→9個)の為に電力量も5割増になるがpH制御は必要なくなる。
また、①②いずれにおいてもクロム酸カリウムや二クロム酸カリウムなどのクロム酸塩、二クロム酸塩やフッ化ナトリウムを少量、溶液中に添加するとカソード上で起こる逆反応(次亜塩素酸イオンや塩素酸イオンの塩化物イオンへの還元反応)
- ClO- + H2O + 2e- → Cl- + 2OH-
- ClO3- + 3H2O + 6e- → Cl- + 6OH-
を抑制できる。(ただしクロム酸塩や二クロム酸塩は二酸化鉛に対しては使えない。また、フッ化ナトリウムはMMO電極に対しては使えない。) これは水酸化クロムの多孔質膜がカソードに形成される為。この膜はカソードへの陰イオンの接近を妨げるが陽イオンの接近とその還元は促進する。膜は特定の厚さに達すると自然に成長を停止する。[2]
工業的製法では、塩素酸ナトリウムと塩化カリウムの複分解により生成する。
- NaClO3(aq) + KCl(aq) → NaCl(aq) + KClO3(s)
この反応は塩素酸カリウムの水への溶解度が低く、生成物の連続的な沈殿により化学平衡が右側に移動することで起こる(ルシャトリエの原理)。前駆体の塩素酸ナトリウムは、塩化ナトリウムの電気分解により工業的に大量に製造される。[2]
直接の電気分解以外としては次の方法がある。しかし工業的には廃れた。
塩素酸カリウムは次亜塩素酸ナトリウム水溶液中で加熱により不均化した後、塩化カリウムとの複分解によっても生成する。[3]
- 3NaClO(aq) → 2 NaCl(s) + NaClO3(aq)
この時、次亜塩素酸HClOの塩素酸イオンClO3-への不均化が起こる(ただし、この反応は高温でないと進行しない。そして遅い)。
- 3ClO- → 2Cl- + ClO3-
生じた塩素酸イオンはカリウムイオンK+により塩素酸カリウムとして析出・沈殿。
- NaClO3(aq) + KCl(aq) → NaCl(aq) + KClO3(s)
また、塩素ガスを水酸化カリウムの水溶液(高温)に通すことによっても生成する。 [4]
- 3 Cl2(g) + 6 KOH(aq) → KClO3(aq) + 5 KCl(aq) + 3 H2O(l)
いずれの場合も得られた粗製塩素酸カリウムの結晶は熱水からの再結晶で精製する。(水への溶解度の差が高温と低温の間で大きく、熱飽和水溶液を冷却することで容易に沈殿・分離する。この熱飽和水溶液を作成する段階で約10分間の沸騰も同時に行い、不安定な不純物である亜塩素酸カリウムや次亜塩素酸カリウムを分解する。この沸騰は偶発的な発火を防ぐために必要。)その後、吸引ろ過を行い結晶に付着した水(微量の不純物を含む)を除去し精製する。
性質[編集]
- 密度 2.326 g/cm3、融点は 356 ℃ で、無色の光沢をもつ単斜板状結晶[5]。
- 吸湿性はない。
- 水に溶けアルコールにもいくぶん溶ける。
- 中性およびアルカリ性溶液では酸化作用を示すことは少ない(水溶液は基本的には中性)が、酸性にすると強い酸化剤となる。その標準酸化還元電位は以下の通りである。
- 加熱すると、酸素を放出して、塩化カリウムになる。この反応は金属酸化物、とくに二酸化マンガン MnO2 を加えると促進される。二酸化マンガンを触媒として加熱する時、70 ℃ ぐらいで酸素を発生しはじめるので実験室などで酸素を得るために利用される。ただし、有機物・硫黄・赤リン・炭素などの可燃物が混入していると爆発することがあるので注意を要する。
用途[編集]
酸化剤としてマッチ・花火・爆薬(スプレンゲル爆薬、チェダイト、ミージアンキー)などの原料となり、漂白剤・染料・医薬品などの製造にも用いられる。しかし、速度論的に不安定なため現在では花火と爆薬の用途に使われることはほとんどなく過塩素酸カリウムに置き換えられた。光に当てたり長期間保存したものは感度が特に高い亜塩素酸カリウムを含み、乾燥状態では有機物・赤リン・硫黄などの可燃性物質と接触しただけでも爆発することがある。また新しいものでも摩擦・衝撃などに鋭敏で、爆発事故をおこしやすく、濃硫酸・濃硝酸に触れても爆発しやすい。混合爆薬として用いられることもある。
安全性[編集]
塩素酸カリウムを始めとする塩素酸塩は反応性が高く、多くの可燃性物質と混合し点火すると激しく燃焼し、場合によっては自発的・偶発的に発火や爆発することがある。塩素酸カリウムと赤リンの混合物はアームストロングの混合物と呼ばれて僅かな刺激でも発火・爆発する。 また酸の存在下では二酸化塩素や塩素酸を生じて発火する危険がある。昇華により精製された硫黄「硫黄華」は、全体的に高純度であるにもかかわらずかなりの量の硫黄酸を含んでいる。ほとんどの硫黄には微量の酸(ポリチオン酸や亜硫酸など)が含まれており、塩素酸カリウムと硫黄の組成物は自然発火を引き起こす可能性がある。また、塩素酸カリウムと発火促進特性を持つ化合物(硫化リン、硫化アンチモンなど)の混合物も、衝撃や摩擦に非常に敏感であるため非常に危険である。 そのため塩素酸カリウムを含む火工品組成物では赤リン・硫黄・硫化リン・硫化アンチモンなどを避ける必要がある。
また、不純物の混入にも気を付ける必要がある。銅イオンにより塩素酸銅を生じる。硝酸アンモニウムなどのアンモニウム塩と混合すると塩素酸アンモニウムを生じる。いずれも極めて発火・爆発しやすく危険である。
規制[編集]
GHSにおける酸化性固体(区分2)に該当し、各国で貯蔵や運搬に規制がある(国連番号1485)。日本では船舶安全法や航空法によってGHSに基づく規制があり、また消防法に基づく危険物第1類に指定されている。日本国内では毒物及び劇物取締法に基づき劇物に指定されている(昭和40年政令第2号)が、急性毒性や刺激性は他の劇物ほど高くない。
参考文献[編集]
- 化学大辞典編集委員会(編)、1993、『化学大辞典』第1巻、共立出版 ISBN 978-4-320-04015-1
- Wagman, D.D.; Evans, W.H.; Parker, V.B.; Schumm, R.H.; I. Halow; S.M. Bailey; K.L. Churney; R.I. Nuttal; K.L. Churney and R.I. Nuttal (1982) (英語). The NBS tables of chemical thermodynamics properties. Journal of physical and chemical reference data. volume 11 Suppl. 2. ISBN 0883184176. NCID BA18990540
関連項目[編集]
脚注[編集]
- ^ Wagman et al. 1982.
- ^ a b Vogt, Helmut; Balej, Jan; Bennett, John E.; Wintzer, Peter; Sheikh, Saeed Akbar; Gallone, Patrizio (June 15, 2000). “Chlorine Oxides and Chlorine Oxygen Acids”. In Ullmann. Ullmann's Encyclopedia of Industrial Chemistry. Wiley‐VCH Verlag. doi:10.1002/14356007.a06_483. ISBN 9783527303854
- ^ Anne Marie Helmenstine, Ph.D.. “Potassium Chlorate Synthesis (Substitute) Formula”. About.com Education. 2015年7月9日閲覧。
- ^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0-07-049439-8
- ^ 化学大辞典編集委員会編 1993.




