クロム酸塩


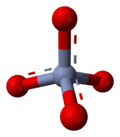
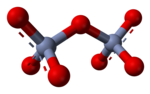
クロム酸塩(クロムさんえん、英: chromate)および二クロム酸塩(にクロムさんえん、英: dichromates)は、それぞれクロム酸と二クロム酸の塩のことである。クロム酸塩はクロム酸イオン、CrO42− を持ち、鮮やかな黄色を呈する。一方、二クロム酸塩は二クロム酸イオン、Cr2O72− を含み、鮮やかな橙色を呈する。
特徴[編集]
クロム原子は両方とも酸化数が +6 であり、どちらのアニオンも強力な酸化剤である。酸化数 +6(または VI)のクロムはしばしば六価クロムと呼ばれる。
水溶液では、クロム酸イオンと二クロム酸イオンは化学平衡の関係にある。
この平衡は低 pH のとき二クロム酸側が優勢になり、pH が塩基性になるとクロム酸側が優勢になる。これはルシャトリエの原理の古典的な例である。また、この平衡は溶液中のクロム濃度にも依存する。
酸化剤または酸化還元反応の滴定剤として使われ、そのとき六価クロムは還元されて青緑色の三価クロムが生ずる。
ナトリウム、カリウム、アンモニウム塩は水溶性の粒状の固体で、化学実験において広く用いられる。また重金属、ランタノイド、アルカリ土類金属のクロム酸塩および二クロム酸塩は水に僅かにしか溶けない。かつては水に難溶性もしくは不溶性のクロム酸塩は黄色顔料として使われていたが、毒性が強く耐光性に弱い上硫化水素により黒変するため、環境問題の観点上から製造・使用が制限されてきている。また、水に難溶性もしくは不溶性の二クロム酸塩は以前から顔料としても使用されておらず、水に難溶性もしくは不溶性のクロム酸塩も顔料以外の用途が極めて少ないため、重金属、ランタノイド、アルカリ土類金属のクロム酸塩および二クロム酸塩の有用性はほとんどなくなっている。
用途[編集]
化学的酸素要求量 (COD) 計測による環境解析に使われる。
亜鉛、アルミニウムなどの金属の防蝕剤として使われる。
構造[編集]
クロム酸塩鉱物[編集]

鉱物学において、クロム酸塩からなる鉱物をクロム酸塩鉱物(クロムさんえんこうぶつ、英: chromate mineral)という。
クロム酸塩鉱物は自然界では滅多に見られないが、最もよく見られるのは紅鉛鉱である。カリウムを含むクロム酸鉱物及びその関連鉱物がアタカマ砂漠で見られるが、かなり稀少である。
安全性[編集]
クロム酸塩、二クロム酸塩ともに発癌性である。六価クロムの化合物はその全てが毒性および発癌性を有すると見なすことができる。労働安全衛生法では「クロム酸およびその塩」として、第2類特定化学物質に指定されている。
脚注[編集]
参考文献[編集]
この節の加筆が望まれています。 |