熱力学ポテンシャル (ねつりきがくポテンシャル、英語 : thermodynamic potential )とは、熱力学 において、系の平衡状態 における熱力学的性質の情報を全て持つ示量性 状態量である。完全な熱力学関数 とも呼ばれる[1]
概要 「熱力学的性質の情報を全て持つ」とは全ての状態量がこの関数の偏微分 の組み合わせにより与えられるという意味である。言い換えれば、完全な熱力学関数が与えられればそこから状態方程式 が決まる[2] 統計力学 から導出される。熱力学からは関数形に制約を与えるが具体的な関数形は得られない。
熱力学ポテンシャルの一つである内部エネルギー U は、エントロピー S 、物質量 N 、体積 V 、或いはその他の示量性状態量[3] X を変数に持つ関数 U (S ,N ,V ,X )
(
∂
U
∂
S
)
N
,
V
,
X
=
T
(
S
,
N
,
V
,
X
)
{\displaystyle \left({\frac {\partial U}{\partial S}}\right)_{N,V,X}=T(S,N,V,X)}
(
∂
U
∂
N
i
)
S
,
V
,
X
=
μ
i
(
S
,
N
,
V
,
X
)
{\displaystyle \left({\frac {\partial U}{\partial N_{i}}}\right)_{S,V,X}=\mu _{i}(S,N,V,X)}
(
∂
U
∂
V
)
S
,
N
,
X
=
−
p
(
S
,
N
,
V
,
X
)
{\displaystyle \left({\frac {\partial U}{\partial V}}\right)_{S,N,X}=-p(S,N,V,X)}
(
∂
U
∂
X
)
S
,
N
,
V
=
x
(
S
,
N
,
V
,
X
)
{\displaystyle \left({\frac {\partial U}{\partial X}}\right)_{S,N,V}=x(S,N,V,X)}
となり、熱力学温度 T 、化学ポテンシャル μi 、圧力 p 、及び X に対応する示強性状態量[4] x が得られる。これらの状態量から熱容量 や圧縮率 なども計算される。内部エネルギーの全微分は
d
U
=
T
d
S
+
∑
i
μ
i
d
N
i
−
p
d
V
+
x
d
X
{\displaystyle dU=T\,dS+\sum _{i}\mu _{i}\,dN_{i}-p\,dV+x\,dX}
となる。全微分の形を変形すれば
d
S
=
1
T
d
U
−
∑
i
μ
i
T
d
N
i
+
p
T
d
V
−
x
T
d
X
{\displaystyle dS={\frac {1}{T}}\,dU-\sum _{i}{\frac {\mu _{i}}{T}}\,dN_{i}+{\frac {p}{T}}\,dV-{\frac {x}{T}}\,dX}
となり、エントロピーは内部エネルギー、物質量、体積、或いはその他の示量性状態量を変数にもつ関数 S (U ,N ,V ,X )S (U ,N ,V ,X )U による偏微分は
(
∂
S
∂
U
)
N
,
V
,
X
=
1
T
(
U
,
N
,
V
,
X
)
{\displaystyle \left({\frac {\partial S}{\partial U}}\right)_{N,V,X}={\frac {1}{T(U,N,V,X)}}}
であり、この式は熱力学温度を導入する関係式として用いられる。
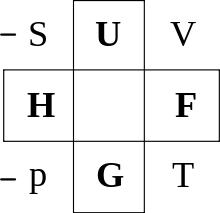
ルジャンドル変換 ルジャンドル変換で繋がっている熱力学関数 とその変数のまとめ(参照:en:Thermodynamic square ) 完全な熱力学関数には自然な変数の組があり、同じ状態量であっても、変数が異なればそれは完全な熱力学関数とはならない。例えば、内部エネルギー U は、エントロピー S に変えて温度 T を変数に持つときには完全な熱力学関数とはならない。系の平衡状態を指定する状態変数の組が (T ,N ,V ,X ) である場合は、ルジャンドル変換
d
F
=
d
(
U
−
T
S
)
=
−
S
d
T
+
∑
i
μ
i
d
N
i
−
p
d
V
+
x
d
X
{\displaystyle dF=d(U-TS)=-S\,dT+\sum _{i}\mu _{i}\,dN_{i}-p\,dV+x\,dX}
によってヘルムホルツエネルギー F が完全な熱力学関数となる。
エントロピーに対してもルジャンドル変換を考えることができて
d
Ψ
=
d
(
S
−
β
U
)
=
−
U
d
β
+
∑
i
μ
i
T
d
N
i
−
p
T
d
V
+
x
T
d
X
{\displaystyle d\Psi =d(S-\beta U)=-U\,d\beta +\sum _{i}{\frac {\mu _{i}}{T}}\,dN_{i}-{\frac {p}{T}}\,dV+{\frac {x}{T}}\,dX}
などの完全な熱力学関数を導入することができる[5] Ψ =−F /T [6]
熱力学ポテンシャルとその変数の例[6]
熱力学ポテンシャル
記号
自然な変数
微分
内部エネルギー U (S ,N ,V ,X )
dU =TdS +μdN −pdV +xdX
エンタルピー H (S ,N ,p ,x )
dH =TdS +μdN +Vdp −Xdx
ヘルムホルツエネルギー F (T ,N ,V ,X )
dF =−SdT +μdN −pdV +xdX
ギブズエネルギー G (T ,N ,p ,x )
dG =−SdT +μdN +Vdp −Xdx
グランドポテンシャル J (T ,μ ,V ,X )
dJ =−SdT −Ndμ +Vdp −Xdx
エントロピー S (U ,N ,V ,X )
dS =(1/T )dU −(μ /T )dN +(p /T )dV −(x /T )dX
Massieu関数
Ψ (β ,N ,V ,X ) [5] dΨ =−Udβ −(μ /T )dN +(p /T )dV −(x /T )dX
Kramers関数
Φ (β ,α ,V ,X ) [5] dΦ =−Udβ +Ndα +(p /T )dV −(x /T )dX
ギブズ-デュエムの関係 系のスケール変換を考えると、内部エネルギー U 、エントロピー S 、体積 V 、物質量 N の示量性から
U
(
λ
S
,
λ
V
,
λ
N
)
=
λ
U
(
S
,
V
,
N
)
{\displaystyle U(\lambda S,\lambda V,\lambda N)=\lambda U(S,V,N)}
である。U の同次性 から
U
=
S
∂
U
∂
S
+
V
∂
U
∂
V
+
∑
i
N
i
∂
U
∂
N
i
=
S
T
−
V
p
+
∑
i
N
i
μ
i
{\displaystyle U=S{\frac {\partial U}{\partial S}}+V{\frac {\partial U}{\partial V}}+\sum _{i}N_{i}{\frac {\partial U}{\partial N_{i}}}=ST-Vp+\sum _{i}N_{i}\mu _{i}}
の関係が導かれる。
ルジャンドル変換をしていくと、
H
=
U
+
p
V
=
S
T
+
∑
i
N
i
μ
i
{\displaystyle H=U+pV=ST+\sum _{i}N_{i}\mu _{i}}
F
=
U
−
T
S
=
−
V
p
+
∑
i
N
i
μ
i
{\displaystyle F=U-TS=-Vp+\sum _{i}N_{i}\mu _{i}}
G
=
F
+
p
V
=
∑
i
N
i
μ
i
{\displaystyle G=F+pV=\sum _{i}N_{i}\mu _{i}}
J
=
F
−
∑
i
μ
i
N
i
=
−
V
p
{\displaystyle J=F-\sum _{i}\mu _{i}N_{i}=-Vp}
などの関係式が得られる。
また、この式を微分すると
S
d
T
−
V
d
p
+
∑
i
N
i
d
μ
i
=
0
{\displaystyle S\,dT-V\,dp+\sum _{i}N_{i}\,d\mu _{i}=0}
の関係式が得られる。この関係式をギブズ-デュエムの関係 と言い、示強性状態量の組 (T , p , μ ) を系の平衡状態を指定する状態変数として選ぶことは出来ないことを表している。
平衡状態の安定性 系が温度 T ex 熱力学第二法則 から、系に変化が起きるとき
δ
′
Q
≤
T
ex
δ
S
{\displaystyle \delta 'Q\leq T_{\text{ex}}\delta S}
である。一方、エネルギー保存則 から
δ
′
Q
=
δ
U
+
δ
′
W
=
δ
U
+
p
ex
δ
V
−
μ
ex
δ
N
{\displaystyle \delta 'Q=\delta U+\delta 'W=\delta U+p_{\text{ex}}\delta V-\mu _{\text{ex}}\delta N}
である。p ex μ ex
δ
U
−
T
e
x
δ
S
+
p
e
x
δ
V
−
μ
e
x
δ
N
≤
0
{\displaystyle \delta U-T_{\mathrm {ex} }\delta S+p_{\mathrm {ex} }\delta V-\mu _{\mathrm {ex} }\delta N\leq 0}
となる。系が平衡状態 にあるとき、変化が起こらない ので、
δ
U
−
T
e
x
δ
S
+
p
e
x
δ
V
−
μ
e
x
δ
N
>
0
{\displaystyle \delta U-T_{\mathrm {ex} }\delta S+p_{\mathrm {ex} }\delta V-\mu _{\mathrm {ex} }\delta N>0}
である。
これが成り立つ条件は、1次変分について
(
∂
U
∂
S
−
T
e
x
)
δ
S
+
(
∂
U
∂
V
+
p
e
x
)
δ
V
+
(
∂
U
∂
N
−
μ
e
x
)
δ
N
=
0
{\displaystyle \left({\frac {\partial U}{\partial S}}-T_{\mathrm {ex} }\right)\delta S+\left({\frac {\partial U}{\partial V}}+p_{\mathrm {ex} }\right)\delta V+\left({\frac {\partial U}{\partial N}}-\mu _{\mathrm {ex} }\right)\delta N=0}
および、2次変分について
1
2
(
∂
2
U
∂
S
2
δ
S
2
+
∂
2
U
∂
V
2
δ
V
2
+
∂
2
U
∂
N
2
δ
N
2
)
+
∂
2
U
∂
S
∂
V
δ
S
δ
V
+
∂
2
U
∂
S
∂
N
δ
S
δ
N
+
∂
2
U
∂
V
∂
N
δ
V
δ
N
>
0
{\displaystyle {\frac {1}{2}}\left({\frac {\partial ^{2}U}{\partial S^{2}}}\delta S^{2}+{\frac {\partial ^{2}U}{\partial V^{2}}}\delta V^{2}+{\frac {\partial ^{2}U}{\partial N^{2}}}\delta N^{2}\right)+{\frac {\partial ^{2}U}{\partial S\partial V}}\delta S\delta V+{\frac {\partial ^{2}U}{\partial S\partial N}}\delta S\delta N+{\frac {\partial ^{2}U}{\partial V\partial N}}\delta V\delta N>0}
である。
1次変分の条件から
系が熱を交換するとき(δS ≠0
∂
U
∂
S
=
T
=
T
ex
{\displaystyle {\frac {\partial U}{\partial S}}=T=T_{\text{ex}}}
系の体積が変化するとき(δV ≠0
∂
U
∂
V
=
−
p
=
−
p
ex
{\displaystyle {\frac {\partial U}{\partial V}}=-p=-p_{\text{ex}}}
系が物質を交換するとき(δN ≠0
∂
U
∂
N
=
μ
=
μ
ex
{\displaystyle {\frac {\partial U}{\partial N}}=\mu =\mu _{\text{ex}}}
などの平衡条件が得られる。
2次変分の条件から
∂
2
U
∂
S
2
=
(
∂
T
∂
S
)
V
=
T
C
V
≥
0
{\displaystyle {\frac {\partial ^{2}U}{\partial S^{2}}}=\left({\frac {\partial T}{\partial S}}\right)_{V}={\frac {T}{C_{V}}}\geq 0}
∂
2
U
∂
V
2
=
−
(
∂
p
∂
V
)
S
=
1
V
κ
S
≥
0
{\displaystyle {\frac {\partial ^{2}U}{\partial V^{2}}}=-\left({\frac {\partial p}{\partial V}}\right)_{S}={\frac {1}{V\kappa _{S}}}\geq 0}
∂
2
U
∂
S
2
∂
2
U
∂
V
2
−
(
∂
2
U
∂
S
∂
V
)
2
=
T
C
p
1
V
κ
S
=
T
C
V
1
V
κ
T
≥
0
{\displaystyle {\frac {\partial ^{2}U}{\partial S^{2}}}{\frac {\partial ^{2}U}{\partial V^{2}}}-\left({\frac {\partial ^{2}U}{\partial S\partial V}}\right)^{2}={\frac {T}{C_{p}}}{\frac {1}{V\kappa _{S}}}={\frac {T}{C_{V}}}{\frac {1}{V\kappa _{T}}}\geq 0}
などが得られる。
ここで、CV は定積熱容量 、Cp は定圧熱容量 、κS は断熱圧縮率 、κT は等温圧縮率 である。
C
p
>
C
V
>
0
,
κ
T
>
κ
S
>
0
{\displaystyle C_{p}>C_{V}>0,~\kappa _{T}>\kappa _{S}>0}
平衡状態の安定性から熱力学ポテンシャルは一般に凸関数 となる。
統計力学との関係 完全な熱力学関数は分配関数 と関係付けられる。巨視的な熱力学と微視的な統計力学 を結びつける関係である。
S
(
E
,
N
,
V
)
=
k
ln
W
(
E
,
N
,
V
)
{\displaystyle S(E,N,V)=k\ln W(E,N,V)}
F
(
β
,
N
,
V
)
=
−
1
β
ln
Z
(
β
,
N
,
V
)
{\displaystyle F(\beta ,N,V)=-{\frac {1}{\beta }}\ln Z(\beta ,N,V)}
J
(
β
,
μ
,
V
)
=
−
1
β
ln
Ξ
(
β
,
μ
,
V
)
{\displaystyle J(\beta ,\mu ,V)=-{\frac {1}{\beta }}\ln \Xi (\beta ,\mu ,V)}
ここで、β =1/kT 逆温度 である。k はボルツマン定数 である。
具体例 この節の
加筆 が望まれています。
(2020年12月 )
脚注
^ 田崎『熱力学』 ^ 佐々真一; 兵頭俊夫 編『熱力学入門』共立出版、2000年、76頁。ISBN 4-320-03347-7 。 ^ 例えば分極 P や磁化 M など。
^ 例えば分極 P に対応する外部電場 E や磁化 M に対応する外部磁場 H など。
^ a b c β =1/T α =μ /T
^ a b 久保『熱学・統計力学』 p.90
参考文献