「エチゾラム」の版間の差分
| 61行目: | 61行目: | ||
そして作用発現および持続が短時間(6時間以内)であるという特徴を持ち、服用後約3時間(食後30分経口)で最高血中濃度に到達する。 |
そして作用発現および持続が短時間(6時間以内)であるという特徴を持ち、服用後約3時間(食後30分経口)で最高血中濃度に到達する。 |
||
抗不安薬としては他のマイナートランキライザーと大同小異であるが、作用が強い分だけ連用後の退薬症状(いわゆる[[依存症|禁断症状]])が出やすい。すなわち、強い作用と持続が短いという特性から[[不眠症|不眠]]の際 |
抗不安薬としては他のマイナートランキライザーと大同小異であるが、作用が強い分だけ連用後の退薬症状(いわゆる[[依存症|禁断症状]])が出やすい。すなわち、強い作用と持続が短いという特性から[[不眠症|不眠]]の際に利用される睡眠導入剤の補助(単独での処方ではなく、例えば、[[トリアゾラム]]に追加されるなど)として利用される場面が多い。また筋弛緩作用も強いため、[[肩こり]]などの症状にも処方される場合がある。 |
||
== 適用 == |
== 適用 == |
||
2013年10月3日 (木) 10:33時点における版
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 投与経路 | 経口 |
| 薬物動態データ | |
| 生物学的利用能 | 93% |
| 代謝 | 肝臓 |
| 半減期 | 約6時間 |
| 排泄 | 腎臓 |
| 識別 | |
| CAS番号 | 40054-69-1 |
| ATCコード | N05BA19 (WHO) |
| PubChem | CID: 3307 |
| DrugBank | ? |
| KEGG | D01514 |
| 化学的データ | |
| 化学式 | C17H15ClN4S |
| 分子量 | 342.8 |
| エチゾラム | |
|---|---|
| 形状 | 白色または微黄色結晶 |
| 融点 | 145–149 °C |

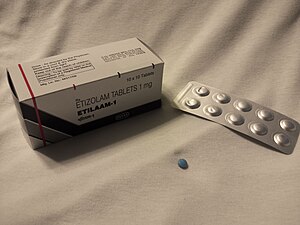
(小さいため写真では分かり難いが割線が入っている)
エチゾラム(etizolam)は、チエノジアゼピン系に属する抗不安薬(マイナートランキライザー)。睡眠導入剤として処方される事もある(後述)。エチゾラムは多くの後発医薬品が存在する。日本国内の商品名はデパス。
日本国外では、Depas、Sedekopan等の商品名で販売される。
化学名は 4-(2-Chlorophenyl)-2-ethyl-9-methyl-6H-thieno[3,2-f][1,2,4]triazolo[4,3-a][1,4]diazepine 。
作用機序

ベンゾジアゼピン作用機序と神経の活動電位
チエノジアゼピン系抗不安薬は、ベンゾジアゼピン系抗不安薬と同一の作用機序を持つ。すなわち、シナプス後細胞側に存在するGABAA受容体に結合することによりCl-イオンを透過させやすくし、神経細胞の膜電位を負の方向に過分極(活動電位の閾値に到達させる方向とは逆方向)させるので、神経細胞全体としては興奮が起こりにくくなり、結果神経活動全体に対して抑制的に働く。
GABAA受容体は3種類のサブユニットα、β、γが複数ずつ組み合わされて構成されたイオンチャネル共役型受容体であり、そのたんぱく質のモチーフは4回膜貫通型の膜たんぱく質型に分類される。そしてGABAA受容体の存在する組織の部位によってサブユニット構成が異なることが知られている。GABAがGABAA受容体に結合することでCl-イオンチャンネルが開くが、ベンゾジアゼピン結合部位はGABA結合部位とは異なりアロステリック的にGABAの作用を増強するように働く。また、ベンゾジアゼピン類はγサブユニットと関係が深いことが研究により判明している。
GABAA受容体は小脳などを含めた広く脳全体に分布しているが、特にベンゾジアゼピン類に感受性を持つGABAA受容体が多いのは視床下部および大脳辺縁系、特に扁桃核である。これらの部位においてチエノジアゼピン系抗不安薬もGABA作用を増強し神経伝達に対して抑制作用を示すことで、不安・緊張などの情動異常を改善する。それ故、中枢神経の他の部位が関与する機能、例えば高次脳機能等に対しては抑制作用が少ない。
また、ベンゾジアゼピン系抗不安薬と同様に、睡眠導入および筋弛緩作用も併せ持つ。そして、大量では呼吸抑制を引き起こす。
薬理
エチゾラムはジアゼパムに比べ、強い力価(重量あたりの薬理作用強度)を持つ。すなわち、薬理実験ではベンゾジアゼピンの5 - 6倍の作用を示し、1/4程度の量で作用が期待される。
そして作用発現および持続が短時間(6時間以内)であるという特徴を持ち、服用後約3時間(食後30分経口)で最高血中濃度に到達する。
抗不安薬としては他のマイナートランキライザーと大同小異であるが、作用が強い分だけ連用後の退薬症状(いわゆる禁断症状)が出やすい。すなわち、強い作用と持続が短いという特性から不眠の際に利用される睡眠導入剤の補助(単独での処方ではなく、例えば、トリアゾラムに追加されるなど)として利用される場面が多い。また筋弛緩作用も強いため、肩こりなどの症状にも処方される場合がある。
適用
- 神経症・心身症・うつ病・パニック障害および統合失調症等の影響による不安・緊張・睡眠障害および胃潰瘍
- 神経症における軽度のうつ・神経衰弱症状、心身症における軽度のうつ
- 頸椎症、腰痛症、筋収縮性頭痛における筋緊張
用量
- 神経症、うつ病
- 成人に1日3mgを3回に分けて、経口投与する。
- 心身症、頚椎症、腰痛症、筋収縮性頭痛
- 成人に1日1.5mgを3回に分けて、経口投与する。
- 睡眠障害
- 成人に1日1 - 3mgを就寝前に1回、経口投与する。
いずれの場合にも、年齢、症状により適宜増減する。体内に残存しやすい高齢者は1日1.5mgまでとする。
- 同効薬
- クロチアゼパム、ジアゼパム、クロルジアゼポキシド、クロキサゾラム、ニトラゼパム、エスタゾラム等
- 併用注意
- 中枢神経抑制剤 - 両薬剤が相加的に作用を発現する。
- MAO阻害剤 - 同剤は肝臓でのエチゾラム代謝を競争的に阻害するため、作用強度が増大したり持続時間の延長がみられることがある。
- フルボキサミン - 同剤は肝臓でのエチゾラム代謝を競争的に阻害するため、作用強度が増大したり持続時間の延長がみられることがある。
これらの薬剤と併用する場合は、投与量を適宜減量する必要がある。
物性
- 融点 146 - 149℃
- デパス及びそのジェネリック製品では、フィルムコート錠となっているが、腸溶錠ではない。エチゾラムは、pH4.0以下の酸性水溶液(胃液)では開環体へと変化し効力が減弱するが、アルカリ性の小腸に達すると再び閉環体に戻り、活性を持って小腸で吸収される。アルカリ水溶液中では37℃で4時間は安定である。
- 光分解性を有することが知られている。
一般的注意
眠気、注意力・集中力・反射運動能力等の低下が起こることがあるので、自動車や機器の操作運転は従事しない。自分の判断で勝手に服用を中止したりしない。アルコールとの併用は神経抑制作用とアルコールの酩酊作用を増強するため危険。
使用禁忌
慎重投与
- 心障害、肝障害、腎障害のある患者
- 脳に器質的障害のある患者(作用が強く現れる)
- 小児および高齢者
- 中等あるいは重篤な呼吸障害を持つ患者
副作用
- 精神神経系副作用
- ときに眠気、ふらつき、めまい、歩行失調、頭痛・頭重、言語障害、また、まれに不眠感、興奮、焦燥、振戦、眼症状(霧視、調節障害)が現れることがある。
- 統合失調症等の患者で逆に刺激興奮、錯乱等が現れることがある。
- 依存性
- 大量連用により、まれに薬物依存を生じることがある。
- また、大量投与または連用中における投与量の急激な減少ないし中止により、まれにけいれん発作、ときにせん妄、振戦、不眠、不安、幻覚、妄想等の禁断症状が現れることがある。
- 肝機能障害
- 黄疸あるいは血清中の酵素指標の上昇など肝機能障害を示すことがある。
- 長期間の使用では眼瞼痙攣[2]
また、以下の少数の副作用が報告されている。
- 呼吸抑制、炭酸ガスナルコーシス
- 呼吸抑制が現れることがある。中等あるいは重篤な呼吸障害を持つ患者では炭酸ガスナルコーシスが現れることがある。
- 悪性症候群
- 発熱、強度の筋強剛、嚥下困難、頻脈、血圧の変動、発汗、白血球の増加、血清CK(CPK)の上昇等、悪性症候群の症状が現れることがある。
- 横紋筋融解症
- 筋肉痛、脱力感、CK(CPK)値上昇、血中および尿中ミオグロビン上昇など横紋筋融解症が現れることがある。
- 間質性肺炎
- 発熱、咳嗽、呼吸困難、肺音の異常(捻髪音)等、間質性肺炎の症状が現れることがある。この薬剤に対するアレルギー反応が原因と考えられている。
- 遠心性環状紅斑 skin lesions [3]
耐性・依存・離脱
他のベンゾジアゼピンと同様、突然または急速な断薬によってリバウンド不眠などのベンゾジアゼピン離脱症候群が起こる。[4] まれに断薬時に悪性症候群を起こすケースがある。[5]
過剰摂取
エチゾラムは、ベンゾジアゼピン系の過剰摂取による自殺の例がある。エチゾラム過剰摂取が致命的であるというエビデンスが存在する[6]。
乱用
エチゾラムは乱用のポテンシャルがある薬物である。エチゾラムは霊長類での実験にて、バルビツール酸の作用に影響を与えることが示されている。[7]
WHOの薬物依存エキスパート委員会では、エチゾラムの乱用ポテンシャルと治療有用性について共に"High"との評価であった。[8]
ラット:経口LD50→♂3619.4mg/kg,♀3509.4mg/kg
マウス:経口LD50→♂4358.1mg/kg,♀4258.4mg/kg
と基本的には安全な薬である(体重60kg直接換算で半数致死量21万錠(1mg)~)と思われるが、ヒトにおいて5mg単回投与(誤投与)で植物状態例と死亡例があり、乱用は避け、慎重に使いたい。
商品名
| 商品名 | メーカー名 | 型式 | 成分量 | 識別コード | 備考 |
|---|---|---|---|---|---|
| デパス (先発品) |
田辺三菱製薬 | デパス細粒1% | 10mg/g | ||
| デパス錠0.5mg | 0.5mg | Y DP/0.5 | 白色、フィルムコート錠 | ||
| デパス錠1mg | 1.0mg | Y DP/1 | |||
| アロファルム | テイコクメディックス1) | アロファルム錠0.5 | 0.5mg | O.S A0.5 | 白色錠 |
| アロファルム錠1.0 | 1.0mg | O.S A1.0 | |||
| エチカーム | 東和薬品 | エチカーム錠0.5mg | 0.5mg | Tw.ET0.5 | 白色、フィルムコーティング錠 |
| エチカーム錠1mg | 1.0mg | Tw.ET1.0 | |||
| エチセダン | 共和薬品工業 | エチセダン錠0.5mg | 1.0mg | KW 091 0.5 | 白色 - 淡黄白色、フィルムコート錠 |
| エチセダン錠1mg | 1.0mg | KW 092 1 | |||
| エチゾラム | サンノーバ2) | エチゾラム0.5mg錠「EMEC」 | 0.5mg | EE04 | 白色、口腔内崩壊錠(素錠) |
| エチゾラム1.0mg | 1.0mg | ||||
| エチゾラン | 小林化工 | エチゾラン錠 | 0.5mg | KN 123 0.5mg | 白色、フィルムコート錠 |
| エチドラール | シオノケミカル | エチドラール細粒 | 10mg/g | ||
| エチドラール錠0.5mg | 0.5mg | ETD-0.5 | |||
| エチドラール錠1mg | 1.0mg | ETD-1 | |||
| カプセーフ | 大原薬品工業 | カプセーフ錠0.5mg | 0.5mg | 0.5:OH-51 | 白色、フィルムコート錠 |
| カプセーフ錠1mg | 1.0mg | ||||
| グペリース | ニプロジェネファ | グペリース錠 | 0.5mg | GP0.5:TP-110 | 白色、フィルムコート錠 |
| サイラゼパム | マルコ製薬 | サイラゼパム錠0.5 | 0.5mg | 11R | 白色、フィルムコート錠 |
| セデコパン | 長生堂製薬 | セデコパン細粒 | 10mg/g | 白色細粒剤 | |
| セデコパン錠0.5mg | 0.5mg | chSD | 白色、フィルムコート錠 | ||
| セデコパン錠1mg | 1.0mg | chSI | |||
| デゾラム | 大正薬品工業 | デゾラム錠0.5mg | 0.5mg | TYK 201 | 白色、フィルムコート錠 |
| デゾラム錠1mg | 1.0mg | TYK 202 | |||
| デムナット | 鶴原製薬 | デムナット錠0.5mg | 0.5mg | TSU430 | 白色、フィルムコート錠 |
| ノンネルブ | 日新製薬 | ノンネルブ錠0.5 | 0.5mg | NS 193 | 白色、フィルムコート錠 |
| パルギン | 藤永製薬3) | パルギン錠0.5mg | 0.5mg | PG0.5 | 白色、素錠 |
| パルギン錠1mg | 1.0mg | PG1 | |||
| メディピース | メディサ新薬4) | メディピース錠0.5 | 0.5mg | SW 037 SW-038 |
白色、フィルムコート錠 |
| メディピース錠1 | 1.0mg | ||||
| モーズン | 辰巳化学 | モーズン錠0.5mg | 0.5mg | Tu MZ-050 | 白色 - 微黄色、フィルムコーティング錠 |
| エチゾラム錠0.5mg「TCK」 | 0.5mg | ||||
| エチラーム (Etilaam) |
インタスファーマ | エチラーム錠0.5mg | 0.5mg | インドなどで流通 (日本語圏未流通)、青色、フィルムコート錠 | |
| エチラーム錠1mg | 1mg |
- 1)テイコクメディックスと太田製薬とは2005年10月に合併した
- 2)製造 サンノーバ 販売 エルメッド エーザイ
- 3)製造 藤永製薬 販売 三共
- 4)製造 メディサ新薬 販売 旭化成ファーマ
種類
- 錠剤:0.5, 1mgの錠剤
- 細粒:1%
日本での経緯
エチゾラムは旧・吉冨製薬(現・田辺三菱製薬)が開発し、商品名デパスとして1983年9月に承認され、1984年3月に発売された。多くの後発医薬品が存在し、日本国外でもDepas、Sedekopan等の商品名で販売されている(アメリカ合衆国、カナダでは未認可である)。
- 承認年月日 1983年9月21日
- 薬価基準収載日 1984年3月17日
関連項目
出典
- ^ Lopedota A, Cutrignelli A, Trapani A, et al. (May 2007). “Effects of different cyclodextrins on the morphology, loading and release properties of poly (DL-lactide-co-glycolide)-microparticles containing the hypnotic agent etizolam”. J Microencapsul 24 (3): 214?24. doi:10.1080/02652040601058152. PMID 17454433.
- ^ Wakakura M, Tsubouchi T, Inouye J (March 2004). “Etizolam and benzodiazepine induced blepharospasm”. J. Neurol. Neurosurg. Psychiatr. 75 (3): 506?7. doi:10.1136/jnnp.2003.019869. PMC 1738986. PMID 14966178.
- ^ Kuroda K, Yabunami H, Hisanaga Y (January 2002). “Etizolam-induced superficial erythema annulare centrifugum”. Clin. Exp. Dermatol. 27 (1): 34?6. doi:10.1046/j.0307-6938.2001.00943.x. PMID 11952667.
- ^ Hirase M, Ishida T, Kamei C (November 2008). “Rebound insomnia induced by abrupt withdrawal of hypnotics in sleep-disturbed rats”. Eur. J. Pharmacol. 597 (1-3): 46?50. doi:10.1016/j.ejphar.2008.08.024. PMID 18789918.
- ^ Kawajiri M, Ohyagi Y, Furuya H, et al. (February 2002). “[A patient with Parkinson's disease complicated by hypothyroidism who developed malignant syndrome after discontinuation of etizolam]” (Japanese). Rinsho Shinkeigaku 42 (2): 136?9. PMID 12424963.
- ^ Nakamae T, Shinozuka T, Sasaki C, et al. (November 2008). “Case report: Etizolam and its major metabolites in two unnatural death cases”. Forensic Sci. Int. 182 (1-3): e1?6. doi:10.1016/j.forsciint.2008.08.012. PMID 18976871.
- ^ Woolverton WL, Nader MA (December 1995). “Effects of several benzodiazepines, alone and in combination with flumazenil, in rhesus monkeys trained to discriminate pentobarbital from saline”. Psychopharmacology (Berl.) 122 (3): 230?6. doi:10.1007/BF02246544. PMID 8748392.
- ^ [[http://whqlibdoc.who.int/trs/WHO_TRS_787.pdf WHO Expert Committee on Drug Dependence 26th report]]
- 医薬品インタビューフォーム デパス錠・細粒
外部リンク
- 田辺三菱製薬株式会社 - デパス
