硫化鉛(II)
| 硫化鉛(II) | |
|---|---|
| |

| |
別称 Plumbous sulfide 方鉛鉱, Sulphuret of lead | |
| 識別情報 | |
| CAS登録番号 | 1314-87-0 |
| ChemSpider | 14135 |
| |
| 特性 | |
| 化学式 | PbS |
| モル質量 | 239.30 g/mol |
| 密度 | 7.60 g/cm3[1] |
| 融点 |
1118 °C, 1391 K, 2044 °F |
| 沸点 |
1281 °C, 1554 K, 2338 °F |
| 水への溶解度 | 2.6×10−11 kg/kg (計算値、pH7)[2] 8.6×10−7 kg/kg[3] |
| 溶解度平衡 Ksp | 9.04×10−29 |
| 屈折率 (nD) | 3.91 |
| 構造 | |
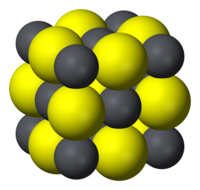
| 結晶構造 | 塩化ナトリウム型(立方晶), cF8 |
| 空間群 | Fm3m, No. 225 |
| 格子定数 (a, b, c) | a = 5.936 [4] Å |
| 配位構造 | 正八面体型 (Pb2+) 正八面体型 (S2−) |
| 熱化学 | |
| 標準生成熱 ΔfH |
–98.7 kJ/mol |
| 標準モルエントロピー S |
91.3 J/mol |
| 標準定圧モル比熱, Cp |
46.02 J/°C mol |
| 危険性 | |
| 安全データシート(外部リンク) | External MSDS |
| EU分類 | 生殖毒性 Repr. Cat. 1/3 有害 (Xn) 環境毒性 (N) |
| NFPA 704 | |
| Rフレーズ | R61, R20/22, R33, R62, R50/53 |
| Sフレーズ | S53, S45, S60, S61 |
| 引火点 | 不燃性 |
| 関連する物質 | |
| その他の陰イオン | 酸化鉛(II) セレン化鉛(II) テルル化鉛(II) |
| その他の陽イオン | 一硫化炭素 一硫化ケイ素 硫化ゲルマニウム(II) 硫化スズ(II) |
| 関連物質 | 硫化タリウム 硫化鉛(IV) 硫化ビスマス |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
硫化鉛(II)(りゅうかなまり に、英: lead(II) sulfide)は、化学式PbSをもつ無機化合物である。方鉛鉱とも呼ばれる基礎的な鉱物で、鉛の最も重要な化合物である。半導体として特殊用途に用いられる。
基本的性質・合成・関連物質[編集]
硫化水素または硫化物を鉛イオンの水溶液に加えると、黒色の沈殿として得られる。
この反応の平衡定数は、3×106 mol/Lである[5]。
無色または白色から黒色への劇的な色の変化を伴うこの反応は、定性無機分析に用いられていた。現在でも、硫化水素または硫化物の存在を検出する常法として、酢酸鉛試験紙がある。
関連するセレン化鉛(II)、テルル化鉛(II)と同様、半導体としての性質を示す[6]。また、もっとも古くから用いられてきた半導体でもある[7]。その他のIV-VI族半導体と異なり、塩化ナトリウム型の結晶構造を持つ。
鉛の主要鉱物として、化学変換に多大な努力がなされてきた。主なプロセスは精錬であり、生成した酸化物を還元して金属鉛を得る。
この二段階反応の理論的な化学反応式は以下の通りである[8]。
ナノ粒子[編集]
硫化鉛(II)を含むナノ粒子と量子ドットは詳細に研究されている[9]。 伝統的に、このような物質は、鉛の塩と、様々な硫化物イオン源を組み合わせて作られる[10][11]。 近年、硫化鉛(II)のナノ粒子は太陽電池に応用されつつある[12]。
安全性[編集]
硫化鉛(II)は非常に溶解性が低いため、ほとんど無害であるが、精錬における熱分解によって、危険な粉塵を生じる[13]。
硫化鉛(II)は溶解性が低く、血液のpHでは安定な物質であるため、鉛の化合物としては無害なほうであろう[14]。
炭酸鉛類を用いて硫化鉛(II)を合成する際には、大きな安全上のリスクがある。炭酸鉛は特に溶解性が高く、生理学的に好ましくない状態をもたらす。
応用[編集]
以前、硫化鉛(II)は黒色の顔料として用いられていたが、近年では古くから知られていた半導体としての特性が研究されている[15]。
赤外線センサー(光導電体)[編集]
硫化鉛(II)は赤外線センサーの素子として、もっとも古く、もっとも身近である。放射による素子の温度上昇に反応する熱センサーとは異なり、硫化鉛(II)は赤外線センサーとして、放射された光子に直接反応する。
硫化鉛(II)素子を用いて放射を検出する方法は二通りある。光子が硫化鉛(II)素子に当たるときに生じる微弱電流か、光子による素子の電気抵抗の変化が観測されるが、後者がよく用いられる。室温では、硫化鉛(II)は波長1-2.5 μmの放射に反応する。この波長領域は、短波長赤外線(SWIR)と呼ばれる赤外領域の短波長側に相当する。この波長は、非常に高温の物体のみが放射する。
液体窒素やペルティエ素子を用いて硫化鉛(II)素子を冷却すると、検出する波長領域はおよそ2-4 μmに変化する。この波長を放射する物体はいまだ数百°Cという高温のはずであるが、冷却されていないセンサーが検出する温度ほどは高くない。
同じ目的に用いられるその他の化合物には、アンチモン化インジウム (InSb) や テルル化カドミウム水銀 (HgCdTe)があり、より長波長の赤外線の検出については、これらの方がやや優れている。
高い誘電率のため、ケイ素、ゲルマニウム、InSb、HgCdTeと比較して、検出器としての動作は遅い。
天文学[編集]
金星の高度2.6 km以上の大気は、輝きのある物質で覆われている。この物質の成分は完全にはわかっていないが、地球で水の氷が雪として降るのと同様に、金星では硫化鉛(II)の結晶が雪として降っているという説がある(金星の雪を参照)。もしそうならば、他の惑星でこの物質が同定された初のケースになる。比較的考えにくいが、硫化ビスマスやテルルという説もある[16]。
脚注[編集]
- ^ Patnaik, Pradyot (2003). Handbook of Inorganic Chemical Compounds. McGraw-Hill. ISBN 0-07-049439-8 2009年6月6日閲覧。
- ^ W. Linke (1965). Solubilities. Inorganic and Metal-Organic Compounds. 2. Washington, D.C.: American Chemical Society. p. 1318
- ^ Ronald Eisler (2000). Handbook of Chemical Risk Assessment. CRC Press. ISBN 1-56670-506-1
- ^ http://www.springermaterials.com/docs/pdf/10681727_889.html
- ^ Lide, D. R., ed. (2005), CRC Handbook of Chemistry and Physics (86th ed.), Boca Raton (FL): CRC Press, ISBN 0-8493-0486-5
- ^ Vaughan, D. J.; Craig, J. R. (1978). Mineral Chemistry of Metal Sulfides. Cambridge: Cambridge University Press. ISBN 0-521-21489-0;
- ^ C.Michael Hogan. 2011. Sulfur. Encyclopedia of Earth, eds. A.Jorgensen and C.J.Cleveland, National Council for Science and the environment, Washington DC
- ^ Charles A. Sutherland; Edward F. Milner; Robert C. Kerby; Herbert Teindl; Albert Melin; Hermann M. Bolt (2005). Lead. in Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. doi:10.1002/14356007.a15_193.pub2
- ^ “The Quantum Mechanics of Larger Semiconductor Clusters ("Quantum Dots")”. Annual Review of Physical Chemistry 41 (1): 477–496. (1990-01-01). doi:10.1146/annurev.pc.41.100190.002401.
- ^ Zhou, H. S.; Honma, I.; Komiyama, H.; Haus, Joseph W. (2002-05-01). “Coated semiconductor nanoparticles; the cadmium sulfide/lead sulfide system's synthesis and properties” (英語). The Journal of Physical Chemistry 97 (4): 895–901. doi:10.1021/j100106a015.
- ^ Wang, Wenzhong; Liu, Yingkai; Zhan, Yongjie; Zheng, Changlin; Wang, Guanghou (2001-09-15). “A novel and simple one-step solid-state reaction for the synthesis of PbS nanoparticles in the presence of a suitable surfactant”. Materials Research Bulletin 36 (11): 1977–1984. doi:10.1016/S0025-5408(01)00678-X.
- ^ Lee, HyoJoong; Leventis, Henry C.; Moon, Soo-Jin; Chen, Peter; Ito, Seigo; Haque, Saif A.; Torres, Tomas; Nüesch, Frank et al. (2009-09-09). “PbS and CdS Quantum Dot-Sensitized Solid-State Solar Cells: "Old Concepts, New Results"” (英語). Advanced Functional Materials 19 (17): 2735–2742. doi:10.1002/adfm.200900081. ISSN 1616-3028.
- ^ Lead sulfide MSDS
- ^ Fritz Bischoff; L. C. Maxwell; Richard D. Evens; Franklin R. Nuzum (1928). “Studies on the Toxicity of Various Lead Compounds Given Intravenously”. Journal of Pharmacology and Experimental Therapeutics 34 (1): 85–109.
- ^ Putley, E H; Arthur, J B (1951). “Lead Sulphide – An Intrinsic Semiconductor”. Proceedings of the Physical Society. Series B 64: 616. doi:10.1088/0370-1301/64/7/110.
- ^ “'Heavy metal' snow on Venus is lead sulfide”. Washington University in St. Louis 2009年7月7日閲覧。
参考文献[編集]
- 山口勝也. "化学沈着法による PbS 光導電セルの試作." 照明学会雑誌 1965年 49巻 5号 p.247-253, doi:10.2150/jieij1917.49.5_247




