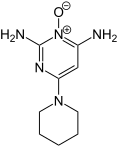
ミノキシジル
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 投与経路 | 経口/ 外用 |
| 薬物動態データ | |
| 代謝 | 肝臓 |
| 半減期 | 4.2 時間 |
| 排泄 | 腎臓 |
| 識別 | |
| CAS番号 | 38304-91-5 |
| ATCコード | C02DC01 (WHO) D11AX01 (WHO) |
| PubChem | CID: 4201 |
| DrugBank | APRD00086 |
| ChemSpider | 10438564 |
| KEGG | D00418 |
| 化学的データ | |
| 化学式 | C9H15N5O |
| 分子量 | 209.251 g/mol |
ミノキシジル(Minoxidil)とは血管拡張薬として開発された成分。後に発毛効果があるとされ発毛剤に転用され、日本以外ではRogaine(ロゲイン)の商品名で売られている。
日本では一般用医薬品として各社から市販されている。優れた発毛効果をもたらすことから「飲む育毛剤」とも呼ばれている[1]。
概要[編集]
1960年代にアップジョン社(現在のファイザー)が創製し、高血圧の経口薬として用いられていた。しかし後に髪を育成し、脱毛症を回復させる効果が発見され、1980年代にアップジョンがはげや脱毛症の治療用として2%のミノキシジル外用溶液を「Rogaine」として販売し始めた。内服薬としては副作用が発見されたため[2]頭部に塗布する液状の外用薬として売られている。なお、ファイザーは世界規模でOTC事業をジョンソン・エンド・ジョンソン(J&J)に売却したため、ロゲインの販売元はJ&J傘下のMcNEIL(マクニール社)に移管されている。
毛成長のメカニズムについては、毛乳頭細胞や毛母細胞の活性化と説明されているが詳細は未だわかっていない。同じはげ治療薬のフィナステリドは薬理作用が異なるので併用が可能であり、また併用した方がそれぞれを個別に使用するよりも発毛効果を高める事が出来る[要出典][3]。
日本国内においてもミノキシジルを成分とした内服薬であるLoniten(ロニテン)及びそのジェネリック医薬品を個人輸入の形で入手する事が可能だが、国内では未認可の薬である上、本来の用途は高血圧の治療のための血管拡張薬であり、服用する事により、重篤な症状を引き起こす可能性があるので注意が必要である。(脱毛の治療#ミノキシジル参照)発毛効果としては、外用薬よりも内服薬のほうが高いとされている。
日本[編集]
日本ではミノキシジル成分の医療用医薬品が未発売であるが、大正製薬が一般用医薬品として開発を行い1999年からミノキシジル成分1%の「リアップ」として発売開始された(ダイレクトOTC第1号製品)。同時期に国内で承認・上市した(医療用医薬品)バイアグラと共に生活改善薬として人気を博し、発売当初は品薄状態が続いた。
2005年には女性用の「リアップレディ」も発売され、2009年にはミノキシジルを5%配合した「リアップX5」が発売された。また2017年にはミノキシジル5%に加え、皮脂の分泌、酸化を抑え、頭皮の炎症を抑える効果がある成分(ピリドキシン塩酸塩、トコフェロール酢酸エステル、l-メントール)を配合した「リアップX5プラスローション」が発売された。なお、「リアップ」発売前から現在まで「リアップ」よりも主成分が濃厚で廉価である理由で「ロゲイン」の個人輸入も多く行われてきた。
2018年には後発医薬品が解禁され、他社も男性用のミノキシジル5%製剤に参入するようになり、同年8月にアンファーから「スカルプD メディカルミノキ5」[4]が、同年11月にはロート製薬から「リグロEX5」[5]、東和薬品から「ミノアップ」[6]がそれぞれ発売された。
副作用[編集]
脱毛に対抗する薬なので、最も一般的な副作用は頭皮の痒みである。ミノキシジルやロゲインなどの外用薬に含まれる基剤成分・プロピレングリコールに対するアレルギー反応がしばしば見られる。多量のミノキシジルは低血圧の原因となる可能性がある。日焼けした頭皮に使用する場合に見られがちであるが、ワセリンやトレチノインと併用すると薬剤の過剰な吸収が起こりえることが知られている。
ミノキシジルの使用中は脱毛を止められるが、使用をやめると再び起こり始める。また、成分が母乳中に移行するため、「リアップ」シリーズでは授乳する乳児がいる場合での使用は禁忌である。
なお、ミノキシジルを使用すると初期脱毛が起こるケースがある。初期脱毛はヘアサイクルが休止期から成長期に移行する際に起こるもので、あくまで一時的な症状である。一般的には1〜2ヶ月で症状が収まるため、重篤な副作用として捉える必要はない[7]。
あまり一般的ではないが、他の副作用には以下のようなものがある(「リアップ」の添付文書には具体的な症例を提示しつつ異変を感じたら薬剤師・医師に相談するよう促す文章となっている。)。
ニキビを除き、上記の症状は薬剤の使いすぎの目安になるとされるが、そうでなくても発症する可能性は有るので発症した場合は即ちに医師の診断を受ける事が強く薦められる。
重篤な副作用[編集]
「ロゲイン」の開発段階で3名、市販化された「リアップ」の使用中に3名(1999年末の時点)が薬品との因果関係は不明としながらも循環器疾患で死亡しており、後者に関しては2003年に長妻昭衆議院議員が質問主意書を提出し、同年9月に政府・厚生労働省からの答弁書で明らかになるまで販売元の大正製薬は公表しなかった。さらに1999年の発売当初から2003年までに循環器系の副作用が500例寄せられている事も同答弁書で明らかにされた。
「ロゲイン」の副作用で死者が出た事が「リアップ」発売前からワイドショーやスポーツ紙を中心に報道されていたこともあり、「いきなり誰でも買えるOTC(大衆薬)で発売するのは危険」とする医師・薬剤師・業界関係者などの識者は多かった。また、「リアップ」は購入時に薬剤師へ相談する必要があるが、大正製薬への服用相談も多く寄せられていた。大正製薬はニュースリリースを発表[8]すると共に購入時の既往症などのチェックを強化するよう販売店に指導した。その後、2009年の改正薬事法施行により第一類医薬品に区分されたため、法規制が強化された。2018年以降に順次発売されている「リアップ」以外の製品も同様である。
脚注・出典[編集]
- ^ “【医師監修】飲む育毛剤(ミノキシジル)の効果と副作用 | AGAメディカルケアクリニック|オフィシャル”. 2022年5月20日閲覧。
- ^ 大人の科学Vol.30 92ページ 「ミノキシジル」は、AGA治療向けの内服薬として開発が行われていた。しかし、イヌを使った動物実験の結果、心臓破裂で死亡した例があり、内服薬としての開発は中止された。
- ^ http://www.hairmedical.com/propecia/[出典無効]
- ^ 『スカルプDのアンファーから、第1類医薬品の"発毛剤"登場! 発毛成分「ミノキシジル」5%配合の『スカルプD メディカルミノキ5』』(プレスリリース)アンファー株式会社、2018年8月6日。2018年11月23日閲覧。
- ^ 『ロート製薬から男性用発毛剤が新発売「ミノキシジル」国内最大濃度5%配合『リグロEX5』』(プレスリリース)ロート製薬株式会社、2018年11月1日。2018年11月23日閲覧。
- ^ “【新製品】ミノキシジル5%配合の発毛剤を21日に新発売 東和薬品”. 薬事日報 (2018年11月19日). 2018年11月23日閲覧。
- ^ “ミノキシジルの【効果と副作用】初期脱毛は怖い?内服薬と液体の効き目の違い、飲み方も解説”. MOTEO. 2022年5月20日閲覧。
- ^ http://www.taisho.co.jp/company/release/2003/03_0927-j.htm
