周期律
周期律(しゅうきりつ、英: periodic law)は、元素を原子番号順に配列すると元素の物理的、化学的性質が一定の周期性で変化することである。これにより元素がSブロック元素、Pブロック元素、Dブロック元素、Fブロック元素、Gブロック元素…に分類される。また、周期律に従い元素を配列した表が周期表である。
歴史[編集]
三つ組元素[編集]
現在では周期表は原子番号順によって配列されているが、発見当初は原子量によって配列していた。ごく一部の例外を除いて、元素の原子番号が増加するにつれて原子量も増加するため、原子量順に元素を配列することによってもほぼ同じように周期律が再現される。
最初に原子量と元素の性質の間に関係があることに気が付いたのはヨハン・デーベライナーであるとされている。デーベライナーは元素の中に性質の良く似たものが3つ存在し、それがほぼ等間隔の原子量で並んでいることに気が付いた。例えば
- カルシウム(原子量 40.1) - ストロンチウム(原子量 87.6) - バリウム(原子量 137.3)
- 硫黄(原子量 32.1) - セレン(原子量 79.0) - テルル(原子量 127.6)
- 塩素(原子量 35.5) - 臭素(原子量 79.9) - ヨウ素(原子量 126.9)
のような組み合わせである。デーベライナーは1829年にこれを「三つ組元素(triad)」と呼ぶことを提唱した。
デーベライナーの時代にはまだ原子や分子といった概念が定着していなかったため、異なる原子同士の原子量を比較するのは困難であった。それは、物質の組成式をどう考えるかが人によって異なっており、そのため原子量も提案する人によって値がまちまちだったためである。
発展[編集]
この事態を打開したのがスタニズラオ・カニッツァーロである。カニッツァーロは1858年にアボガドロの仮説を受け入れれば、同体積の気体に含まれるある元素の質量を様々な気体で求めて、その最大公約数から原子量が一意に決定できることを示した。
また気化できない金属元素についてはデュロン=プティの法則から、ある一定の熱容量を持つ固体に含まれるある元素の質量を様々な固体で求めて、その最大公約数から原子量が一意に決定できることを示した。これにより原子量を元素同士で比較できるようになった。
ベギエ・ド・シャンクルトワは1862年に当時知られていた塩素までの元素の原子量に着目すると、原子量 16ごとに似た性質の元素が現れることに気が付いた。ド・シャンクルトワはこれをらせん状の図に表現して「地のらせん」と呼んだ。
また、ジョン・ニューランズは1863年に短周期周期表を作成し、原子量順に元素を並べると8個ごとに似た性質の元素が現れることに気が付いた。そしてこれを1865年に「オクターブの法則」として発表した。
1869年にはドミトリ・メンデレーエフが短周期周期表を作成し発表した。メンデレーエフは単純に原子量順に並べるだけでなく、性質が良く類似する元素がまとまるようにした。性質が類似しない元素が入ってしまう場合には、そこに未発見の元素があるものと考えて空欄とし、その持つべき性質を示した。後にこの空欄を埋めるような元素が次々に発見されていったため、メンデレーエフの周期表は大きな信頼を得ることになった。
ロタール・マイヤーは1864年に28の元素をそれらがとる原子価ごとに分類した表を作って書籍の中で発表した。その後、マイヤーはこの表の拡張を行なっていき、ほぼメンデレーエフと同じ周期表を作成していたが発表はしなかった。発表はメンデレーエフより遅れて1870年に行なわれたため、メンデレーエフの影に隠れる形になってしまった。また元素を原子量順に並べると原子容が周期的に変化することを発見した。
完成[編集]
未発見の元素が発見されていき、周期表の空欄が埋まってくると、原子量順に並べるのでは不具合があることが分かってきた。例えばアルゴン(原子量 40.0)はその性質から明らかに希ガスに分類され、カリウム(原子量 39.1)はアルカリ金属に分類される。しかし、単純に原子量順に並べるとカリウムが希ガスに、アルゴンがアルカリ金属になってしまう。また、コバルト(原子量 58.9)とニッケル(原子量 58.7)では原子量の差がほとんど無く、遷移金属であるため性質も似ており周期表上の位置がはっきりと確定できない。
その後、原子の内部構造が明らかにされることで、周期表は原子量順ではなく原子番号順、すなわち陽子数順に並べるのが合理的であることが明らかとなってきた。そして1913年にヘンリー・モーズレイにより特性X線から原子番号を決定する方法が発見されたことにより、すべての元素の周期表上の位置を確定することが可能になった。
なぜ周期律が成立するか[編集]
電子構造と反応性[編集]
原子の内部構造は原子核と電子からなるが、他の原子と結合を形成したり反応したりするときには、電子が重要な役割を果たす。そして原子の中の電子はその性質は均一ではなく階層構造を形成している(記事 電子配置に詳しい)。すなわち原子の中の電子は電子殻と呼ばれるグループを形成している。
そもそも電子殻が構成されるのは、電子が量子力学に従う粒子であることが原因である。電子の持つエネルギーの値は階段状の不連続な値をとり、エネルギーの高い電子ほど原子核より遠い位置に存在する。言い換えると、エネルギーの状態が似通った電子が集まって電子殻が構成される。そして電子殻はエネルギーの低いものほど内側に、高いものほど外側に存在する。中でももっともエネルギーの高い、最外殻に存在する電子の一群を価電子と言い、他の原子と結合を形成するときの主役となる。そのため、原子の中で価電子の配置の仕方は元素の性質に直結している。価電子の配置の仕方が同じようであれば、同じような性質を示すことになるのである。
また、価電子よりも内側の電子殻に存在する電子は、よりエネルギーの高い価電子のすべてが他の原子と相互作用してからでないと結合や反応に関与しない。従って、最外殻よりも内側の電子殻は化学的に不活性な状態であり、閉殻と呼ばれる。
さて、さきほど電子のエネルギーは不連続な値をとり、その値の大小で広がり方が大きくも小さくもなると説明したが、エネルギーの値で区別される電子の状態を軌道と呼ぶ。すなわち、電子殻は1つあるいは複数の軌道から構成されている。ある原子は電気的に中性な状態ではその原子番号と同じだけの数の電子を含む。軌道には数字とアルファベットの組み合わせからなる以下に示すような名前が付いている。
- K殻 — 1s
- L殻 — 2s 2p
- M殻 — 3s 3p 3d
- N殻 — 4s 4p 4d 4f
- O殻 — 5s 5p 5d 5f 5g
以降も同様に続く。そしてs軌道は1つ、p軌道は3つ、d軌道は5つ、f軌道は7つのエネルギーの等しい軌道からなる。パウリの排他原理のため、1つの軌道は2つまでの電子しか占めることができない。すなわちs軌道には最大2つ、p軌道には最大6つ、d軌道には最大10個、f軌道には最大14個までの電子が入ることができる。そして電子はエネルギーの最も低い軌道から順に占有していく。
各軌道のエネルギーの高さは低い方からおおまかには次のような順番になっている。
- 1s | 2s 2p | 3s 3p | 4s 3d 4p | 5s 4d 5p | 6s 4f 5d 6p | 7s 5f 6d 7p | …
ここで区切り(|)の位置は比較的エネルギーの高さに大きな差がある位置を示す。ここに示したように1~3つ目までの区切りまでは区切りの中は同じ電子殻の軌道しか存在しない。しかし第4と第5の区切りでは1つ下の電子殻の軌道が含まれる。そして、第6と第7の区切りでは1つ下と2つ下の電子殻の軌道が含まれる。実はこの区切りが周期表の周期を表している。そして、周期表では第4周期で初めて遷移元素が現れ第6周期と第7周期でランタノイド系列とアクチノイド系列とが現れる。遷移元素やランタノイド系列の性質とこの軌道の構成との間には密接なつながりがある。
短周期と長周期[編集]
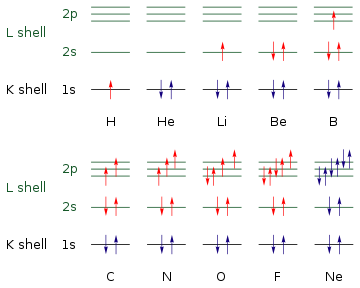
まず最初に水素(原子番号 1)では1s軌道に1つだけ電子が入る。次にヘリウム(原子番号 2)では1s軌道に2つの電子が入る。するとここでK殻が閉殻となる。閉殻した原子は価電子が存在しないため、結合を作ったり反応したりする能力に乏しく安定である。この性質を持つのが希ガス元素である。
次にリチウムでは2s軌道に1つ電子が入る。リチウムは1価の陽イオンになりやすいなど、1s軌道に電子が1つだけ入っている水素と類似した性質を示す。次にベリリウムでは2s軌道に2つ電子が入る。ただしベリリウムではL殻が閉殻ではない、すなわち価電子を2つ持つため、ヘリウムとはかなり性質が異なっている。続いてホウ素からネオンまでは2p軌道に1つずつ、電子が入っていく。ネオンまでいくとL殻は閉殻となる。このリチウムからネオンまでの8個の元素によって作られる1つの周期は短周期と呼ばれる。
次にナトリウムからアルゴンまでは同じように3s軌道と3p軌道に電子が入っていくことになる。そしてこれらの元素は、リチウムからネオンまでの元素の中で同じような価電子を持つ元素と類似した性質を持つことになる。例えばケイ素は価電子として3s軌道に2つ、3p軌道に2つの電子を持ち、これは2s軌道に2つ、2p軌道に2つの価電子を持つ炭素と相似であり、元素の性質も類似する。こうして元素の族ができ、周期が再現される。
カリウムとカルシウムは4s軌道の電子が価電子となるため、前の周期のナトリウムとマグネシウムに対応する。しかし、スカンジウムでは3d軌道に電子が入る。価電子の数としては3つであり、これはアルミニウムと対応し、性質の類似する部分もある(例えば酸化数として+III価をとるなど)。だがアルミニウムの価電子はp軌道のものであるので、価電子の配置としては相似ではなく、性質の異なる部分も多い。このため以前はスカンジウムとアルミニウムは同じ3族とし、その中でアルミニウムは3A亜族、スカンジウムは3B亜族とする扱いがなされていた。しかし、現在では別の族として扱うことになっている(スカンジウムは3族、アルミニウムは13族)。
亜鉛までは3d軌道が占有されていく。ガリウムになると次に4p軌道が占有される。ガリウムでは価電子は4s軌道の電子2つ、3d軌道の電子10個、4p軌道の電子1つということになるが、3d軌道の電子は完全に占有されてしまうとエネルギーが低下し価電子としての働きが弱くなる性質がある。そのためガリウムの価電子の配置は実質的にアルミニウムと相似と考えて良く、同じ族に入ることになる。そして順に4p軌道が占有されていき、クリプトンで再び閉殻となる。カリウムからクリプトンまでの18個の元素によって作られる1つの周期は長周期と呼ばれる。
ルビジウムからキセノンまでは前の周期と同じように5s軌道、4d軌道、5p軌道に電子が入っていき、同じような周期が再現される。
次の周期では4f軌道が占有されていく部分がある。この部分はランタノイド元素として区別されている。f軌道の性質もd軌道と類似しており、完全に占有されてしまうと価電子としての働きが弱くなる。そのため、4f軌道が占有されると次の5d軌道が占有されていくの部分の元素は前の周期の4d軌道が占有されていく部分の元素と類似する性質を示す。
