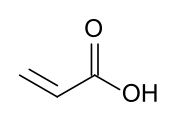
アクリル酸
| アクリル酸[1] | |
|---|---|
| |

| |
別称
| |
| 識別情報 | |
| CAS登録番号 | 79-10-7 |
| PubChem | 6581 |
| ChemSpider | 6333 |
| UNII | J94PBK7X8S |
| EC番号 | 201-177-9 |
| DrugBank | DB02579 |
| KEGG | D03397 |
| ChEBI | |
| ChEMBL | CHEMBL1213529 |
| RTECS番号 | AS4375000 |
| バイルシュタイン | 635743 |
| Gmelin参照 | 1817 |
| |
| |
| 特性 | |
| 化学式 | C3H4O2 |
| モル質量 | 72.06 g mol−1 |
| 外観 | 無色透明の液体 |
| 匂い | 刺激臭[3] |
| 密度 | 1.051 g/mL |
| 融点 |
14 °C, 287 K, 57 °F |
| 沸点 |
141 °C, 414 K, 286 °F |
| 水への溶解度 | 混和 |
| log POW | 0.28[4] |
| 蒸気圧 | 3 mmHg[3] |
| 酸解離定数 pKa | 4.25 (H2O)[5] |
| 粘度 | 1.3 cP at 20 °C (68 °F) |
| 危険性 | |
| 安全データシート(外部リンク) | MSDS |
| GHSピクトグラム |     
|
| GHSシグナルワード | 危険(DANGER) |
| Hフレーズ | H226, H302, H312, H314, H332, H400 |
| Pフレーズ | P210, P233, P240, P241, P242, P243, P260, P261, P264, P270, P271, P273, P280, P301+312 |
| NFPA 704 | |
| 引火点 | 68 °C (154 °F; 341 K) |
| 発火点 | 429 °C (804 °F; 702 K) |
| 爆発限界 | 2.4–8.02%[3] |
| 許容曝露限界 | 無し[3] |
| 関連する物質 | |
| その他の陰イオン | アクリレート |
| 関連するカルボン酸 | 酢酸 プロピオン酸 乳酸 3-ヒドロキシプロピオン酸 マロン酸 酪酸 クロトン酸 |
| 関連物質 | アリルアルコール プロピオンアルデヒド アクロレイン アクリル酸メチル |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
アクリル酸(アクリルさん、英: acrylic acid)は、化学式が CH2=CHCOOH で表される有機化合物である。最も単純な不飽和カルボン酸で、カルボキシ基に直接ビニル基が結合している。IUPAC命名法では、2-プロペン酸(2-propenoic acid)と表される。年間で100万トン以上製造されている[6]。
融点 12 °C、沸点 141.6 °Cの無色透明の液体で、特有の刺激臭を有する。CAS登録番号は[79-10-7]。酸解離定数(pKa)は4.25、粘度は1.3 mPa s(20 °C)。
工業的製法[編集]
アクリル酸の工業的な合成法は、プロピレンの二段階酸化である。プロピレンを金属触媒存在下に酸素で酸化してアクロレインとし、さらにもう一段階の酸化によりアクリル酸とする。一段目の酸化反応は、触媒表面におけるプロピレンのアリル位水素の引き抜きと格子酸素の挿入等を経て、アクロレインが生成して完了するとされ、触媒は Mo-Bi-Fe に各種金属が添加された複合金属酸化物が用いられている。二段目の酸化反応は、アクロレインのアルデヒド基からの水素引き抜きと酸素挿入によるアクリル酸への転換反応であり、触媒は Mo-V に各種金属が添加された複合金属酸化物が用いられている[7]。両者の酸化反応は最適な条件が異なるため別々の反応器で行われ、また冷却を容易にするため触媒を詰めた多数の管を集合させた反応器形状にするとともに、発熱抑制および爆発反応回避のために反応ガス中に水蒸気を添加して行われる[7]。過去にはさまざまな合成プロセスが存在したが、原料・コストの両面からスタンダード・オイルの後継会社であるスタンダード・オイル・オブ・オハイオ(ソハイオ、SOHIO)社が開発した、アンモ酸化に代表される金属酸化物触媒による上記のプロセスがほとんどを占めるようになった[7]。
利用[編集]
アクリル酸は適当な重合開始剤、あるいは酸素などの作用により容易に重合し、ポリアクリル酸(PAA)を与える。この重合体はカルボキシル基を多数持つために非常に親水性が高い。さらに架橋を加えて網目状としたポリマーは、ナトリウム塩の形とすると高吸水性ゲルとして優れた性能を示すことから、紙おむつ用などに用いられる。
アクリル酸をメチルエステルとしたアクリル酸メチル(methyl acrylate, MA)も、ポリアクリル酸メチル(PMA)などのポリマーの原料として重要である。
安全性[編集]
毒物及び劇物取締法により劇物に指定されている[8]。また消防法による第4類危険物 第2石油類に該当する[9]。
出典[編集]
- ^ Merck Index, 11th Edition, 124.
- ^ a b International Union of Pure and Applied Chemistry (2014). Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013. The Royal Society of Chemistry. pp. 746. doi:10.1039/9781849733069. ISBN 978-0-85404-182-4
- ^ a b c d NIOSH Pocket Guide to Chemical Hazards 0013
- ^ “Acrylic acid_msds”. 2024年4月23日閲覧。
- ^ Dippy, J. F. J.; Hughes, S. R. C.; Rozanski, A. (1959). “The dissociation constants of some symmetrically disubstituted succinic acids”. Journal of the Chemical Society: 2492–2498. doi:10.1039/JR9590002492.
- ^ Ohara, Takashi; Sato, Takahisa; Shimizu, Noboru; Prescher, Günter; Schwind, Helmut; Weiberg, Otto; Marten, Klaus; Greim, Helmut (2005), "Acrylic Acid and Derivatives", Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a01_161.pub2。
- ^ a b c “アクリル酸製造触媒の開発史”. 2022年6月22日閲覧。
- ^ 毒物及び劇物指定令 昭和四十年一月四日 政令第二号 第二条 一の四
- ^ 法規情報 (東京化成工業株式会社)

