塩素酸カリウム
| 塩素酸カリウム | |
|---|---|
| |

| |
別称 塩素(V)酸カリウム | |
| 識別情報 | |
| CAS登録番号 | 3811-04-9 |
| EC番号 | 223-289-7 |
| 国連/北米番号 | 1485 |
| RTECS番号 | FO0350000 |
| 特性 | |
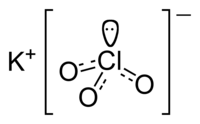
| 化学式 | KClO3 |
| モル質量 | 122.55 g/mol |
| 外観 | 白色の結晶粉末 |
| 密度 | 2.32 g/cm3, 固体 |
| 融点 |
356 °C |
| 沸点 |
~400 °C (分解) |
| 水への溶解度 | 7.3 g/100 ml (20 °C) |
| 熱化学 | |
| 標準生成熱 ΔfH |
−397.73 kJ mol−1[1] |
| 標準モルエントロピー S |
141.3 J mol−1K−1 |
| 標準定圧モル比熱, Cp |
100.25 J mol−1K−1 |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 0548 |
| EU分類 | 酸化剤(O) 有害(Xn) 環境への危険性(N) |
| EU Index | 017-004-00-3 |
| NFPA 704 | |
| Rフレーズ | R9, R22, R51/53 |
| Sフレーズ | (S2), S13, S16, S27, S61 |
| 引火点 | なし |
| 関連する物質 | |
| その他の陰イオン | 臭素酸カリウム ヨウ素酸カリウム |
| その他の陽イオン | 塩素酸アンモニウム 塩素酸ナトリウム 塩素酸バリウム |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
塩素酸カリウム(えんそさんカリウム、potassium chlorate)は化学式 KClO3 と表される、カリウムの塩素酸塩。塩剥(えんぼつ、えんぽつ)ともいう。CAS登録番号は [3811-04-9]。1786年に、パートレットにより合成された。
性質
- 密度 2.326 g/cm3、融点は 356 ℃ で、無色の光沢をもつ単斜板状結晶[2]。
- 吸湿性はない。
- 水に溶けアルコールにもいくぶん溶ける。
- 中性およびアルカリ性溶液では酸化作用を示すことは少ないが、酸性にすると強い酸化剤となる。その標準酸化還元電位は以下の通りである。
- ClO3−(aq)+ 6 H+(aq) + 6 e− = Cl−(aq) + 3 H2O, E°= 1.45 V
生成方法
塩化カリウム水溶液を熱時電解してつくられる。熱すると 400 ℃で分解して過塩素酸カリウムと塩化カリウムになる。
さらに加熱すれば、酸素を放ってすべてが塩化カリウムとなる。この反応は金属酸化物、とくに二酸化マンガン MnO2 を加えると促進され、70 ℃ ぐらいで酸素を発生しはじめるので、実験室などで酸素を得るために利用される。ただし、有機物・硫黄・炭素などが混ざると爆発することがあるので、注意を要する。
用途
酸化剤としてマッチ・花火・爆弾などの原料となり、漂白剤・染料・医薬品などの製造にも用いられる。長期間保存したものは亜塩素酸カリウムを含み、乾燥状態では有機物・リン・硫黄などの可燃性物質と接触しただけでも爆発することがある。また新しいものでも摩擦・衝撃などに鋭敏で、爆発事故をおこしやすく、濃硫酸・濃硝酸に触れても爆発しやすい。混合爆薬として用いられることもある。
危険物取扱および関連法規
日本国内では消防法により第1類危険物(酸化性固体)、毒物及び劇物取締法により劇物と規定される。


