ヘック反応
ヘック反応(ヘックはんのう、Heck reaction)あるいは溝呂木・ヘック反応(みぞろきヘックはんのう、Mizoroki-Heck reaction)は、パラジウム錯体を触媒として塩基存在下、ハロゲン化アリールまたはハロゲン化アルケニルでアルケンの水素を置換する反応である[1][2]。反応名は、本反応の発見者である溝呂木勉およびリチャード・ヘックに因む。2010年、ヘックはこの反応の発見および開発の功績により、ノーベル化学賞を授与された。
 |
| ヘック反応一般式 |
|---|
ヘック反応はパラジウム触媒存在下で行われる。ハロゲン化物 (I, Br, Cl[3]) あるいはトリフラートは、アリル、ベンジル、ビニル化合物が用いられる。アルケンは、少なくとも一つの水素原子を有し、電子不足であるアクリラート、エステル、アクリロニトリル等のオレフィンが用いられる。触媒としては、テトラキス(トリフェニルホスフィン)パラジウム(0)、塩化パラジウム(II)、酢酸パラジウム(II)、配位子としてはトリフェニルホスフィンやBINAP、塩基としてはトリエチルアミン、炭酸カリウム、酢酸ナトリウム等が使用される。
例:ヨードベンゼンを酢酸パラジウムを触媒としてアクリル酸メチルと反応させると、アクリル酸メチルのβ位の水素がフェニル基で置換されてケイ皮酸メチルが生成する。
歴史[編集]
1971年に溝呂木勉ら、1972年にリチャード・ヘックらによって独立に報告された。 溝呂木らの論文がややマイナーな論文誌Bull. Chem. Soc. Japan(日本化学会欧文誌)に掲載されたのに対し、ヘックらの論文はメジャーな論文誌J. Org. Chem.(アメリカ化学会発行)に掲載されたことからヘックの名が有名となり単にヘック反応と呼ばれることが多い。 なおヘックらの論文には溝呂木らの論文が引用されている。
1971年、溝呂木らは、メタノール中、120℃(オートクレーブ)、塩基として酢酸カリウム、触媒として塩化パラジウムを用いた、ヨードベンゼンとスチレンのカップリングによるスチルベンの生成を報告した[1]。これは、先行する寺西ら(1969年[7])やヘックら(1969年[8])によって報告された、化学量論量の2価パラジウム触媒を用いる有機水銀ハロゲン化物 (ArHgCl) とアルケンのカップリング反応を発展させたものである。
 |
| 溝呂木 1971年 |
|---|
1972年のヘックの論文では、溝呂木の論文に言及した上で、「独立に発見された」内容について詳細に述べられている[2]。ヘックの反応条件は、触媒(酢酸パラジウム)、塩基(嵩高いアミン)、無溶媒である点が異っている。
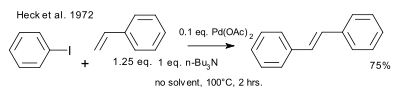 |
| Heck 1972年 |
|---|
これらの反応では、活性種である0価パラジウムは、パラジウムのアルケンに対する配位で生じている。
1974年、ヘックはこの反応にホスフィン配位子を導入した[9]。
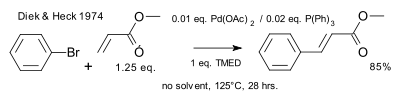 |
| Heck 1974年 ホスフィン |
|---|
反応機構[編集]
パラジウム錯体は通常は0価のものが活性であり0価-2価のサイクルで反応していると考えられている。 酢酸パラジウムなど2価のパラジウムを触媒として使用する場合にはトリフェニルホスフィンなどのホスフィン配位子を添加する。 このホスフィン配位子は酢酸パラジウムを還元して活性種の0価のパラジウム種へと変える還元剤の役割も果たす[10]。 しかし反応系によっては2価→4価のサイクルで反応しているとされるものもある
反応例ではまず、酢酸パラジウム(II)はトリフェニルホスフィンにより還元され、ジトリフェニルホスフィンパラジウム(0) (1) となり、トリフェニルホスフィンは酸化されトリフェニルホスフィンオキシドとなる。 ステップAは酸化的付加であり、ハロゲン化アリール(あるいはハロゲン化アルケニル)パラジウム錯体に酸化的付加し、有機パラジウム化合物が生成する。パラジウムは次にアルケン (3) とπ複合体を形成し、ステップBにおいて、有機パラジウムが反応相手の二重結合に対してシン付加する。ねじれひずみを解消するためにトランス異性体に回転した後、ステップCにおいて、パラジウムはそれが結合している炭素の隣りの炭素上の水素とともにシン-β脱離してパラジウム-アルケンπ複合体 (5) を与える。最後に、パラジウム錯体からハロゲン化水素が還元的脱離して触媒が再生される。通常はここで副生するハロゲン化水素をトラップするために3級アミンや炭酸カリウムのような塩基が添加される。反応において炭酸イオンは化学量論量消費され、パラジウムは触媒量でよい。同様のパラジウム触媒サイクルはワッカー酸化においても見られる。
 |
| 反応機構 |
|---|
反応サイクルはビニル化合物に限定されず、薗頭・萩原カップリングではアルキン、鈴木・宮浦カップリングではアリルホウ酸、右田・小杉・スティルカップリングではアリルスズ化合物が用いられる。 また、根岸カップリングではアリルハライドと有機亜鉛化合物のカップリングに、パラジウムと同様に第10族元素であるニッケルが用いられる。白金も第10族元素であるが、炭素と強い結合を形成するため、上記のような反応における触媒活性を示さない。
ハロゲン化アリールの代わりにフェノールトリフラートやジアゾニウム塩、カルボン酸ハロゲン化物が用いられることもある。 カルボン酸ハロゲン化物を使用した場合には酸化的付加の後、脱一酸化炭素が起こってハロゲン化アリールを使用した場合と同じパラジウム種に変換される。 付加を受けるアルケンを1,3-ジエンとすると付加後に生成するのはβ脱離が起こりにくいπ-アリルパラジウムとなるので、パラジウムの結合位置にさらに他の求核剤を反応させることができる(#バリエーションを参照)。
立体選択性[編集]
本カップリング反応は、酸化的付加後、ハロゲン化パラジウム基と嵩高い有機基が互いに避けるように回転しトランス異性体となるので、立体選択性を示す。ヘック反応は工業的に、ナプロキセンや、サンスクリーン剤の成分であるオクチルメトキシケイ皮酸 (Octyl methoxycinnamate) の生産に用いられている。
ナプロキセンの合成は、臭素化されたナフタレン誘導体とエチレンのカップリング反応を含む[11]。
 |
| ナプロキセン生産におけるヘック反応 |
|---|
バリエーション[編集]
分子内ヘック反応[編集]
反応するハロゲン化アリール(あるいはハロゲン化アルケニル)とアルケンが同一分子内にある場合、生成物は環状化合物となる。 この反応は分子内ヘック反応と呼ばれる。 分子内ヘック反応では分子間のヘック反応に比べて立体障害の影響を受けにくいため、環を形成する反応として非常に有用である。 そのため立体的に混雑して合成しにくい多環式の天然物の環構築などに利用されている[12]。
不斉ヘック反応[編集]
生成物がキラルなヘック反応で添加するホスフィン配位子をキラルなものとすれば不斉ヘック反応となる。BINAPやホスフィン-オキサゾリンを分子内に持つ不斉配位子を利用した反応が報告されている[13]。
ヘックオキシアリル化[編集]
ヘックオキシアリル化変法では、syn付加中間体においてパラジウム置換基がヒドロキシル基によって置換され、生成物はテトラヒドロフラン環を含む[14]。
 |
| オキシアリル化 |
|---|
アミノ-ヘック反応[編集]
アミノ-ヘック反応では、窒素ー炭素結合が生成する。例えば、強力な電子求引性基を持つオキシムは分子内に存在する末端ジエンと反応してピリジンを与える[15]。触媒はテトラキス(トリフェニルホスフィン)パラジウム(0)、塩基はトリエチルアミンが用いられている。
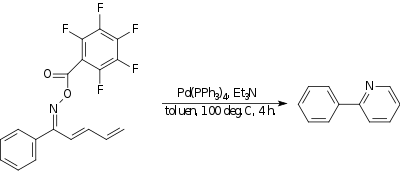 |
| アミノ-ヘック反応 |
|---|
イオン液体ヘック反応[編集]
イオン液体の存在下、ヘック反応はリン配位子無しでも進行する。例えば、逆相シリカゲルに固定化したパラジウムとイオン液体 (bmim)PF6を用いて、水中でヘック反応の行った報告がある[16]。この際、触媒は回収可能である。
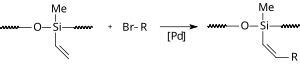 |
| シロキサンへの応用 |
|---|
脚注[編集]
- ^ a b Mizoroki, T.; Mori, K.; Ozaki, A. (1971). “Arylation of Olefin with Aryl Iodide Catalyzed by Palladium”. Bull. Chem. Soc. Jap. 44: 581. doi:10.1246/bcsj.44.581.
- ^ a b Heck, R. F.; Nolley, Jr., J. P. (1972). “Palladium-catalyzed vinylic hydrogen substitution reactions with aryl, benzyl, and styryl halides”. J. Org. Chem. 37 (14): 2320–2322. doi:10.1021/jo00979a024.
- ^ Littke, A. F.; Fu, G. C. (2005). "Heck reactions of aryl chlorides catalyzed by palladium/tri-tert-butylphosphine: (E)-2-Methyl-3-phenylacrylic acid butyl ester and (E)-4-(2-phenylethenyl)benzonitrile". Organic Syntheses (英語). 81: 63.
- ^ Heck, R. F. (1982). “Palladium-Catalyzed Vinylation of Organic Halides”. Org. React. 27: 345–390. doi:10.1002/0471264180.or027.02.
- ^ A. de Meijere, F. E. Meyer, Jr.; (1994). “Fine Feathers Make Fine Birds: The Heck Reaction in Modern Garb”. Angew. Chem. Int. Ed. Engl. 33: 2379–2411. doi:10.1002/anie.199423791.
- ^ Beletskaya, I. P.; Cheprakov, A. V. (2000). “The Heck Reaction as a Sharpening Stone of Palladium Catalysis”. Chem. Rev. 100: 3009–3066. doi:10.1021/cr9903048.
- ^ Fujiwara, Y.; Noritani, I.; Danno, S.; Asano, R.; Teranishi, S. (1969). “Aromatic substitution of olefins. VI. Arylation of olefins with palladium(II) acetate”. J. Am. Chem. Soc. 91: 7166. doi:10.1021/ja01053a047.
- ^ Heck, R. F. (1969). “Mechanism of arylation and carbomethoxylation of olefins with organopalladium compounds”. J. Am. Chem. Soc. 91: 6707. doi:10.1021/ja01052a029.
- ^ Dieck, H. A.; Heck, R. F. (1974). “Organophosphinepalladium complexes as catalysts for vinylic hydrogen substitution reactions”. J. Am. Chem. Soc. 96: 1133. doi:10.1021/ja00811a029.
- ^ Ozawa, F.; Kubo, A.; Hayashi, T. (1992). “Generation of Tertiary Phosphine-Coordinated Pd(0) Species from Pd(OAc)2 in the Catalytic Heck Reaction”. Chemistry Lett.: 2177–2180. doi:10.1246/cl.1992.2177.
- ^ De Vries, J. G. (2001). “The Heck reaction in the production of fine chemicals”. Can. J. Chem. 79: 1086. doi:10.1139/cjc-79-5-6-1086.
- ^ Dounay, A. B.; Overman, L. E. (2003). “The asymmetric intramolecular Heck reaction in natural product total synthesis”. Chem. Rev. 103 (8): 2945–2964. doi:10.1021/cr020039h.
- ^ Shibasaki, M.; Vogl, E. M.; Ohshima, T. (2004). “Asymmetric Heck reaction”. Adv. Synth. Catal. 346: 1533–1552. doi:10.1002/adsc.200404203.
- ^ Kiss, L.; Kurtan, T.; Antus, S.; Brunner, H. (2003). “Further insight into the mechanism of Heck oxyarylation in the presence of chiral ligands” (PDF). Arkivoc: GB–653J.
- ^ Kitamura, M.; Kudo, D.; Narasaka, K. (2005). “Palladium(0)-catalyzed synthesis of pyridines from β-acetoxy-γ,δ-unsaturated ketone oximes” (PDF). Arkivoc: JC–1563E.
- ^ Hagiwara, H.; Sugawara, Y.; Hoshi, T.; Suzuki, T. (2005). “Sustainable Mizoroki–Heck reaction in water: remarkably high activity of Pd(OAc)2 immobilized on reversed phase silica gel with the aid of an ionic liquid”. Chemical Communications (23): 2942–2944. doi:10.1039/b502528a. PMID 15957033.

