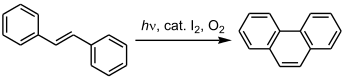スチルベン
| trans-スチルベン | |
|---|---|
 | |
| IUPAC名 | trans-スチルベン(許容慣用名)、(E)-1,2-ジフェニルエテン |
| 分子式 | C14H12 |
| 示性式 | C6H5CH=CHC6H5 |
| 分子量 | 180.25 |
| CAS登録番号 | 103-30-0 |
| 形状 | 無色結晶 |
| 融点 | 122–125 °C |
| 沸点 | 305–307 °C |
| SMILES | c1(/C=C/c2ccccc2)ccccc1 |
| cis-スチルベン | |
|---|---|
 | |
| IUPAC名 | cis-スチルベン(許容慣用名)、(Z)-1,2-ジフェニルエテン |
| 分子式 | C14H12 |
| 分子量 | 180.25 |
| CAS登録番号 | 645-49-8 |
| 形状 | 無色液体 |
| 融点 | 5–6 °C[1] |
| 沸点 | 148–151 °C/20 mmHg[2] |
| SMILES | c1(/C=C\c2ccccc2)ccccc1 |
スチルベン (stilbene) とは、芳香族の炭化水素の1種の有機化合物。その構造から明らかなように、分子全体が共役系であり、π電子雲が分子全体に広がっている。IUPAC系統名は 1,2-ジフェニルエテン。二重結合のシス-トランス異性により、トランス体(E体)とシス体(Z体)が存在するが、熱力学的にはトランス体がより安定である。両異性体ともに市販されている。
化合物名は、19世紀中期に名付けられたもので、ギリシャ語の stilbein (光ること)に由来する[3]。
合成法[編集]
トランス体、シス体それぞれに、選択的な合成法が知られる。
トランス体は、ベンゾインのクレメンゼン還元により得る手法が知られている[4]。
シス体は、α-フェニルケイヒ酸、つまり、(E)-ケイヒ酸の2位の炭素に結合している水素がフェニル基に置換された化合物を、脱炭酸することによって合成できる[5]。
用途[編集]

スチルベンは分子全体に共役系が広がっているので、スチルベン、あるいは、その誘導体は、色素や蛍光増白剤の原料や、シンチレーターの燐光体、色素レーザーの利得媒質として用いられる。
天然においては、植物中にスチルベンの誘導体(スチルベノイド)が植物中に見られる。その1例がレスベラトロールである。
スチルベンの誘導体として、強力なエストロゲン作用を持つために、かつて流産の阻止などに用いられたものの、発がん性が認められて使用が中止された合成品のジエチルスチルベストロールがある。
光反応[編集]
スチルベンはジアリールエテン類の中の最も単純な化合物であり、アゾベンゼン同様、紫外光の照射によりシス-トランス異性化を行う。
スチルベンの場合はさらに電子環状反応を起こして環化し、4a,4b-ジヒドロフェナントレンが発生する。ここにヨウ素などの酸化剤を共存させておいた場合、脱水素化が起こりフェナントレンを与える。
出典[編集]
- ^ Brackman, D. S.; Plesch, P. H. (1952). "406. Some physical properties of cis-stilbene". J. Chem. Soc. 2188–2190. doi:10.1039/JR9520002188.
- ^ Buss, A. D.; Warren, S.; Leake, J. S.; Whitham, G. H. (1983). "On the preparation of (E)- and (Z)-stilbene from the diastereoisomeric 1,2-diphenyl-2-diphenylphosphinoylethan-1-ols". J. Chem. Soc., Perkin Trans. 1 2215–2218. doi:10.1039/P19830002215.
- ^ Oxford Dictionary of English, 2003.
- ^ Shriner, R. L.; Berger, A. (1943). "trans-Stilbene". Organic Syntheses (英語). 23: 86.; Collective Volume, vol. 3, p. 786
- ^ Buckles, R. E.; Wheeler, N. G. (1953). "cis-Stilbene". Organic Syntheses (英語). 33: 88.; Collective Volume, vol. 4, p. 857