キラリティー


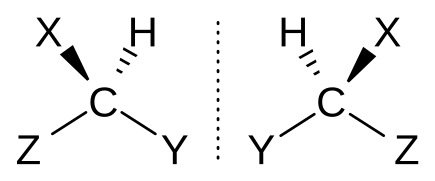
キラリティー(英: chirality)は、3次元の図形や物体や現象が、その鏡像と重ね合わすことができない性質である。
概要[編集]
キラリティがあることをキラル (chiral) という。英語風の発音でカイラリティ、カイラルともいう[注釈 1]。
これらの語はギリシャ語で「手」を意味するχειρ (cheir) が語源である。手はキラルなものの一例で、右手とその鏡像である左手は互いに重ね合わせられない(右手の掌と左手の甲を向かい合わせたときに重なり合わないということである)。
一方でキラリティがない、つまり鏡像と重ね合わせられることをアキラル (achiral) という。キラルな図形とその鏡像を互いに(たとえば右手に対する左手を)エナンチオモルフ (enantiomorphs) と言い、ギリシャ語で「反対」を意味するεναντιος (enantios) が語源である。
対掌性(たいしょうせい)ともいい、「対掌」とは右と左の手のひらの対を意味している。対称性と紛らわしいが、キラリティとは鏡像対称性の欠如であり、むしろ逆の意味になる。
幾何学的な図形のほか、分子、結晶、スピン構造などについて使われる。以下では分子のキラリティを中心に述べる。
キラリティーと対称性[編集]
| キラル | アキラル | ||
|---|---|---|---|
| non-Sn | S1 = σ | S2 = i | |
| C1 | 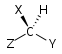 |
 |

|
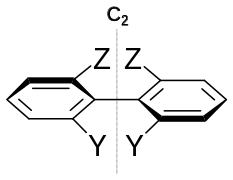
| C2 |  |
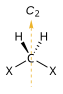 |

|
立体図形の対称操作は全て、n回回転 (Cn) と鏡映 (σ) の組み合わせで表せる。n回回転 (Cn) とはn回の回転で360度回転して元に戻る回転操作で、つまりは360/n度回転させる操作である。従ってC1とは何もしない操作でもある。n回回転 (Cn ) と、その軸に垂直な面での鏡映 (σ) を続けて行う操作をn回回映 (Sn) という。したがって1回回映 (S1) とは鏡映に他ならない。一点を中心に図形の全ての点を反対側に映す操作を反転といい i で表すが、これは2回回映 (S2) に等しい。
このような対称操作とキラリティーの関係は表のようにまとめられる。キラルとはSn軸を持たないことと同義である。鏡映面や反転中心をもたないことは、キラルであることの必要条件であるが十分条件ではない。あくまでも、回映軸が存在するか否かがキラリティーの有無の必要十分条件である。また、キラル図形は全く対称性を持たないもの(無対称)とnが2以上のCn軸だけ持つものに分類できる。
分子のキラリティ[編集]
化学におけるキラリティーは、結合の組み換えなしには分子をそれ自身の鏡像に重ね合わせることができないという性質である。
キラルな分子をキラル分子という。キラル分子は、ちょうど右手と左手のように互いに鏡像である1対の立体異性体を持ち、これら2つの異性体は互いにエナンチオマー (enantiomer)、対掌体(たいしょうたい。対称体は誤り)、あるいは鏡像異性体(きょうぞういせいたい)であるという。
エナンチオマーの等量混合物をラセミ体という。
エナンチオマーの絶対配置を区別するにはRS表記法を使うが、アミノ酸や糖では絶対配置既知の化合物から相対的に決定される伝統的なDL表記法も使われる。
多くのキラル分子は不斉炭素などの不斉中心を持つが、不斉中心の存在はキラルであることの十分条件でも必要条件でもない(後述)。
類義語・廃語[編集]
不斉 (asymmetry) の意味は「無対称」で、本来は、単にキラルであるだけでなく回転対称性もないということである。
歴史的には、酒石酸のキラリティーを発見したパスツールは1860年にdissymétrieという語を使ったが、英語とドイツ語に翻訳される際にasymmetryとAsymmetrieに変わった。日本語ではasymmetryを不斉、dissymmetryを不均斉と翻訳してきた[1]。しかし不均斉という言葉は現在あまり使われておらず、不斉をキラリティーとほぼ同義語に使うことも多い。また『学術用語集 化学編』[2]では asymmetry に無対称という訳語を当てているが[1]、無対称という言葉も化学用語としては現在あまり使われていない。
光学異性体という用語は高校の化学にも出てくるが、物質を分類する方法としてはIUPACでは推奨していない[3]。エナンチオマー以外にジアステレオマーを含みうるからである。
キラリティーの源[編集]
立体幾何学 — 静的な視点[編集]
メタンは4個の水素原子が正四面体の頂点に位置し炭素原子はその中心に位置するテトラヘドラル対称(Td対称)な分子であり、アキラルである。この水素をひとつずつ別の原子で置き換えてゆくと少しずつ対称性が崩れ、4個の原子全てが異なるものになると、無対称でキラルな分子となる。このとき、元はTd対称の中心であった炭素原子を不斉中心 (asymmetric center/asymmetric centre) またはキラル中心 (chiral center, chiral centre) という。このように、本来は対称的なアキラル分子の構造が変化してキラル分子になったと考えたとき、元の対称的分子の対称中心、対称軸、対称面などが変化して非対称な中心・軸・面になったという見方から、不斉中心・不斉軸・不斉面とよび、これらを不斉源と称する。なお、ここでの対称中心は反転対称の中心という意味ではなく、異なる対称軸の交点(不動点となる)という意味で使っている。不斉中心、不斉軸、不斉面を定義することは命名法の上で必要である[4]。
なお、不斉中心・不斉軸・不斉面の定義としては、「点の周りの空間、直線の周りの空間、面の周りの空間を不斉に占有する」ときのそれらの点・直線・面のことともされている[4]。IUPACではキラル中心、キラル軸の定義を「鏡像と重ならないような空間配置になるように、置換基をその周囲に持つ (a set of ligands is held so that it results in a spatial arrangement which is not superposable on its mirror image)」原子および軸としている[3]。
- 不斉中心
- その4つの単結合の置換基が全て異なる炭素原子を不斉炭素と呼び、不斉炭素を持つ分子はキラルになることが多い。例えば不斉炭素の置換基が全てアキラルであれば、この分子はキラルである。不斉炭素の置換基のうち2個が互いに対掌体であれば、この分子はアキラルである。炭素以外の原子でも置換基がほぼ正四面体に結合すれば同じことであり、炭素に限定しない場合は不斉中心と呼ぶ。
- 不斉軸
- アレン (allene) 誘導体、単結合周りの回転が止まったビフェニル誘導体やBINAPのように、対称軸となる原子結合鎖に異なる置換基が結合することでキラルとなった場合に、この軸を不斉軸という。これらの分子には不斉中心はないがキラルである。XYC=C=CXYのような分子は不斉軸の周りのらせんによるキラリティーだとも言える。
- 不斉面
- 1つのベンゼン環の2個の炭素を原子鎖で結合したシクロファンや2個のヘキサペンタジエニルアニオンが鉄(II) に配位したフェロセンの誘導体では不斉中心がないのにキラルなものがある。これらはベンゼン環平面への置換によりキラルとなったとして、ベンゼン環平面を不斉面と定義する。trans-シクロオクテンもエナンチオマーが単離でき、その二重結合と隣接原子を含む平面が不斉面となる[4]。これらは不斉面に垂直ならせん軸によるキラリティーとも言える。
- らせん軸
- ヘリセンには不斉中心も不斉軸も不斉面もないがキラルであり、ヘリシティーが右ねじと左ねじのエナンチオマーを持つ。
結合軸回転 — 動的な視点[編集]
通常の分子では単結合は自由回転できるので多くの立体配座(コンホメーション)を取りえ、これらの立体配座間で常に変化している。したがって、分子Rのコンホメーションのどれかと分子Lのコンホメーションのどれかとが鏡像ならば、分子Rと分子Lは互いに対掌体である。だが高い立体障壁などにより自由回転が抑制されると、異なる立体配座を持つ分子が配座異性体または回転異性体、アトロプ異性体として分離される。そして互いに鏡像である配座異性体同士は互いにエナンチオマーとなる。
前述のビフェニル誘導体やBINAPは芳香環を結ぶ単結合の周りの回転が抑制されたためにエナンチオマーが生じたのであり、アトロプ異性体でもある。またシクロファンなどの面不斉化合物も、不斉面となるベンゼン環に結合する単結合周りの回転が抑制されたためのアトロプ異性体でもある。
エナンチオマーの性質の違い[編集]
キラル分子のエナンチオマーは物質量、結合のエネルギーは等しい。そのためにほとんどの物理的性質(密度、融点、沸点、屈折率、熱伝導度など)は全く同じである。しかし、旋光性と、ある条件下での化学的性質(生化学的性質を含む)が異なることがある。
旋光性[編集]
旋光性は不斉原子を有する分子の持つ電気双極子の構造が電磁波の偏光面を変えるので、対になるキラル分子は、絶対値が等しく正負が逆の偏光性を示す(右回りに回転させるほうが(+)で、左回りに回転させるほうが (-) である。それぞれ右旋性、左旋性という)。しかしながら旋光性の強度(旋光度)や装置の検出限界などによっては、キラル分子が見かけ上で光学活性を示さないこともある。
生体分子活性[編集]
キラル分子のエナンチオマーは、アキラルな分子に対する反応性は全く同じだが、別なキラル分子との反応や、キラルな反応場下での反応(たとえば酵素反応)は反応性が異なる。この性質は有機合成においてエナンチオ選択性や不斉合成に応用される。機能性生体分子のほとんどはエナンチオマーを識別するので(基質選択性を参照のこと)、2つのエナンチオマーの生理活性は非常に異なるのが普通である。
アミノ酸や糖など生体分子の多くはキラルであり、原則として片方のエナンチオマーのみが使われている。非常に例外的に逆のエナンチオマーが使われている場合もある。地球上ではアミノ酸ではL体、糖ではD体が主流だが、このようなホモキラリティーが進化のいつの段階で生じたのかは化学進化上の未解決問題のひとつである。
キラル分子を用いた薬は、高いエナンチオマー純度が要求される。たとえば、サリドマイドを考えると、R体は睡眠薬や乗り物酔い止めとして有効な薬であるが、S体は催奇性を持っている。しかし、R体・S体を分離する(光学分割)することも可能だが、R体のみを服用しても比較的速やかに体内でS体に変化することがわかっている。このため、R体が催眠作用のみを持ち、S体のみが催奇性だけを現すという当初の一般薬理評価には近年疑問が持たれている。
キラル中心「孤立電子対」を持つ化合物のキラリティー[編集]

孤立電子対(非共有電子対)が空間を占める時、キラリティーが生じることがある。この効果は特定のアミン、ホスフィン[5]、スルホニウムおよびオキソニウムイオン、スルホキシド、カルバニオンにまで拡がっている。主な要件は、孤立電子対は別として、その他の3つの置換基が互いに異なっていることである。キラルホスフィン配位子は不斉合成において有用である。
キラルアミンはエナンチオマーが稀にしか分離できないという意味において特別である。キラル中心の窒素反転のエネルギー障壁は一般的におよそ30キロジュール/モルであり、2つの立体異性体は室温で素早く相互変換する。その結果、トレーガー塩基の環状構造のように置換基が制限されない限りは、こういったキラルアミンでは個々のエナンチオマーは分割することは不可能である。
脚注[編集]
注釈[編集]
- ^ ただし、実際の発音は/ˈkaɪərəl/であり、少なくとも音素訳的な立場からは「カイヤラル」または「カイヤアル」の方が適切だと言える。
出典[編集]
- ^ a b 日本化学会編 『標準化学用語辞典』 第2版、丸善、2005年、「不均斉」の項。ISBN 4-621-07531-4.
- ^ 文部省・日本化学会編 『学術用語集 化学編』 増訂2版、南江堂、1986年。ISBN 4524408215.
- ^ a b IUPAC Recommendations 1996; Basic Terminology of Stereochemistry. (外部リンク参照)
- ^ a b c 大木道則 『立体化学』 第4版、東京化学同人、2002年。ISBN 4-8079-0550-3.
- ^ Quin, L. D. A Guide to Organophosphorus Chemistry; John Wiley & Sons, 2000. ISBN 0-471-31824-8.
関連人物[編集]
関連項目[編集]
- 立体異性体
- 光学異性体
- 不斉炭素
- 不斉合成
- ラセミ体
- プロキラリティー
- ホモキラリティー
- 鏡像体過剰率
- プファイファー効果
- 超臨界流体クロマトグラフィー
- カイラル対称性(素粒子論)
- ルイ・パスツール
- 鏡像
外部リンク[編集]
- IUPAC (Basic Terminology of Stereochemistry)
- キラリティーとにおい(英語)
- 鏡の国の生命 - ウェイバックマシン(2018年11月6日アーカイブ分)