アルキン


アルキン(ドイツ語: Alkin、英語: alkyne)は、分子内に炭素間三重結合を1個だけ持ち、一般式が CnH2n−2 で表される鎖式炭化水素の総称である。アセチレン系炭化水素とも呼ばれる。広義には分子内に非環式および環式の C−C 三重結合を持つ化合物全般を指し、この場合「アセチレン」の語を一般名称として用いる。
構造[編集]
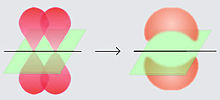
アルキンの2つの炭素原子の電子軌道は共にsp混成しており、それぞれ2つのp軌道と2つのsp混成軌道を持つ。各炭素原子はsp軌道を1つずつ提供し、それらが重なることによりσ結合を形成する。また、p軌道同士が重なり合うことによって作られる2つのπ結合も持っている。合計3つの C−C 結合からなるため、これは三重結合と呼ばれる。残りのsp軌道は他の原子とσ軌道を作る。例えば親化合物であるアセチレンでは水素原子と結合している。アルキン上の2つのsp軌道は互いに反対向きに位置しており、アセチレンでは H−C−C 結合角は180度である。合計6個の電子が関与しているため、この三重結合は非常に強く、結合エネルギーは 837 kJ/mol である。個別の結合エネルギーはσ結合 369 kJ/mol、1つめのπ結合 268 kJ/mol、2つめのπ結合 202 kJ/mol である。C−C 結合距離は 121 pm であり、これはアルケンの 134 pm、アルカンの 153 pm と比べ短い。
命名法[編集]
IUPAC命名法では、語幹に -yne を付加することによって命名する。つまり、対応するアルカン alkane の語尾 -ane を -yne に変えればよい。三重結合の位置は位置番号で表し、これが最も小さくなるように番号を与える。アルキンを2つ以上含む場合は数辞を付け -diyne (ジアルキン), -triyne (トリアルキン), ... とする。例えば、 は 1-ブチン 1-butyne、 は 2-ペンチン 2-pentyne、は ノナ-2,5-ジイン nona-2,5-diyne である。親化合物 HC≡CH は許容慣用名アセチレン acetylene を持つ。
アルキニル基[編集]
アルキンの水素原子を1個取り除いた形である1価の置換基はアルキニル基(—き)と呼ばれる。三重結合上の水素を除いた場合はエチニル基 ethynyl (HC≡C−) など、その他の鎖上の水素原子を除いた場合はプロパ-2-イン-1-イル基 prop-2-yn-1-yl (HC≡CCH2−) などのように呼ぶ。後者は特に慣用名プロパルギル基で呼ばれることも多い。エチニルベンゼン ethynylbenzene (HC≡CC6H5)、プロパルギルアルコール propargyl alcohol (HC≡CCH2OH) などのように用いる。
末端アルキンと内部アルキン[編集]
アルキンはsp混成軌道でσ結合を作ることにより、各炭素原子上に1つずつ、計2つの置換基を持つことができる。このうち片方が水素原子と結合しているものを末端アルキン(まったんアルキン、terminal alkyne)と呼ぶ。例えば示性式 CH3C≡CH で表されるプロピン(メチルアセチレン)がその例である。
これに対し、2つの炭素原子上に共に水素原子以外の基を持つものを内部アルキン(ないぶアルキン、internal alkyne)と呼ぶ。置換する基はヘテロ原子である場合もある。2-ペンチン 2-pentyne などがその例である。これは示性式 で表され、2つのアルキン炭素原子はそれぞれメチル基とエチル基を持っている。
酸性度[編集]
末端アルキンのプロトンはアルカンやアルケンに比べて解離しやすい。アセチレンの pKa は25であり、アンモニア (35) とエタノール (16) の中間程度で、エチレン (44)、エタン (50) よりはるかに低い。これは、生成するアセチリド C≡C− 上の電子対が収容されるsp軌道のs性が高いため、負電荷が安定化されやすいからであると説明される。一般に、ある軌道のs性が高い場合、正電荷を持つ原子核との距離がより小さくなるため、そのエネルギーは低くなる。
アセチリド[編集]
末端アルキンに強塩基、例えば金属ナトリウム、ナトリウムアミド、n-ブチルリチウム、グリニャール試薬などを作用させると、水素を発生しながらアセチリドを生じる。
アセチリドは強い求核剤として有機合成上有用であり、C−C 結合生成反応に使われる。
他に銀アセチリドや銅アセチリドも知られる。
合成[編集]
隣接する2つのハロゲンを持つアルカン誘導体の脱ハロゲン化水素化によって合成される。
アセチリドをハロゲン化アルキルと反応させ、炭素骨格を伸ばすことができる。
フリッツ・バッテンバーグ・ビーチェル転位 (Fritsch-Buttenberg-Wiechell rearrengement) は1,1-ジアリール-2-ブロモエチレンからアリール基が転位したアルキンを合成する反応である。中間体としてカルベンを経由する。
アルデヒドに下式に示すα-ジアゾホスホナート化合物を作用させると炭素が1個増えた末端アルキンが得られる。このホスホナートは開発者の名をとって「大平-ベストマン試薬」と呼ばれる[1][2]。
天然物[編集]

アルキンは天然物としてはそれほどありふれたものではなく、よく知られている化合物は1000種類程度である。そのうち生理活性を示すものは多くないが、殺菌剤、自己防衛のための毒、あるいは誘引物質などとして知られるものもある。
例えばヤドクガエルは哺乳類や爬虫類などの捕食者から身を守るためにヒストリオニコトキシンと呼ばれる毒素を皮膚から分泌するが、これは分子内に2つのアルキンを持つ化合物である。また、アルキンを含む天然物群の一角はエンジイン構造を持つ抗生物質によって占められている。活性部位にエンジイン構造を持つカリケアミシン・ネオカルチノスタチンなどの天然物は細胞毒性または抗腫瘍活性を示すものが多く、それらは化学療法剤として利用できる可能性を持つ。
その他には、ドクゼリの毒成分シクトキシン、中国雲南省に自生するホウライタケ科の猛毒菌Trogia venenataの毒成分2R-アミノ-4S-ヒドロキシ-5-ヘキシン酸と2R-アミノ-5-ヘキシン酸[3]などが知られる。
主なアルキン[編集]
- アセチレン C2H2
- プロピン(メチルアセチレン) C3H4
- ブチン(1-ブチン、2-ブチン) C4H6
- ペンチン(1-ペンチン) C5H8
- アセチレンジカルボン酸ジメチル (DMAD)
- ジフェニルアセチレン(トラン)
- プロパルギルアルコール
関連項目[編集]
- アルカン
- アルケン
- ベンザイン - 構造式で C≡C 三重結合が描かれる芳香族中間体。
- ニトリル - C≡N 三重結合を持つ化合物群。
- ポリアセチレン - アセチレンが重合した高分子。
- ポリイン
- カルビン
参考文献[編集]
- ^ Ohira, S. Synth. Commun. 1989, 19, 561.
- ^ Müller, S.; Liepold, B.; Roth, G.; Bestmann, H. J. Synlett, 1996, 521. DOI: 10.1055/s-1996-5474
- ^ Deadly chinese mushrooms: Amino acids revealed as cause of deaths in Yunnan province., Internetchemistry.com, 2012年2月12日








