ホスホール
| ホスホール | |
|---|---|

|

|
1H-Phosphole | |
| 識別情報 | |
| CAS登録番号 | 288-01-7 |
| PubChem | 164575 |
| ChemSpider | 144273 |
| |
| |
| 特性 | |
| 化学式 | C4H5P |
| モル質量 | 84.06 g mol−1 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ホスホール (phosphole) とは、分子式が C4H5P と表される有機リン化合物[1]。ピロールの窒素がリンに置き換わった類縁体にあたる。ホスホール環を含む一連の誘導体も一般に「ホスホール」と呼ばれる。理論面での興味だけではなく、遷移金属化合物における配位子として、またより複雑な有機リン化合物への前駆体として興味が持たれてきた化合物である。
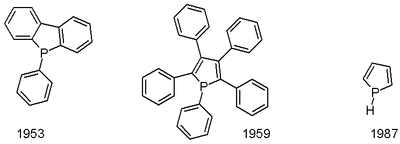
ホスホールを含む環縮合化合物では 1953年、トリフェニルホスフィンとフェニルナトリウムとの反応により p-フェニルジベンゾホスホールが得られることが ゲオルク・ウィッティヒらによって報告された[2]。その後、ホスホールを単環で持つ化合物の最初の例として、1959年にペンタフェニルホスホールを得たとする複数の報告がある[3][4]。そして親化合物である無置換のホスホールは、1983年に p-アニオンのプロトン化により低温で調製され反応性が調べられた[5]。
ホスホール誘導体を得る通常の合成ルートでは、McCormackの手法を利用する。そこではまず 1,3-ジエンとジクロロホスフィンからジヒドロホスホール環を作り、その後脱水素化によりホスホール環を得る[6]。ほか、ジルコナシクロペンタジエン(シクロペンタジエンのメチレン基 -CH2- がジルコニウム -Zr(Cp2)- に置き換わったもの)とジクロロフェニルホスフィンから 1-フェニル-1H-ホスホールが得られる[7]。
ピロールやチオフェン、フランなど他の複素5員環化合物と異なり、ホスホールの芳香族性は弱い。それはリンの非共有電子対が炭素のπ電子系と共役しにくいためである.[8]。例えば、ホスホールは電子不足なアルキンとディールス・アルダー反応を起こすなど、ジエン性を示す。
脚注[編集]
- ^ 総説: Mathey, F. (1988). “The organic chemistry of phospholes”. Chem. Rev. 88: 429–453. doi:10.1021/cr00084a005.
- ^ Wittig, G.; Geissler, G. (1953). “Zur Reaktionsweise des Pentaphenyl-phosphors und einiger Derivate”. Justus Liebigs Ann. Chem. 580: 44-57. doi:10.1002/jlac.19535800107.
- ^ Leavitt, F. C.; Manuel, T. A.; Johnson, F. (1959). “Novel heterocyclo pentadienes”. J. Am. Chem. Soc. 81: 3163-3164. doi:10.1021/ja01521a083.
- ^ Braye, E. H.; Hubel, W. (1959). “Proton [1,5] shifts in P-unsubstituted 1H-phospholes. Synthesis and chemistry of 2H-phosphole dimers”. Chem. Ind. (London): 1250-1251.
- ^ Charrier, C.; Bonnard, H.; De Lauzon, G.; Mathey, F. (1983). J. Am. Chem. Soc. 105: 6871-6877. doi:10.1021/ja00361a022.
- ^ W. B. McCormack (1973). "3-Methyl-1-Phenylphospholene oxide". Organic Syntheses (英語).; Collective Volume, vol. 5, p. 787
- ^ Paul J. Fagan and William A. Nugent (1998). "1-Phenyl-2,3,4,5-Tetramethylphosphole". Organic Syntheses (英語).; Collective Volume, vol. 9, p. 653
- ^ D. B. Chesnut, L. D. Quin (2007). “The important role of the phosphorus lone pair in phosphole aromaticity”. Heteroatom Chemistry 18: 754-758. doi:10.1002/hc.20364.