一酸化二硫黄
| 酸化二硫黄 | |
|---|---|

| |
| |
| 識別情報 | |
| CAS登録番号 | 20901-21-7 [1] |
| PubChem | 140772 |
| ChemSpider | 124163 |
| |
| 特性 | |
| 化学式 | S2O |
| モル質量 | 80.1294 g/mol[1] |
| 外観 | 無色のガスまたは暗赤色の固体[2] |
| 構造 | |
| 配位構造 | 角度 |
| 危険性 | |
| 主な危険性 | 有毒 |
| 関連する物質 | |
| 関連物質 | 一酸化硫黄、 オゾン、 二酸化硫黄 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
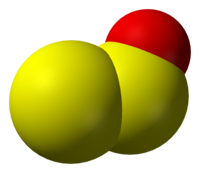
一酸化二硫黄(いっさんかにいおう、disulfur monoxide)は硫黄酸化物の一種で化学式は S2O である。
低硫黄酸化物の一つ。低圧下で気体として存在する化合物であり、凝縮して明るい色固体を形成し、室温では不安定である[3] 。
S-S-O角度が117.88°、S-S結合長が188.4pm、S-O結合長が146.5pmの角分子です[4]。
1933年Peter W. Schenkによって発見された[5]。
合成[編集]
- 3 S8 + 12 CuO → 12 CuS + 4 S2O + 4 SO2
また塩化チオニルと硫化銀(I)を160℃で反応させると得られる[6]。
- SOCl2 + Ag2S → 2 AgCl + S2O
- 3 SO → SO2 + S2O
脚注[編集]
- ^ a b c “Disulfur monoxide”. NIST (2008年). 2020年4月29日閲覧。
- ^ B Hapke and F Graham (May 1989). “Spectral properties of condensed phases of disulfur monoxide, polysulfur oxide, and irradiated sulfur”. Icarus 79 (1): 47. Bibcode: 1989Icar...79...47H. doi:10.1016/0019-1035(89)90107-3.
- ^ R. Steudel: Sulfur-Rich Oxides SnO and SnO2" in Elemental Sulfur und Sulfur-Rich Compounds II, Steudel, R., 2003, Springer, Berlin-Heidelberg. ISBN 9783540449515
- ^ Meschi, D. J.; Myers, R. J. (1959). “The microwave spectrum, structure, and dipole moment of disulfur monoxide”. Journal of Molecular Spectroscopy 3 (1–6): 405–416. Bibcode: 1959JMoSp...3..405M. doi:10.1016/0022-2852(59)90036-0.
- ^ a b Ralf Steudel (2003), [一酸化二硫黄, p. 204, - Google ブックス Elemental Sulfur and Sulfur-Rich Compounds II] (ドイツ語), Springer, ISBN 354040378-7。
{{citation}}:|url=の値が不正です。 (説明) - ^ a b Ralf Steudel (2003), [一酸化二硫黄, p. 205, - Google ブックス Elemental Sulfur and Sulfur-Rich Compounds II] (ドイツ語), Springer, ISBN 354040378-7。
{{citation}}:|url=の値が不正です。 (説明)
