酸化ヨウ素(V)
| 酸化ヨウ素(V) Iodine pentoxide | |
|---|---|
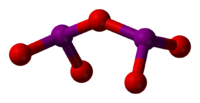
| |
diiodine pentoxide | |
別称 無水ヨウ素酸[1]、五酸化二ヨウ素 | |
| 識別情報 | |
| CAS登録番号 | 12029-98-0 |
| PubChem | 159402 |
| ChemSpider | 140179 |
| ChEBI | |
| |
| |
| 特性 | |
| 化学式 | I2O5 |
| モル質量 | 333.81 g/mol |
| 外観 | 吸湿性のある、白色の結晶性固体[2] |
| 密度 | 4.980 g/cm3[2] |
| 融点 |
300 °Cで分解[3] |
| 水への溶解度 | 187.4g/100g(13℃)[1] |
| 溶解度 | 硝酸に可溶 エタノール、エーテル、クロロホルム、二硫化炭素に不溶[1] |
| 危険性 | |
| 主な危険性 | 酸化性 |
| NFPA 704 | |
| 引火点 | (不燃性) |
| 関連する物質 | |
| その他の陰イオン | 五フッ化ヨウ素 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
酸化ヨウ素(V)(さんかヨウそ、英: Iodine pentoxide)はヨウ素酸の無水物で、化学式I2O5で表される無機化合物。無水ヨウ素酸、五酸化二ヨウ素とも呼ばれる。乾燥した空気中で、ヨウ素酸を200℃に熱して脱水することにより得られる[2]。
- 2HIO3 → I2O5 + H2O
構造
ヨウ素-酸素-ヨウ素の角度は139.2°であるが、分子は鏡面ではないため分子対称性はC2v対称ではない。ヨウ素原子から終端の酸素原子までの間は1.80Åで、二つのヨウ素原子をつなぐ酸素原子までの間は1.95Åである[4]。
反応
強い酸化性を持ち、室温で一酸化炭素を二酸化炭素に容易に酸化させる。
- 5CO + I2O5 → I2 + 5CO2
この反応により、気体試料中の一酸化炭素濃度を測定することができる。
酸化ヨウ素(V)は、三酸化硫黄やビス(フルオロスルフリル)ペルオキシド(S2O6F2)と、ヨージル塩[IO2+]を形成する。硫酸とはヨードシル塩[IO+]を形成する。
通常の条件では安定している。275℃以上で酸素とヨウ素とに分解が始まり、生成したヨウ素により褐色に変色する。日光により同様に分解する。
塩化水素との反応で、水と三塩化ヨウ素を生じる。硫化水素とは激しく反応し、ヨウ素、ヨウ化水素、硫黄、水を生じる[1]。
安全性
関連項目
脚注
- ^ a b c d “製品安全データシート” (PDF). キシダ化学 (2011年7月25日). 2012年5月6日閲覧。
- ^ a b c グリーンウッド, ノーマン; アーンショウ, アラン (1997). Chemistry of the Elements (英語) (2nd ed.). バターワース=ハイネマン. pp. 851–852. ISBN 978-0-08-037941-8。
- ^ Patnaik, P. (2002). Handbook of Inorganic Chemicals. McGraw-Hill. ISBN 0070494398
- ^ Selte, K.; Kjekshus, A. (1970). “Iodine Oxides: Part III. The Crystal Structure of I2O5” (pdf). Acta Chemica Scandinavica 24 (6): 1912–1924. doi:10.3891/acta.chem.scand.24-1912.

