エリスロマイシン
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 胎児危険度分類 | |
| 法的規制 | |
| 投与経路 | 経口投与、点滴静脈注射、局所 |
| 薬物動態データ | |
| 代謝 | 肝臓(under 5% excreted unchanged) |
| 半減期 | 1.5 時間 |
| 排泄 | 胆汁 |
| 識別 | |
| CAS番号 | 114-07-8 |
| ATCコード | D10AF02 (WHO) J01FA01 (WHO)S01AA17 (WHO) |
| PubChem | CID: 3255 |
| DrugBank | APRD00953 |
| ChemSpider | 12041 |
| KEGG | D00140 |
| 化学的データ | |
| 化学式 | C37H67NO13 |
| 分子量 | 733.93 g/mol |
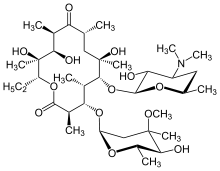
エリスロマイシン (INN:erythromycin) とは、14員環マクロライド系抗菌薬の1つである。日本では「エリスロシン」の商品名でも販売されてきた経緯が有るものの、化学でエリスロシン(英語:erythrosine)と言った場合には、全く別な赤色の合成着色料の1種の名称である。
所在[編集]
エリスロマイシンは天然に存在する化合物の1つであり、放線菌属の Saccaropolyspora erythraea[1] (旧名 Streptomyces erythraeus[2])によって作り出される。14員環ラクトン環に2つの糖(L-クラジノースとD-デソアミン)が付いた構造を持つ。合計10箇所の不斉中心を有するなど構造が複雑なため、合成するのは難しいとされる化合物である。
作用機序[編集]
細菌のタンパク質合成装置であるリボソームの機能を阻害する事によって、細菌の増殖を抑える。エリスロマイシンは細菌のリボソーム中の50S サブユニットにおける 23s rRNA に結合し、伸張するペプチドの出口を塞ぎ、ペプチドの転位を阻害する。
細胞壁とは無関係なので、細胞壁を持たないマイコプラズマなどにも効果が望める。一方で、リボソームの結合部位に変異を持った細菌に対しては、エリスロマイシンが結合し難いため著しく効果が減弱する[注釈 1]。また、ラクトンである14員環の部分を特異的に加水分解する酵素を有した細菌も知られている。
薬物動態[編集]
エリスロマイシンは胃酸によって容易に失活するため、経口投与する場合には、胃酸で溶けないコーティングを施すか、胃酸に対して、より安定な塩やエステル体を投与する必要がある。
吸収・分布[編集]
空腹時であれば吸収される速度は高く、ほとんどの組織や食細胞に拡散する。食細胞中での濃度が高くなり易いため、感染部位に到達し易く、食細胞が活動している間に高濃度のエリスロマイシンが放出される。ただし、髄液への移行は無い。適切な剤形で経口投与した場合のバイオアベイラビリティは、50パーセント程度である。
代謝・排泄[編集]
体内に吸収されたエリスロマイシンは、大部分が肝臓で脱メチル化を受ける。脱メチル化されたエリスロマイシンの抗菌活性は、低下する事が知られている。参考までに、主な排出経路は胆汁である。なお、ごく少量は尿に排出されるものの、血液透析や腹膜透析を行ってもエリスロマイシンは、ほとんど体内から除去されない。半減期は約1.5時間である。
用途[編集]
エリスロマイシンの抗菌スペクトルはペニシリンと類似するが若干幅広く、ペニシリンにアレルギーを持つヒトに対して、しばしば使用される。クラミジア、梅毒、淋病の流行に対処する場合にも用いられる。呼吸器系への感染症に関しては、マイコプラズマ・クラミドフィラなどの非定型微生物に対しても効果を持つ。しかし、市中肺炎の原因菌の1つであるインフルエンザ菌には抗菌活性を示さない。
併用禁忌・薬物相互作用[編集]
かつてエリスロマイシンを投与した場合に突然死を起こした症例が報告されたため、大規模なコホート研究が行われ、ベラパミルやジルチアゼムなどをエリスロマイシンと同時に投与した患者において発生し得る、頻脈や心臓性突然死との関連が明らかにされた[3]。エリスロマイシンは、シトクロムP450 の1つであるCYP3A4と複合体を形成して、CYP3A4を阻害し、ベラパミルやジルチアゼムなどの代謝も遅らせる。このため、それらの薬剤やQT時間を延ばすような薬剤を使用している患者に対して、エリスロマイシンの投与は避けるべきであると結論付けられた。他の例としてテルフェナジン (Seldane, Seldane-D)、アステミゾール (Hismanal)、シサプリド(Propulsid, 多くの国でQT時間を延長させる効果のため認可が取り消された)、ピモジド (Orap) が挙げられる。
さらに、エリスロマイシンはCYP3A4の阻害作用に加えて、P糖タンパク質の機能も阻害するため、他の様々な薬物の代謝や排泄などに影響を与え得るため、薬物相互作用に注意が必要である。なお、エリスロマイシンの胃酸に対する不安定さを改善するために化学修飾を行って開発した、同じ14員環マクロライド系抗菌薬であるクラリスロマイシンでも、同様の現象が知られている。
また、エリスロマイシンの作用点は細菌のリボソームだが、これはリンコマイシンやクリンダマイシンと作用点が重なる関係で、リンコマイシンやクリンダマイシンの作用が消える[4]。
副作用[編集]
下痢、吐き気、腹痛、嘔吐などの消化器系障害がよく見られる。これらの症状はエリスロマイシンが胃酸によって分解された際に生じる、ヘミケタルと言う物質が、消化管の蠕動運動を亢進するため発生するとされる。これが発生する理由は、消化管ホルモンの1つであるモティリンの代わりに作用し、すなわち、モティリン受容体を刺激して、結果として胃の運動を促進すると判明した[5]。
このような問題が有る事も手伝って、エリスロマイシンを第1選択薬として処方する事は、あまり無い。しかしながら、このような運動性を誘発する効果をエリスロマイシンは持つため、胃不全麻痺 (gastroparesis) を処置する際には有効であるとされる。エリスロマイシンの静脈内投与が食道胃十二指腸鏡検査の際に、胃の内容物を排出させるために用いる場合もある。
聴覚障害などのより重大な副作用は稀である。アレルギー反応は一般的ではないが、蕁麻疹やアナフィラキシーが起こる場合がある。胆汁鬱帯、スティーブンス・ジョンソン症候群、中毒性表皮壊死症なども稀に見られる。
妊娠後期に母親がエリスロマイシンを摂取すると、子供の幽門狭窄症の可能性を増加させることが示されている。
歴史[編集]
1949年にフィリピンの科学者アベラルド・アギュイラー (Abelardo Aguilar) は、彼を雇用していたイーライリリーに、ある土のサンプルを送った。マクガイア (J. M. McGuire) が率いるイーライリリーの研究チームは、そのサンプルに含まれていた菌株 Streptomyces erythraeus の代謝産物からエリスロマイシンの単離に成功した。サンプルが採取されたフィリピンの地名のイロイロを取って、商品名はイロソン(Ilosone)と名付られ、1952年に上市された。イロチシン(Ilotycin)とも呼ばれた。
1981年にハーバード大学の化学教授でノーベル化学賞受賞者のロバート・バーンズ・ウッドワードとその研究チームが、エリスロマイシンAの最初の立体選択的不斉合成を報告した。
剤形[編集]
腸溶コーティング錠剤、徐放性カプセル、ドライシロップ、経口懸濁液、点眼液、軟膏、ゼリー、注射剤の形で入手可能である[注釈 2]。
商品名として エリスロシン, Robimycin, E-Mycin, E.E.S. Granules, E.E.S.-200, E.E.S.-400, E.E.S.-400 Filmtab, Erymax, Ery-Tab, Eryc, Erypar, EryPed, Eryped 200, Eryped 400, Erythrocin Stearate Filmtab, Erythrocot, E-Base, Ilosone, MY-E, Pediamycin, PCE Dispertab などが知られる。
脚注[編集]
注釈[編集]
- ^ このリボソームを変化させる事で細菌が獲得した耐性は、マクロライド・リンコマイシン・ストレプトグラミン耐性(MLS耐性)として知られる。これは、14員環や16員環のマクロライド系抗菌薬だけでなく、リンコマイシンやストレプトグラミンに対しても耐性を発揮するためである。
- ^ 日本において一般に流通しているのは、一部剤形のみである。
出典[編集]
- ^ “エリスロマイシン Erythromycin”. 第十八改正日本薬局方名称データベース. 国立医薬品食品衛生研究所 (2021年7月16日). 2022年6月4日閲覧。
- ^ Labeda, David P. (1987-01-01). “Transfer of the Type Strain of Streptomyces erythraeus (Waksman 1923) Waksman and Henrici 1948 to the Genus Saccharopolyspora Lacey and Goodfellow 1975 as Saccharopolyspora erythraea sp. nov., and Designation of a Neotype Strain for Streptomyces erythraeus”. International Journal of Systematic Bacteriology 37 (1): 19. doi:10.1099/00207713-37-1-19.
- ^ Ray, W.A.; Murray, K. T.; Meredith, S.; Narasimhulu, S. S.; Hall, K.; Stein, C. M. (2004). "Oral Erythromycin and the risk of sudden death from cardiac causes". NEJM(ニューイングランド・ジャーナル・オブ・メディシン). 351: 1089–1096. PMID 15356306
- ^ 上野 芳夫・大村 智 監修、田中 晴雄・土屋 友房 編集 『微生物薬品化学(改訂第4版)』 p.188 南江堂 2003年4月15日発行 ISBN 4-524-40179-2
- ^ 重信 弘毅・石井 邦雄(編集)『パートナー薬理学』 p.310 南江堂 2007年4月15日発行 ISBN 978-4-524-40223-6
