過塩素酸アンモニウム
| 過塩素酸アンモニウム | |
|---|---|

| |
| |
Ammonium perchlorate | |
別称 AP | |
| 識別情報 | |
| CAS登録番号 | 7790-98-9 |
| EC番号 | 232-235-1 |
| 国連/北米番号 | 1442 |
| RTECS番号 | SC7520000 |
| 特性 | |
| 化学式 | NH4ClO4 |
| モル質量 | 117.49 g/mol |
| 外観 | 無色の結晶 |
| 密度 | 1.95 g/cm3 |
| 融点 |
200 °C以上で溶融する前に発熱分解[1] |
| 水への溶解度 | 11.56 g/100 mL (0 °C) 20.85 g/100 mL (20 °C) 57.01 g/100 mL (100 °C) |
| 溶解度 | メタノールに可溶 アセトンに部分的に可溶 エーテルに不溶 |
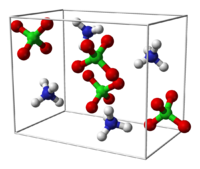
| 構造 | |
| 結晶構造 | 斜方晶 (< 513 K) 立方晶 (> 513 K) |
| 危険性 | |
| 安全データシート(外部リンク) | External MSDS |
| EU分類 | Oxidant (O) |
| EU Index | 017-009-00-0 |
| NFPA 704 | |
| Rフレーズ | R9, R44 |
| Sフレーズ | (S2), S14, S16, S27, S36/37 |
| 関連する物質 | |
| その他の陰イオン | 塩素酸アンモニウム 塩化アンモニウム |
| その他の陽イオン | 過塩素酸カリウム 過塩素酸ナトリウム 過塩素酸リチウム |
| 関連物質 | 過塩素酸 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
過塩素酸アンモニウム(かえんそさんアンモニウム、ammonium perchlorate)は過塩素酸のアンモニウム塩にあたる無機化合物。
化学的性質[編集]
結晶は無色。多くのアンモニウム塩と同様に溶融する前に分解する。他の物質を強く酸化させる性質を持つ固体(酸化性固体)であり、可燃性物質と混合させて、熱、衝撃、摩擦により分解し、きわめて激しい燃焼を得る。
加熱すると約 150 ℃ で分解を始めて酸素を発生し、400 ℃ で発火する。分解時、多量のガスを発生するので危険である[2]。
強熱すると爆発を引き起こす場合がある。
製造[編集]
アンモニアと過塩素酸の反応によって生産される。過塩素酸ナトリウムの水溶液に塩化アンモニウムを加えて析出させて生産することもできる[3]。
用途[編集]
過塩素酸アンモニウムと合成ゴム、金属粉などを混錬して成形したコンポジット推進薬(APCP)はロケットエンジンの推進剤に使用されている。コンポジット推進薬を用いた固体燃料ロケットのブースターはアメリカのスペースシャトルや日本のH-IIロケットで用いられている。また過塩素酸アンモニウムは産業用の火薬の一種であるカーリットの主原料としても使用されている。
300℃まで結合力を持つ一部のエポキシ系接着剤に含まれている。
規制[編集]
GHSにおける火薬類(等級1.1)または酸化性固体(区分2)に該当し、各国で貯蔵や運搬に規制がある(国連番号0402または1442)。日本では船舶安全法や航空法によってGHSに基づく規制があり、また消防法に基づく危険物第1類に指定されている。
燃焼生成物には有毒で発癌性がありオゾン層を破壊し、酸性雨や地球温暖化の原因になる塩素化合物が含まれる。
関連項目[編集]
脚注[編集]
- ^ Liu, L.; Li, F.; Tan, L.; Ming, L.; Yi, Y. (2004), “Effects of Nanometer Ni, Cu, Al and NiCu Powders on the Thermal Decomposition of Ammonium Perchlorate”, Propellant, Explosives, Pyrotechnics 29: 34–38
- ^ T. L. Boggs, Deflagration Rate, Surface Structure and Subsurface Profile of Self-Deflagrating Single Crystals of Ammonium Perchlorate. AIAA Journal, 8(5), 1970, pp. 867--873.
- ^ Helmut Vogt, Jan Balej, John E. Bennett, Peter Wintzer, Saeed Akbar Sheikh, Patrizio Gallone “Chlorine Oxides and Chlorine Oxygen Acids” in Ullmann's Encyclopedia of Industrial Chemistry 2002, Wiley-VCH. doi:10.1002/14356007.a06_483


