Fasリガンド
Fasリガンド(Fas ligand、略号:FasL、別名:CD95L)は、トポロジーII型の膜貫通型蛋白質であり、腫瘍壊死因子(TNF)ファミリーの一員である。アポトーシスを誘導する受容体に結合する。Fasリガンド・受容体相互作用は、免疫系の制御や悪性腫瘍の進行において重要な役割を果たしている。
構造
[編集]Fasリガンド(FasL)は、細胞傷害性T細胞表面に発現しているホモ三量体を形成するII型膜貫通タンパク質である。 Fasリガンドは、標的細胞の膜を貫通するFas受容体(FasR)を三量体化することでシグナルを伝達し、これによりアポトーシスを誘導する。
膜結合型のFasリガンドが、セリンマトリックスメタロプロテアーゼ(MMP-7)により切断される事で、可溶性のFasリガンドが生じる。 可溶性Fasリガンドはアポトーシス誘導能が低下しており、従って、Fasリガンドの可溶化は活性抑制メカニズムの1つである。
受容体
[編集]- FasR
- Fas受容体(FasR、別名:CD95)は最も盛んに研究された細胞死受容体ファミリーのメンバーである。その遺伝子は、ヒトでは10番染色体に、マウスでは19番染色体に位置している。先行研究では、8つのスプライスバリアントが存在し、7つのアイソフォームが翻訳される。アイソフォームの多くは病態に関連する稀なハプロタイプである。アポトーシス誘導性Fas受容体はアイソフォーム1であり、I型膜貫通型蛋白質である。膜貫通部位と細胞内細胞死ドメインに3つのシステインリッチな偽反復を持つ。ヒト線維芽細胞FS7をマウスに免疫して得られたIgMクラスのモノクローナル抗体により認識される抗原として,京都大学の米原伸により1989年に発見された[5]。
- DcR3
- デコイ受容体3(DcR3)は近年発見された、腫瘍壊死因子スーパーファミリーのデコイ受容体であり、FasL、LIGHT(CD258)、TL1Aと結合する。DcR3は可溶性受容体であり、シグナル伝達には寄与せず(それ故“デコイ(囮)”と呼ばれる)、競合的にFasR-FasL相互作用を妨げる[6]。
シグナル伝達
[編集]Fas(受容体)はリガンドと結合して細胞死誘導シグナル伝達複合体(DISC)を形成する。接触している細胞の細胞膜に結合しているFasリガンド三量体はFas受容体の三量体化を引き起こす。この三量体化はFas抗体でも同様に発生するので、Fasシグナル伝達の研究では、このアポトーシスシグナルは信頼されない[訳語疑問点]。この目的のために、in vitro 研究で使用できる巧妙な抗体三量化法が採用されている。
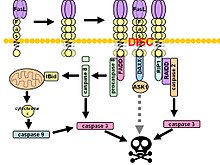
機能
[編集]
FasR-FasL結合に始まるアポトーシスは、免疫系の制御において下記の様な重要な役割を持つ。
- T細胞の恒常性:T細胞が活性化するとその表面にFasリガンドが発現する。T細胞はクローン性増殖の間はFas誘導性アポトーシスに耐性であるが、活性化されるとその期間の長さに従ってFas感受性が高くなり、最終的に活性化誘導細胞死(AICD)に至る。この過程は過剰な免疫反応を防止し、自己反応性T細胞を除去するために必要である。突然変異でFasR-FasL相互作用を欠いたヒトおよびマウスでは、異常なT細胞が蓄積し、リンパ節腫脹、脾腫、エリテマトーデスを来たす。
- 細胞傷害性T細胞の活性:Fas誘導性アポトーシスおよびパーフォリン経路は外来性の抗原を提示している細胞傷害性T細胞誘導性細胞死の二大経路である[7]。
- 免疫特権:角膜や精巣等の免疫特権領域に存在する細胞はFasリガンドを発現し、浸潤リンパ球のアポトーシスを誘導する。これは、身体が免疫特権の確立と維持に用いている多くのメカニズムの一つである。
- 胎児組織への母体寛容:Fasリガンドは母体と胎児間の白血球移動の阻止に貢献しているが、FasR-FasL系の欠陥が原因となる妊娠異常は知られていない。
- 腫瘍の生存維持:腫瘍はFasリガンドを過剰発現することがあり、浸潤リンパ球をアポトーシスに導き、免疫系の攻撃を躱している[8]。Fasリガンドは化学療法後にしばしば増加し、アポトーシス耐性を獲得する。
疾患での役割
[編集]Fas誘導性アポトーシスの欠損により、腫瘍発生や腫瘍の薬剤耐性が発生する。Fasの生殖細胞系列変異は小児のアポトーシス異常である自己免疫性リンパ増殖症候群(ALPS)に関係がある。
相互作用
[編集]Fasリガンドは下記の蛋白質と相互作用する。
関連項目
[編集]出典
[編集]- ^ a b c GRCh38: Ensembl release 89: ENSG00000117560 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000000817 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ Yonehara S, Ishii A, Yonehara M (1989). “A cell-killing monoclonal antibody (anti-Fas) to a cell surface antigen co-downregulated with the receptor of tumor necrosis factor.”. J Exp Med 169 (5): 1747-56. doi:10.1084/jem.169.5.1747. PMC 2189304. PMID 2469768.
- ^ “Death and decoy receptors and p53-mediated apoptosis”. Leukemia 14 (8): 1509–1513. (2000). doi:10.1038/sj.leu.2401865. PMID 10942251.
- ^ “Cytotoxic T cells”. J. Invest. Dermatol. 126 (1): 32–41. (2006). doi:10.1038/sj.jid.5700001. PMID 16417215.
- ^ “Tumor counterattack: fact or fiction?”. Cancer Immunol. Immunother. 54 (11): 1127–1136. (2005). doi:10.1007/s00262-005-0680-7. PMID 15889255.
- ^ a b c d “Cytoskeleton-mediated death receptor and ligand concentration in lipid rafts forms apoptosis-promoting clusters in cancer chemotherapy”. J. Biol. Chem. 280 (12): 11641–7. (March 2005). doi:10.1074/jbc.M411781200. PMID 15659383.
- ^ a b c “Induction of TNF receptor I-mediated apoptosis via two sequential signaling complexes”. Cell 114 (2): 181–90. (July 2003). doi:10.1016/s0092-8674(03)00521-x. PMID 12887920.
- ^ “CD95 (APO-1/Fas) linkage to the actin cytoskeleton through ezrin in human T lymphocytes: a novel regulatory mechanism of the CD95 apoptotic pathway”. EMBO J. 19 (19): 5123–34. (October 2000). doi:10.1093/emboj/19.19.5123. PMC 302100. PMID 11013215.
- ^ a b c “Identification of interaction partners of the cytosolic polyproline region of CD95 ligand (CD178)”. FEBS Lett. 519 (1-3): 50–8. (May 2002). doi:10.1016/s0014-5793(02)02709-6. PMID 12023017.
- ^ a b “Multiple interactions of the cytosolic polyproline region of the CD95 ligand: hints for the reverse signal transduction capacity of a death factor”. FEBS Lett. 509 (2): 255–62. (December 2001). doi:10.1016/s0014-5793(01)03174-x. PMID 11741599.
- ^ “Interaction of peptides derived from the Fas ligand with the Fyn-SH3 domain”. FEBS Lett. 373 (3): 265–8. (October 1995). doi:10.1016/0014-5793(95)01051-f. PMID 7589480.
- ^ “Identification of amino acid residues important for ligand binding to Fas”. J. Exp. Med. 185 (8): 1487–92. (April 1997). doi:10.1084/jem.185.8.1487. PMC 2196280. PMID 9126929.
- ^ “Characterization of Fas (Apo-1, CD95)-Fas ligand interaction”. J. Biol. Chem. 272 (30): 18827–33. (July 1997). doi:10.1074/jbc.272.30.18827. PMID 9228058.
- ^ “A newly identified member of tumor necrosis factor receptor superfamily (TR6) suppresses LIGHT-mediated apoptosis”. J. Biol. Chem. 274 (20): 13733–6. (May 1999). doi:10.1074/jbc.274.20.13733. PMID 10318773.
- ^ “Modulation of dendritic cell differentiation and maturation by decoy receptor 3”. J. Immunol. 168 (10): 4846–53. (May 2002). doi:10.4049/jimmunol.168.10.4846. PMID 11994433.
- ^ “Genomic amplification of a decoy receptor for Fas ligand in lung and colon cancer”. Nature 396 (6712): 699–703. (December 1998). doi:10.1038/25387. PMID 9872321.
関連資料
[編集]- “Fas ligand/Fas system in the brain: regulator of immune and apoptotic responses”. Brain Res. Brain Res. Rev. 44 (1): 65–81. (January 2004). doi:10.1016/j.brainresrev.2003.08.007. PMID 14739003.
- “HIV/SIV escape from immune surveillance: focus on Nef”. Curr. HIV Res. 2 (2): 141–51. (2004). doi:10.2174/1570162043484924. PMID 15078178.