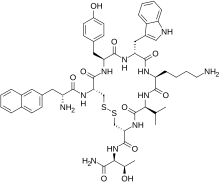
ランレオチド
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Somatuline |
| Drugs.com | monograph |
| ライセンス | US FDA:リンク |
| 胎児危険度分類 | |
| 法的規制 | |
| 投与経路 | Intramuscular, subcutaneous |
| 薬物動態データ | |
| 生物学的利用能 | Approximately 80% |
| 血漿タンパク結合 | 78% |
| 代謝 | In GI tract |
| 半減期 | 2 hours (immediate release) 5 days (sustained release) |
| 排泄 | Mostly biliary |
| 識別 | |
| CAS番号 |
108736-35-2 |
| ATCコード | H01CB03 (WHO) |
| PubChem | CID: 71349 |
| IUPHAR/BPS | 2031 |
| ChemSpider |
64450 |
| UNII |
0G3DE8943Y |
| ChEMBL |
CHEMBL1201185 |
| 化学的データ | |
| 化学式 | C54H69N11O10S2 |
| 分子量 | 1096.33 g/mol 1156.380 g/mol (acetate) |
| |
| |
ランレオチド(Lanreotide)は、先端巨大症および神経内分泌腫瘍に起因する症状(特にカルチノイド症候群)の管理に使用される医薬品である。オクトレオチドと同様に、ソマトスタチンの長時間作用型アナログ製剤に該当する。配列は、H-D-2Nal[※ 1]-Cys(1)-Tyr-D-Trp-Lys-Val-Cys(1)-Thr-NH2 である。
- ^ 2-Naphthyl-D-alanine
日本、米国、英国、オーストラリア、カナダなど数カ国で販売されている。米国では2007年8月30日に販売許可を取得している[1]。日本では2017年7月3日に承認を取得している[2]。
効能・効果[編集]
- 甲状腺刺激ホルモン産生下垂体腫瘍
- 膵・消化管神経内分泌腫瘍
ランレオチドは、下垂体成長ホルモン分泌性腫瘍および非下垂体成長ホルモン分泌性腫瘍による先端巨大症の治療、および神経内分泌腫瘍(特にカルチノイド腫瘍およびVIP産生腫瘍)による症状の管理に使用される。ランレオチドは、米国およびカナダでは先端巨大症の治療にのみ適応承認されている。また英国では、下垂体に発生する稀な腫瘍であるTSH分泌性の甲状腺栄養腺腫(thyrotrophic adenoma)にも適応がある[3]。
ランレオチドは、非内分泌腫瘍に対しても活性を示すので、他のソマトスタチン類似体と共に、一般的な抗腫瘍剤としての可能性が検討されている[4][5]。
2014年12月、米国FDAは、切除不能、高・中分化、局所進行または転移性の膵消化管神経内分泌腫瘍(GEP-NET)患者の治療薬としてランレオチドを承認した[6]。
多嚢胞性肝疾患に使用すると、平均して264mLの容積を減らすことが判明している[要出典]。
薬理[編集]
ランレオチドは、成長ホルモン、甲状腺刺激ホルモン(TSH)、インスリン、グルカゴンなどのホルモンの分泌を阻害する天然の抑制性ホルモンであるソマトスタチンの合成アナログ製剤である。ランレオチドは、ソマトスタチンと同じ受容体に結合するが、末梢の受容体への親和性が高く、同様の作用を有している。しかし、ソマトスタチンが体内で速やかに(数分以内に)分解されるのに対し[7]、ランレオチドは半減期が長く、効果が遥かに長く持続するのが特徴である。
副作用[編集]
重大な副作用として、徐脈(3.7%)が知られている[8]。
主な副作用は、注射部位の軽度から中等度の痛みと、下痢、嘔気、嘔吐等の胃腸障害である。ランレオチドの長期使用により、胆石を形成した事例がある[3]。
自己集合性[編集]
ランレオチドは、直径24.4nmの単分散ナノチューブに自発的に自己組織化する事が示されており[9]、その後、いくつかの生物物理学的研究において、実り多き多目的モデルシステムとして使用されてきた。
参考資料[編集]
- ^ "FDA Approves New Drug to Treat Rare Disease, Acromegaly" (Press release). U.S. Food and Drug Administration. 30 August 2007. 2007年9月6日閲覧。
- ^ “国内ニュース:(祝)膵・消化管神経内分泌腫瘍にランレオチドが承認される”. www.pancan.jp. 2021年6月16日閲覧。
- ^ a b “Somatuline LA”. electronic Medicines Compendium (2003年9月17日). 2006年9月24日時点のオリジナルよりアーカイブ。2007年3月2日閲覧。
- ^ “Role of somatostatin analogs in the clinical management of non-neuroendocrine solid tumors”. Anticancer Drugs 17 (6): 601–8. (2006). doi:10.1097/01.cad.0000210335.95828.ed. PMID 16917205.
- ^ “Rationale for the use of somatostatin analogs as antitumor agents”. Ann Oncol 17 (12): 1733–42. (2006). doi:10.1093/annonc/mdl105. PMID 16801334.
- ^ “FDA Approves Lanreotide Injection for GEP-NETs” (2014年). 2021年6月16日閲覧。
- ^ “Biochemical and functional properties of somatostatin receptors”. J Neurochem 58 (6): 1987–96. (1992). doi:10.1111/j.1471-4159.1992.tb10938.x. PMID 1315373.
- ^ “ソマチュリン皮下注60mg/ソマチュリン皮下注90mg/ソマチュリン皮下注120mg 添付文書”. www.info.pmda.go.jp. PMDA. 2021年6月16日閲覧。
- ^ “Biomimetic organization: Octapeptide self-assembly into nanotubes of viral capsid-like dimension”. Proceedings of the National Academy of Sciences of the United States of America 100 (18): 10258–62. (2003). Bibcode: 2003PNAS..10010258V. doi:10.1073/pnas.1730609100. PMC 193548. PMID 12930900.
