肥大型心筋症
| 肥大型心筋症 | |
|---|---|
| 別称 | Asymmetric septal hypertrophy; idiopathic hypertrophic subaortic stenosis;[1] hypertrophic obstructive cardiomyopathy (HOCM) |
 | |
| 概要 | |
| 診療科 | Cardiology |
| 症状 | Frequently none, feeling tired, leg swelling, shortness of breath, chest pain, fainting[2][3] |
| 原因 | Genetics, Fabry disease, Friedreich's ataxia, certain medications[4][5] |
| 診断法 | Electrocardiogram, echocardiogram, stress testing, genetic testing[6] |
| 鑑別 | Hypertensive heart disease, aortic stenosis, athlete's heart[4] |
| 合併症 | Heart failure, irregular heartbeat, sudden cardiac death[7][8] |
| 使用する医薬品 | Beta blockers, verapamil, disopyramide[9] |
| 治療 | Medications, implantable cardiac defibrillator, surgery (transaortic septal myectomy)[6][9] |
| 予後 | Less than 1% per year risk of death (with treatment)[10] |
| 頻度 | Up to 1 in 200 people[9] |
| 分類および外部参照情報 | |
| Patient UK | 肥大型心筋症 |
肥大型心筋症 (ひだいがたしんきんしょう、英: Hypertrophic cardiomyopathy、HCM) は、明確な原因なく心臓の一部が肥大する心血管疾患である[9]。症状は、無症状な場合から、疲労、脚のむくみ、呼吸困難などさまざまである[3]。また、胸痛や失神を起こす場合もある[3]。合併症には、心不全、不整脈、心停止などがあげられる[7][8]。
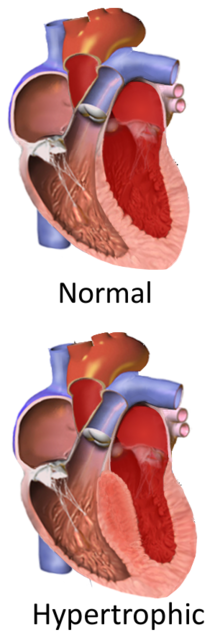
HCMは、親からの遺伝によるものが最も一般的である[5]。心筋タンパク質の生成に関与する遺伝子の突然変異によることが多い[5]。他の原因には、ファブリー病、フリードライヒ運動失調症、タクロリムスなどの特定の医薬品、などがあげられる[4]。HCMは、心筋症の一種であり、主に心筋に影響を与える疾患である[7]。心筋が固くなることにより心臓から血液を送りだす能力が低下し、肥厚した心室中隔により左心室から大動脈への血液の流れが妨げられ、僧帽弁が弱くなる可能性がある[2][9]。
HCMは、心電図と心臓超音波検査によって診断される[6]。この他には、ストレス検査や遺伝子診断などの検査がある[6]。親戚のスクリーニング検査を勧められる場合がある[11]。一般的な初期治療には、ベータ遮断薬、ベラパミル、ジソピラミドが用いられる[9]。左心室の容積と流出量を減少させる可能性のある利尿薬の使用には注意が必要である[12]。特定の種類の不整脈には、植込み型除細動脈の使用が勧められる場合がある[6]。これらの治療で改善されない場合には、中隔心筋切除術や心臓移植などの手術が行われる場合がある[2][13]。治療を受けた場合の死亡リスクは年間1%未満である[10]。 HCMの罹患率は最大200人に1人である[9][13]。男女ともに同じ割合で罹患する[14]。あらゆる年齢層の人が罹患する可能性がある[14]。この疾患の最初の現代的記述は、1958年にドナルド・ティアレによって説明されたものである[15][16]。
出典
[編集]- ^ “Other Names for Cardiomyopathy”. NHLBI (June 22, 2016). 28 July 2016時点のオリジナルよりアーカイブ。31 August 2016閲覧。
- ^ a b c AHA (13 May 2022). “Hypertrophic Cardiomyopathy (HCM)” (英語). www.heart.org. American Heart Association. 6 October 2022時点のオリジナルよりアーカイブ。13 October 2022閲覧。
- ^ a b c “What Are the Signs and Symptoms of Cardiomyopathy?”. NHLBI. National Heart Lung and Blood Institute (24 March 2022). 28 July 2016時点のオリジナルよりアーカイブ。13 October 2022閲覧。
- ^ a b c Ferri, Fred F. (2017). Ferri's Clinical Advisor 2018 E-Book: 5 Books in 1. Elsevier Health Sciences. p. 246. ISBN 9780323529570. オリジナルの2017-11-10時点におけるアーカイブ。 2017年11月10日閲覧。
- ^ a b c “What Causes Cardiomyopathy?”. NHLBI (22 June 2016). 5 October 2017時点のオリジナルよりアーカイブ。10 November 2017閲覧。
- ^ a b c d e Ommen, Steve R.; Mital, Seema; Burke, Michael A.; Day, Sharlene M.; Deswal, Anita; Elliott, Perry; Evanovich, Lauren L.; Hung, Judy et al. (22 December 2020). “2020 AHA/ACC Guideline for the Diagnosis and Treatment of Patients With Hypertrophic Cardiomyopathy: Executive Summary”. Journal of the American College of Cardiology 76 (25): 3022–3055. doi:10.1016/j.jacc.2020.08.044. PMID 33229115 14 October 2022閲覧。.
- ^ a b c “What Is Cardiomyopathy?”. NHLBI (22 June 2016). 10 November 2017時点のオリジナルよりアーカイブ。10 November 2017閲覧。
- ^ a b “Genetics of sudden cardiac death”. Current Cardiology Reports 13 (5): 364–76. (October 2011). doi:10.1007/s11886-011-0209-y. PMID 21789574.
- ^ a b c d e f g Cui, Hao; Schaff, Hartzell V. (2020). “80. Hypertrophic cardiomyopathy”. In Raja, Shahzad G. (英語). Cardiac Surgery: A Complete Guide. Switzerland: Springer. pp. 735-748. ISBN 978-3-030-24176-6. オリジナルの2022-10-13時点におけるアーカイブ。 2022年10月13日閲覧。
- ^ a b “Hypertrophic cardiomyopathy: present and future, with translation into contemporary cardiovascular medicine”. Journal of the American College of Cardiology 64 (1): 83–99. (July 2014). doi:10.1016/j.jacc.2014.05.003. PMID 24998133.
- ^ Phelan, Dermot M.; Symanski, John (2021). “7. Hypertrophic cardiomyopathy”. In EngelEngel, David J.; Phelan, Dermot M. (英語). Sports Cardiology: Care of the Athletic Heart from the Clinic to the Sidelines. Switzerland: Springer. pp. 97-110. ISBN 978-3-030-69383-1. オリジナルの2022-10-14時点におけるアーカイブ。 2022年10月14日閲覧。
- ^ Shah (29 April 2022). “Hypertrophic Cardiomyopathy Treatment & Management: Approach Considerations, Left Ventricular Myomectomy and Mitral Valve Replacement, Pacemaker Implantation”. emedicine. 13 October 2022時点のオリジナルよりアーカイブ。13 October 2022閲覧。
- ^ a b Ralph-Edwards, Anthony; Vanderlaan, Rachel D.; Bajona, Pietro (July 2017). “Transaortic septal myectomy: techniques and pitfalls”. Annals of Cardiothoracic Surgery 6 (4): 410–415. doi:10.21037/acs.2017.07.08. ISSN 2225-319X. PMID 28944183 2022年10月13日閲覧。.
- ^ a b “Types of Cardiomyopathy”. NHLBI (22 June 2016). 4 October 2017時点のオリジナルよりアーカイブ。10 November 2017閲覧。
- ^ “Asymmetrical hypertrophy of the heart in young adults”. British Heart Journal 20 (1): 1–8. (January 1958). doi:10.1136/hrt.20.1.1. PMC 492780. PMID 13499764.
- ^ “From Teare to the present day: a fifty year odyssey in hypertrophic cardiomyopathy, a paradigm for the logic of the discovery process”. Revista Espanola de Cardiologia 61 (12): 1239–44. (December 2008). doi:10.1016/S1885-5857(09)60050-5. PMID 19080961 2017年2月6日閲覧。.
