細胞分裂

細胞分裂(さいぼうぶんれつ、英: cell division)は、親細胞が2つの娘細胞に分裂する過程である[1]。通常、細胞分裂は大きな細胞周期の一部であり、細胞は分裂する前に成長し、遺伝情報を担う染色体が複製され、その後細胞質を分離する段階を含む。核を持たない原核生物では、二分裂により親細胞と同一の遺伝情報をもった娘細胞を生成する。核を持つ真核生物では、細胞分裂は、親細胞と遺伝的に同一の娘細胞を形成する有糸分裂と、有性生殖のために単数体の配偶子を形成する減数分裂の2種類に大別される。
細胞分裂の主要な目的は、元の細胞のゲノムを存続させることであり、分裂前に染色体に保存されているゲノム情報が複製され、それぞれの子細胞に均等に分割されなくてはならない[2]。世代間のゲノム情報の一貫性を確保するために、さまざまな細胞基盤が関与している[3][4][5]。細胞周期を適切に進行させるために、さまざまなチェックポイントが設けられ、DNAの損傷が検出され、修復される[6]。これらのチェックポイントでは、サイクリン-CDK複合体を阻害することにより、細胞周期の進行を止めることができる。
アメーバのような単細胞の微生物では、1回の細胞分裂は生殖に相当し、新規の生物を生み出す。より大きなスケールでは、挿し木から成長する植物のように、有糸分裂によって多細胞生物が子孫を作ることができる。有性生殖生物は、減数分裂で作られた2つの配偶子が融合した単細胞の接合子から発生することができ[7][8]、接合子から成体へと成長した後も、有糸分裂による細胞分裂で自己を再生したり、修復することができる[9]。ヒトの体では、一生の間に約一京回の細胞分裂が行われる[10]。
細胞分裂の様式
[編集]
二分裂
[編集]原核生物(細菌と古細菌)では通常、遺伝物質が2つの娘細胞に均等に配分される二分裂と呼ばれる栄養細胞分裂が行われるほか、出芽のような別の分裂様式も観察されている。二分裂は、細胞分裂前の紡錘体の形成やクロマチン凝縮を伴わない細胞分裂の原始的な形態で、無糸分裂(英: amitosis)とも呼ばれる[11]。どのような種でも、すべての細胞分裂においてDNA複製が1回行われる。細菌の場合、ディビソームというタンパク質複合体が、細胞分裂、分裂時の内膜と外膜の収縮、そして分裂部位でのペプチドグリカン細胞壁の合成を担う。チューブリン様タンパク質であるFtsZは、細胞分裂のための収縮環形成に重要な役割を果たしている[12]。
有糸分裂
[編集]ヒトを含むほとんどの真核生物は、核に複数の染色体を持っている。有糸分裂(英: mitosis)では、それぞれの染色体が複製され、新しい2つの核に分配され、染色体の総数が維持された遺伝的に同一の娘細胞を生成する。各染色体のコピーがそれぞれの娘細胞に確実に分離されるように、有糸分裂では紡錘体が形成される。染色体は、線路を走る車両のように、細長い微小管に沿って移動する。一般に、有糸分裂が起こる前にはDNAが複製されるS期(合成期)がある。有糸分裂の後には細胞質分裂が続き、親細胞の細胞成分(細胞質・細胞小器官・細胞膜など)が、2つの新しい娘細胞に均等に分配される。有糸分裂を構成するそれぞれの段階を総称して動物の細胞周期のM期(有糸分裂期)、すなわち親細胞が遺伝的に同一の2つの娘細胞に分裂する過程が定義される。
減数分裂
[編集]減数分裂(英: meiosis)の場合、染色体の数が親細胞の各2本から、娘細胞の各1本へと減少する[13]。減数分裂では連続した2回の分裂を経て、4つの単数体の娘細胞が作られる。第一減数分裂では、相同染色体が分離され、それぞれの娘細胞は各染色体のコピーを1つずつ持つようになる。これらの染色体は細胞分裂の前に複製されて姉妹染色分体を形成していて第二減数分裂で分離される[14]。ヒトは二倍体であり、細胞は父親と母親からそれぞれ1本ずつ2本一組の染色体を持つ。ヒトの性細胞(配偶子)は減数分裂によって生成する。精子の場合、計2回の細胞質分裂が連続して行われ、それぞれが通常の半分の染色体数を持った合計4つの細胞を生成する。卵巣での卵子形成の場合は状況が異なり、分離された4組の染色体のうちの1組が大きな卵細胞に配置され、精子細胞からのDNAと結合する準備が整う。
真核生物の細胞分裂
[編集]核を持つ真核生物の場合、細胞分裂の過程は、核を持たない原核生物よりも複雑である。ヒトのような高等動物の場合、ほとんどの細胞は親細胞と遺伝的に同一の娘細胞を形成する有糸分裂によって生成するが、重要な例外として、有性生殖のための単数体の配偶子(精子と卵細胞)は減数分裂によって形成される。有糸分裂と減数分裂とは、細胞のライフサイクルのある時点で、有性生殖の過程で行われる。どちらの分裂様式も、真核生物の最後の共通祖先に存在していたと考えられている。
真核生物の細胞周期
[編集]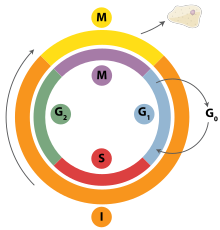
細胞が2つの娘細胞に分裂するまでに起こる一連の段階を細胞周期(英: cell cycle)あるいは細胞分裂周期(英: cell-division cycle)という。これらの段階には、遺伝情報を担うデオキシリボ核酸(DNA)の複製が含まれ、続く細胞質分裂と呼ばれる過程で、細胞質・染色体・その他の構成成分が2つの娘細胞に分割される。
間期
[編集]間期(英: interphase)とは、細胞が有糸分裂、減数分裂、細胞質分裂の前に必ず通る過程である[15]。間期は主にG1期、S期、G2期という3つの段階からなり、この間に細胞は細胞分裂の準備をする。
G1期
[編集]S期
[編集]G2期
[編集]- G2期の間、細胞は、有糸分裂が始まって紡錘体が合成されるM期に入る前に急速に成長し、タンパク質を合成して最終の成長段階を経る。
M期
[編集]
間期 (G₂): 細胞は核分裂の準備をし、細胞分裂のための微小管を作るタンパク質が合成される。
前期: DNAを含むクロマチンが凝集して染色体を形成し、中心体が細胞の対極に移動する。
前中期: 核膜が破壊され、微小管が動原体に結合する。染色体は細胞の中期板に向かって移動する。
中期: 染色体は細胞の中央に並び、セントロメアで紡錘糸に結合する。
後期: 姉妹染色分体は個々の染色体に分離し、引き離される。
終期と細胞質分裂: 染色体は凝縮を解除し、新しく形成された核膜に囲まれる。細胞質分裂は一般的に終期と重なる。
M期(英: mitomic phase、有糸分裂期)は細胞の種類によって有糸分裂か減数分裂のどちらかが行われる。生殖細胞(または配偶子)では減数分裂を行い、体細胞では有糸分裂を行う。M期を正常に進行した細胞は、続く細胞質分裂によって分裂することができる。
有糸分裂
[編集]前期
[編集]- 前期(英: prophase)は細胞分裂の最初の段階である。この段階は核膜が破壊され始め、クロマチンの長い鎖が凝縮して染色体と呼ばれる、より短く目に見える鎖が形成され、核小体が消失し、2つの中心体から有糸分裂紡錘体が形成され始める[18]。染色体の整列と分離に関与する微小管は、紡錘体および紡錘糸と呼ばれる。染色体は顕微鏡でも見ることができ、セントロメアで結合している。減数分裂においては、この凝縮と整列の時期に、相同染色体が同じ部位で二本鎖DNAの切断を受け、その後、断片化した親DNA鎖が非親DNA鎖の組み合わせに組み換えられる(乗換えと呼ばれる)[19]。この過程は高度に保存されたSpo11タンパク質によって引き起こされ、DNA複製や転写に関与するトポイソメラーゼと同様の機構であることが知られている[20]。
前中期
[編集]- 前中期(英: prometaphase)は細胞分裂の第二段階である。この段階は、核膜が完全に破壊され、さまざまな構造が細胞質に露出することから始まる。この破壊によって、中心体から伸長する紡錘体が、姉妹染色分体上の動原体(キネトコア)に結合できるようになる。紡錘体が姉妹染色分体上の動原体と確実に結合することで、後期の段階で染色体を誤りなく分離できるようになる[21]。
中期
[編集]- 中期(英: metaphase)では、染色体のセントロメアが、2つの中心体極から等距離にある仮想上の線である中期板(赤道板とも呼ぶ)の上に整列し、コヒーシンと呼ばれる複合体によってつなぎ止められる。微小管形成中心(MTOC)が両染色体のセントロメアを押し引きすることで、染色体は細胞の中央に移動して整列する。この時点で染色体はまだ凝縮中であり、最もコイル状に凝縮する一歩手前にあり、紡錘糸はすでに動原体に結合している[22]。この時期は、動原体を除くすべての微小管は、後期への進行を推進する不安定な状態にある[23]。この時点で染色体は、それらが結合している紡錘体に向かって細胞の対極に分裂する準備が整う[24]。中期にある紡錘体チェックポイントは、各染色体が紡錘体に正しく結合するまで後期への移行を阻止する。
後期
[編集]- 後期(英: anaphase)は、分裂板で染色体が整列した後に起こり、細胞周期の非常に短い段階である。動原体は、紡錘体に結合するまで後期抑制シグナルを発する。最後の染色体が適切に整列して紡錘体に結合すると、その最終シグナルは消失し、後期への急激な移行を引き起こす[23]。この急激な移行は、後期促進複合体の活性化と、中期-後期移行に重要なタンパク質の分解を促すタグ付け機能によって引き起こされる。分解されるタンパク質の一つがセキュリンで、その分解によって姉妹染色分体をつなぎ止めているコヒーシンリングを切断するセパラーゼという酵素が放出され、染色体が分離する。染色体が細胞の中央に並んだ後、紡錘糸が染色体を引き離す[25]。染色体が分裂して、姉妹染色分体は細胞の対極に移動する[26]。姉妹染色分体が引き離されるにつれて、細胞と原形質は非動原体微小管によって伸長される[27]。さらにこの段階では、Cdh-1との結合による後期促進複合体の活性化により、有糸分裂サイクリンの分解が始まる[28]。
終期
[編集]- 終期(英: telophase)は細胞周期の最終段階である。分裂溝が形成して細胞質とクロマチンが分割される細胞質分裂が起こる。これは、各極に集められたクロマチンの周囲に新しく合成された核膜の形成によって達成される。クロマチンが間期の穏やかな状態に戻ると、核小体が再形成される[29][30]。細胞内容物の分裂は必ずしも均等ではなく、4つの娘細胞のうちの1つが大部分を所有する卵母細胞の形成に見られるように、細胞の種類によって異なることがある[31]。
細胞質分裂
[編集]細胞分裂の最終段階が細胞質分裂(英: cytokinesis)である。この段階では、有糸分裂または減数分裂の最後にある細胞質の分裂が起こる。分離は不可逆的で、2つの娘細胞が作られる。細胞分裂は細胞の運命を決定する上で重要な役割を果たしている。その結果、運命決定分子の量や濃度が全く異なる不均等な娘細胞につながる原因となる[32]。
動物では、細胞質分裂は収縮環の形成と、その後の分割で終了する。しかし植物では、その過程が異なる。まず細胞板が形成され、次に2つの娘細胞の間に細胞壁が発達する[要出典]。
分裂酵母(Schizosaccharomyces pombe)では、細胞質分裂はG1期に起こる[33]。
真核生物のチェックポイント
[編集]細胞周期チェックポイント
[編集]細胞周期にはチェックポイントがあり、細胞は成長段階をさらに進行させたり止めたりすることができる。その一つはG1期のG1/Sチェックポイントで、目的は適切な細胞サイズとDNAの損傷を調べることである。二番目はG2期のG2/Mチェックポイントで、細胞サイズとDNAの複製を調べる。最後のチェックポイントは中期にあり、染色体が有糸分裂紡錘体に正しく結合しているかを確かめる[34]。
各チェックポイントは、サイクリンとサイクリン依存性キナーゼというタンパク質によって制御される。間期はサイクリン量の増加にともなって進行する。サイクリンの量が増えるにつれ、サイクリン依存性キナーゼとサイクリンの結合が増し、細胞を間期へとさらに誘導する。サイクリンが頂点に達すると、このシステムによって細胞は間期から、有糸分裂、減数分裂、細胞質分裂が起こるM期へ移行する[35]。M期に入る細胞が通過しなければならない移行チェックポイントのうち、最も重要なのはG1/S移行チェックポイントである。もし細胞がこのチェックポイントを通過できなければ、細胞周期から抜けることになる[36]。
DNA損傷の修復
[編集]DNA損傷は細胞周期のさまざまな時点で検出され、修復される。G1/Sチェックポイント、G2/Mチェックポイント、および中期と後期の間のチェックポイントはすべて、DNA損傷を監視し、さまざまなサイクリン-CDK複合体を阻害することによって細胞分裂を停止させる。腫瘍抑制タンパク質p53は、G1/SチェックポイントとG2/Mチェックポイントで重要な役割を果たしている。活性化されたp53タンパク質は、細胞周期の停止、修復、アポトーシスに関与する多くのタンパク質の発現を引き起こす。p53は、G1/Sチェックポイントで細胞がDNA複製の準備が整っているかを確認し、G2/Mチェックポイントで細胞が有糸分裂に入る前にその内容を適切に複製していることを確認するなど、細胞増殖を抑制する働きをする[37]。
具体的には、DNA損傷があると、ATMキナーゼおよびATRキナーゼが活性化され、さまざまなチェックポイントキナーゼの活性化が促される[38]。これらのチェックポイントキナーゼはp53をリン酸化し、p53はDNA修復に関連する多くの酵素の産生を促す[39]。活性化されたp53は、p21タンパク質もアップレギュレートし、さまざまなサイクリン-CDK複合体を阻害する。これらのサイクリン-CDK複合体は、転写因子のE2Fファミリーに結合する腫瘍抑制因子である網膜芽細胞腫タンパク質(Rbタンパク質)をリン酸化する。このRbタンパク質の結合により、細胞が早期にS期に移行することはなくなるが、サイクリン-CDK複合体によってリン酸化されないとこのタンパク質は残存し、細胞は細胞周期のG1期で停止状態となる[40]。
DNAが損傷を受けた細胞は、BADがリン酸化されBcl2から解離するAktシグナル伝達経路を変化させることで、アポトーシスを阻害することができる。AktまたはBcl2の機能喪失変異によってこの経路が変化した場合、損傷を受けたDNAを持つ細胞はアポトーシスを受けざるを得なくなる[41]。DNA損傷を修復できない場合、活性化されたp53はアポトーシスによる細胞死を誘導することができる。これは、p53アポトーシスアップレギュレート調節因子(英: p53 upregulated modulator of apoptosis、PUMA)を活性化することで可能になる。PUMAは、抗アポトーシスBcl-2ファミリーメンバーを阻害することにより、アポトーシスを速やかに誘導するアポトーシス促進タンパク質である[42]。
細胞老化
[編集]多細胞生物では、細胞分裂によって老化した細胞を置き換える。しかし動物によっては、細胞分裂が最終的に停止する仕組みを持つものもある。ヒトの場合、平均52回の分裂後にこれが起こり、ヘイフリック限界として知られている。この細胞の現象は細胞老化(英: cellular senescence)と呼ばれる。細胞分裂のたびに、染色体の末端にあるテロメア(染色体DNAの分解を防ぐDNAの保護配列)が短くなる。ヒトでは、この短縮は加齢に関連した病気や寿命の短縮といった悪影響に関連している[43][44]。一方、がん細胞では、まったくと言っていいほど、このような分解はしないと考えられている。がん細胞に多く存在するテロメラーゼと呼ばれる酵素複合体は、テロメアのDNA反復配列を合成することでテロメアを再構築し、細胞分裂が無期限に継続することを可能にする[45]。
非合成分裂
[編集]2022年、科学者たちは、ゼブラフィッシュの幼体の表皮にある扁平上皮細胞で、非合成分裂(英: asynthetic fission)と呼ばれる新しい種類の細胞分裂を発見した[46]。ゼブラフィッシュの幼体が成長するにつれ、皮膚細胞は急速に増加するゼブラフィッシュの表面積を素早く覆わなければならない。これらの皮膚細胞は(有糸分裂のS期で)DNAを複製することなく分裂するため、最大50%の細胞がゲノムサイズを縮小する。これらの細胞はその後、標準的なDNA量を持つ細胞で置き換えられる。科学者たちは、他の脊椎動物でもこのような分裂が見つけられると期待している。
研究の歴史
[編集]
1835年、ドイツの植物学者フーゴー・フォン・モールが、緑藻 Cladophora glomerata の研究中に、顕微鏡下で細胞分裂を初めて発見した[47]。
1943年、クルト・ミシェル(Kurt Michel)が[48]、位相差顕微鏡を使用して細胞分裂を初めて撮影した[49]。
参照項目
[編集]- 細胞融合 - 単一核細胞が結合して多核細胞(合胞体)を形成する細胞過程
- 配偶子接合 - 性が異なる2つの単細胞配偶子の性的融合
- 細胞成長 - 細胞質、核、小器官の体積を含む細胞の総質量の増加
- サイクリン依存性キナーゼ - 細胞周期を調節する酵素
- 不安定細胞 - 生涯を通じて増殖と分裂を続ける細胞
- 分裂期細胞死 - 潜在的にがん化した細胞の増殖を防ぐための細胞機構
- 多核体 - 細胞質分裂を伴わない多核細胞
- 卵割 - 受精後の胚の初期発生における細胞分裂
脚注
[編集]- ^ Martin EA, Hine R (2020). A dictionary of biology (6th ed.). Oxford: Oxford University Press. ISBN 9780199204625. OCLC 176818780
- ^ Golitsin, Yuri N.; Krylov, Mikhail C. C. (2010). Cell division : theory, variants, and degradation. New York: Nova Science Publishers. pp. 137. ISBN 9781611225938. OCLC 669515286
- ^ Fletcher, Daniel A.; Mullins, R. Dyche (28 January 2010). “Cell mechanics and the cytoskeleton”. Nature 463 (7280): 485–492. Bibcode: 2010Natur.463..485F. doi:10.1038/nature08908. ISSN 0028-0836. PMC 2851742. PMID 20110992.
- ^ Li, Shanwei; Sun, Tiantian; Ren, Haiyun (27 April 2015). “The functions of the cytoskeleton and associated proteins during mitosis and cytokinesis in plant cells”. Frontiers in Plant Science 6: 282. doi:10.3389/fpls.2015.00282. ISSN 1664-462X. PMC 4410512. PMID 25964792.
- ^ Hohmann, Tim; Dehghani, Faramarz (18 April 2019). “The Cytoskeleton—A Complex Interacting Meshwork”. Cells 8 (4): 362. doi:10.3390/cells8040362. ISSN 2073-4409. PMC 6523135. PMID 31003495.
- ^ “10.2 The Cell Cycle - Biology 2e | OpenStax” (英語). openstax.org (28 March 2018). 2020年11月24日閲覧。
- ^ Gilbert, Scott F. (2000). “Spermatogenesis”. Developmental Biology (6th ed.). Sinauer Associates
- ^ Gilbert, Scott F. (2000). “Oogenesis”. Developmental Biology (6th ed.). Sinauer Associates
- ^ Maton, Anthea (1997). Cells : building blocks of life (3rd ed.). Upper Saddle River, N.J.: Prentice-Hall. pp. 70–74. ISBN 978-0134234762. OCLC 37049921
- ^ Quammen, David (April 2008). “Contagious Cancer”. Harper's Magazine. ISSN 0017-789X 2019年4月14日閲覧。
- ^ Tippit, D. H.; Pickett-Heaps, J. D. (1976-07-01). “Apparent amitosis in the binucleate dinoflagellate Peridinium Balticum”. Journal of Cell Science 21 (2): 273–289. doi:10.1242/jcs.21.2.273. ISSN 0021-9533. PMID 987046.
- ^ Cell Division: The Cycle of the Ring, Lawrence Rothfield and Sheryl Justice, CELL, DOI
- ^ Griffiths AJ (2012). Introduction to genetic analysis (10th ed.). New York: W.H. Freeman and Co.. ISBN 9781429229432. OCLC 698085201
- ^ Gilbert, Scott F. (2000), “Meiosis” (英語), Developmental Biology. 6th edition (Sinauer Associates) 2023年9月8日閲覧。
- ^ Marieb, Elaine Nicpon (2000). Essentials of human anatomy and physiology (6th ed.). San Francisco: Benjamin Cummings. ISBN 978-0805349405. OCLC 41266267
- ^ Pardee AB (November 1989). “G1 events and regulation of cell proliferation”. Science 246 (4930): 603–8. Bibcode: 1989Sci...246..603P. doi:10.1126/science.2683075. PMID 2683075.
- ^ Morgan, David Owen (2007). The cell cycle : principles of control. London: New Science Press. ISBN 9780199206100. OCLC 70173205
- ^ Schermelleh L, Carlton PM, Haase S, Shao L, Winoto L, Kner P, Burke B, Cardoso MC, Agard DA, Gustafsson MG, Leonhardt H, Sedat JW (June 2008). “Subdiffraction multicolor imaging of the nuclear periphery with 3D structured illumination microscopy”. Science 320 (5881): 1332–6. Bibcode: 2008Sci...320.1332S. doi:10.1126/science.1156947. PMC 2916659. PMID 18535242.
- ^ Lewontin, Richard C.; Miller, Jeffrey H.; Gelbart, William M.; Griffiths, Anthony J.F. (1999). “The Mechanism of Crossing-Over”. Modern Genetic Analysis.
- ^ Keeney, Scott (2001). Mechanism and control of meiotic recombination initiation. Current Topics in Developmental Biology. 52. Elsevier. pp. 1–53. doi:10.1016/s0070-2153(01)52008-6. ISBN 9780121531522. PMID 11529427
- ^ “Prometaphase - an overview | ScienceDirect Topics”. www.sciencedirect.com. 2023年11月21日閲覧。
- ^ “Researchers Shed Light On Shrinking Of Chromosomes”. ScienceDaily. 2019年4月14日閲覧。
- ^ a b Walter, Peter; Roberts, Keith; Raff, Martin; Lewis, Julian; Johnson, Alexander; Alberts, Bruce (2002). “Mitosis”. Molecular Biology of the Cell (4th ed.). Garland Science
- ^ Elrod, Susan (2010). Schaum's outlines : genetics (5th ed.). New York: Mcgraw-Hill. pp. 8. ISBN 9780071625036. OCLC 473440643
- ^ Brooker AS, Berkowitz KM (2014). “The Roles of Cohesins in Mitosis, Meiosis, and Human Health and Disease”. Cell Cycle Control. Methods in Molecular Biology. 1170. New York: Springer. pp. 229–66. doi:10.1007/978-1-4939-0888-2_11. ISBN 9781493908875. PMC 4495907. PMID 24906316
- ^ “The Cell Cycle”. www.biology-pages.info. 2019年4月14日閲覧。
- ^ Urry LA, Cain ML, Jackson RB, Wasserman SA, Minorsky PV, Reece JB (2014). Campbell Biology in Focus. Boston (Massachusetts): Pearson. ISBN 978-0-321-81380-0
- ^ Barford, David (2011-12-12). “Structural insights into anaphase-promoting complex function and mechanism” (英語). Philosophical Transactions of the Royal Society B: Biological Sciences 366 (1584): 3605–3624. doi:10.1098/rstb.2011.0069. PMC 3203452. PMID 22084387.
- ^ Dekker J (2014-11-25). “Two ways to fold the genome during the cell cycle: insights obtained with chromosome conformation capture”. Epigenetics & Chromatin 7 (1): 25. doi:10.1186/1756-8935-7-25. PMC 4247682. PMID 25435919.
- ^ Hetzer MW (March 2010). “The nuclear envelope”. Cold Spring Harbor Perspectives in Biology 2 (3): a000539. doi:10.1101/cshperspect.a000539. PMC 2829960. PMID 20300205.
- ^ Gilbert, Scott F. (2000). “Oogenesis”. Developmental Biology (6th ed.). Sinauer Associates
- ^ Guertin DA, Trautmann S, McCollum D (June 2002). “Cytokinesis in eukaryotes”. Microbiology and Molecular Biology Reviews 66 (2): 155–78. doi:10.1128/MMBR.66.2.155-178.2002. PMC 120788. PMID 12040122.
- ^ The Cell, G.M. Cooper; ed 2 NCBI bookshelf, The eukaryotic cell cycle, Figure 14.7
- ^ Molinari M (October 2000). “Cell cycle checkpoints and their inactivation in human cancer”. Cell Proliferation 33 (5): 261–74. doi:10.1046/j.1365-2184.2000.00191.x. PMC 6496592. PMID 11063129.
- ^ Lindqvist A, van Zon W, Karlsson Rosenthal C, Wolthuis RM (May 2007). “Cyclin B1-Cdk1 activation continues after centrosome separation to control mitotic progression”. PLOS Biology 5 (5): e123. doi:10.1371/journal.pbio.0050123. PMC 1858714. PMID 17472438.
- ^ Paulovich AG, Toczyski DP, Hartwell LH (February 1997). “When checkpoints fail”. Cell 88 (3): 315–21. doi:10.1016/S0092-8674(00)81870-X. PMID 9039258.
- ^ Senturk, Emir; Manfredi, James J. (2013). “p53 and Cell Cycle Effects After DNA Damage”. P53 Protocols. Methods in Molecular Biology (Clifton, N.J.). 962. pp. 49–61. doi:10.1007/978-1-62703-236-0_4. ISBN 978-1-62703-235-3. ISSN 1064-3745. PMC 4712920. PMID 23150436
- ^ Ding, Lei; Cao, Jiaqi; Lin, Wen; Chen, Hongjian; Xiong, Xianhui; Ao, Hongshun; Yu, Min; Lin, Jie et al. (2020-03-13). “The Roles of Cyclin-Dependent Kinases in Cell-Cycle Progression and Therapeutic Strategies in Human Breast Cancer”. International Journal of Molecular Sciences 21 (6): 1960. doi:10.3390/ijms21061960. ISSN 1422-0067. PMC 7139603. PMID 32183020.
- ^ Williams, Ashley B.; Schumacher, Björn (2016). “p53 in the DNA-Damage-Repair Process”. Cold Spring Harbor Perspectives in Medicine 6 (5): a026070. doi:10.1101/cshperspect.a026070. ISSN 2157-1422. PMC 4852800. PMID 27048304.
- ^ Engeland, Kurt (2022). “Cell cycle regulation: p53-p21-RB signaling” (英語). Cell Death & Differentiation 29 (5): 946–960. doi:10.1038/s41418-022-00988-z. ISSN 1476-5403. PMC 9090780. PMID 35361964.
- ^ Ruvolo, P. P.; Deng, X.; May, W. S. (2001). “Phosphorylation of Bcl2 and regulation of apoptosis” (英語). Leukemia 15 (4): 515–522. doi:10.1038/sj.leu.2402090. ISSN 1476-5551. PMID 11368354.
- ^ Jabbour, A. M.; Heraud, J. E.; Daunt, C. P.; Kaufmann, T.; Sandow, J.; O'Reilly, L. A.; Callus, B. A.; Lopez, A. et al. (2009). “Puma indirectly activates Bax to cause apoptosis in the absence of Bid or Bim” (英語). Cell Death & Differentiation 16 (4): 555–563. doi:10.1038/cdd.2008.179. ISSN 1476-5403. PMID 19079139.
- ^ Jiang H, Schiffer E, Song Z, Wang J, Zürbig P, Thedieck K, Moes S, Bantel H, Saal N, Jantos J, Brecht M, Jenö P, Hall MN, Hager K, Manns MP, Hecker H, Ganser A, Döhner K, Bartke A, Meissner C, Mischak H, Ju Z, Rudolph KL (August 2008). “Proteins induced by telomere dysfunction and DNA damage represent biomarkers of human aging and disease”. Proceedings of the National Academy of Sciences of the United States of America 105 (32): 11299–304. Bibcode: 2008PNAS..10511299J. doi:10.1073/pnas.0801457105. PMC 2516278. PMID 18695223.
- ^ Cawthon RM, Smith KR, O'Brien E, Sivatchenko A, Kerber RA (February 2003). “Association between telomere length in blood and mortality in people aged 60 years or older”. Lancet 361 (9355): 393–5. doi:10.1016/S0140-6736(03)12384-7. PMID 12573379.
- ^ Jafri MA, Ansari SA, Alqahtani MH, Shay JW (June 2016). “Roles of telomeres and telomerase in cancer, and advances in telomerase-targeted therapies”. Genome Medicine 8 (1): 69. doi:10.1186/s13073-016-0324-x. PMC 4915101. PMID 27323951.
- ^ Chan KY, Yan CC, Roan HY, Hsu SC, Tseng TL, Hsiao CD, Hsu CP, Chen CH (April 2022). “Skin cells undergo asynthetic fission to expand body surfaces in zebrafish”. Nature 605 (7908): 119–125. Bibcode: 2022Natur.605..119C. doi:10.1038/s41586-022-04641-0. PMID 35477758.
- ^ Biographie, Deutsche. “Mohl, Hugo von - Deutsche Biographie” (ドイツ語). www.deutsche-biographie.de. 2019年4月15日閲覧。
- ^ Masters, Barry R (2008-12-15). “History of the Optical Microscope in Cell Biology and Medicine”. Encyclopedia of Life Sciences. John Wiley & Sons, Ltd.. doi:10.1002/9780470015902.a0003082. ISBN 978-0470016176
- ^ ZEISS Microscopy (2013-06-01), Historic time lapse movie by Dr. Kurt Michel, Carl Zeiss Jena (ca. 1943), オリジナルの2021-11-07時点におけるアーカイブ。 2019年4月15日閲覧。
推薦文献
[編集]- Morgan HI. (2007). "The Cell Cycle: Principles of Control" London: New Science Press.
- J.M.Turner Fetus into Man (1978, 1989). Harvard University Press. ISBN 0-674-30692-9
- Cell division: binary fission and mitosis
- McDougal, W. Scott, et al. Campbell-Walsh Urology Eleventh Edition Review. Elsevier, 2016.
- The Mitosis and Cell Cycle Control Section from the Landmark Papers in Cell Biology (Gall JG, McIntosh JR, eds.) contains commentaries on and links to seminal research papers on mitosis and cell division. Published online in the Image & Video Library of The American Society for Cell Biology
- The Image & Video Library Archived 2011-06-10 at the Wayback Machine. of The American Society for Cell Biology contains many videos showing the cell division.
- The Cell Division of the Cell Image Library
- Images : Calanthe discolor Lindl. - Flavon's Secret Flower Garden
- Tyson's model of cell division and a Description on BioModels Database
- WormWeb.org: Interactive Visualization of the C. elegans Cell Lineage - Visualize the entire set of cell divisions of the nematode C. elegans
