GSK-3
| glycogen synthase kinase 3 alpha | |
|---|---|
| 識別子 | |
| 略号 | GSK3A |
| Entrez | 2931 |
| HUGO | 4616 |
| OMIM | 606784 |
| RefSeq | NM_019884 |
| UniProt | P49840 |
| 他のデータ | |
| EC番号 (KEGG) | 2.7.11.26 |
| 遺伝子座 | Chr. 19 q13.2 |
| glycogen synthase kinase 3 beta | |
|---|---|
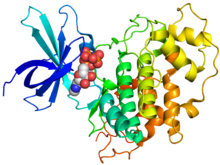 AMP-PNPを結合したヒトGSK-3βの結晶構造
[1] | |
| 識別子 | |
| 略号 | GSK3B |
| Entrez | 2932 |
| HUGO | 4617 |
| OMIM | 605004 |
| PDB | 1Q3W (RCSB PDB PDBe PDBj) More structures |
| RefSeq | NM_002093 |
| UniProt | P49841 |
| 他のデータ | |
| EC番号 (KEGG) | 2.7.11.26 |
| 遺伝子座 | Chr. 3 q13.33 |
GSK-3 (glycogen synthase kinase 3) は、セリンとスレオニンのアミノ酸残基へのリン酸分子の付加を媒介するセリン・スレオニンプロテインキナーゼである。グリコーゲンシンターゼキナーゼ-3、グリコーゲン合成酵素キナーゼ-3などとも呼ばれる。なお直訳すると「グリコーゲンシンターゼ(グリコーゲン合成酵素)をリン酸化する酵素(キナーゼ)」という意味である。GSK-3は、1980年にグリコーゲンシンターゼを調節するキナーゼとして発見され、それが名前の由来となっている[2]。それ以降、GSK-3は様々な経路の40種類以上のタンパク質に対してキナーゼとして機能することが示されている[3]。哺乳類では、GSK-3は2つの遺伝子GSK3A (GSK-3α)、GSK3B (GSK-3β) にコードされていることが知られている。近年、GSK-3は2型糖尿病、アルツハイマー病、炎症、がん、双極性障害など多数の疾患との関連が示唆され、多くの研究の対象となっている。
機構[編集]
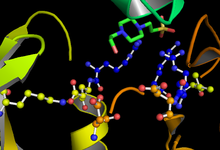
GSK-3は、標的基質のセリン残基またはスレオニン残基をリン酸化することで機能する。GSK-3は通常、基質を最初にリン酸化する「プライミングキナーゼ」を必要とする。GSK-3の標的リン酸化部位から4アミノ酸C末端側のセリン/スレオニン残基に付加された「プライミング」リン酸基が、活性部位に近接する正に帯電したポケットへ結合する。181、200、97、85番残基によって形成される活性部位は、ATPの末端のリン酸基に結合し、基質の標的部位へリン酸基を転移する[4]。
機能[編集]
GSK-3によるタンパク質のリン酸化は通常、下流の標的因子の活性を阻害する[5][6][7]。GSK-3は、細胞増殖、細胞遊走、グルコースの調節、アポトーシスなど、細胞内での中心的なシグナル伝達経路の多くに関与している。
GSK-3は元々、グリコーゲンシンターゼの調節に関与する因子として発見された[2]。グリコーゲンシンターゼはカゼインキナーゼ2 (CK2) によって最初のリン酸化 (プライミング) が行われた後、GSK-3によってC末端の3つのセリン残基のクラスターがリン酸化されて活性が低下する[8]。グリコーゲンシンターゼの調節に加え、インスリン受容体基質 (IRS1)、糖新生に関わる酵素ホスホエノールピルビン酸カルボキシキナーゼとグルコース-6-ホスファターゼのリン酸化など、グルコース濃度の恒常性を維持する他の仕組みへの関与も示唆されている[9] [10]。しかし、これらの経路はGSK-3のアップレギュレーションがなくても阻害され、GSK-3の関与については議論が存在する[8]。
また、GSK-3は免疫や遊走の過程を調節することが示されている。GSK-3は、炎症性サイトカインやインターロイキンの産生といった、自然免疫の応答経路の多くに関与する[11][12]。様々なキナーゼによるGSK-3βの不活性化は、サイトカインの産生や、CD4陽性T細胞のうちナイーブT細胞と記憶T細胞の増殖といった、獲得免疫の応答機構にも影響を与える[12]。細胞遊走過程は炎症応答に不可欠の要素であるが、それにおけるGSK-3の役割については矛盾する結果が得られている。成長円錐での局所的な阻害は運動性を促進することが示されている一方、細胞全体でのGSK-3の阻害は細胞の伸展や遊走を阻害することが示されている[11]。
GSK-3は細胞増殖やアポトーシス経路とも密接に関係している。GSK-3はβ-カテニンをリン酸化して分解標的とすることが示されており[13]、細胞分割と細胞増殖のシグナルを伝達するβ-カテニン/Wnt経路の一部を構成する。また、GSK-3はアポトーシスを調節する転写因子をリン酸化し、多くのアポトーシスシグナル伝達経路に関与する[3]。アポトーシスの調節におけるGSK-3の役割に関しては矛盾する結果が得られている。GSK-3はリン酸化によって、p53のようなアポトーシス促進因子を活性化し[14]、生存促進因子を不活性化することでアポトーシスを促進することが報告されている[15]。いくつかの研究では、GSK-3βのノックアウトマウスはアポトーシスに対して過度の感受性となって胚段階で死亡することが示されている一方で、他の研究ではGSK-3の過剰発現がアポトーシスを誘導することが示されている[16]。全体としては、GSK-3はアポトーシスを促進することも阻害することもあり、この調節は特定の分子的・細胞的状況に依存して変化するようである[17]。
調節[編集]
GSK-3は多数の細胞機能に関与する重要な因子であり、その活性は緊密な調節を受けている。
GSK-3のリン酸化の速度と効率は多数の因子によって調節されている。GSK-3の特定の残基のリン酸化によって、基質へ結合する能力が向上したり低下したりする。GSK-3βの216番目のチロシン残基 (Tyr216) またはGSK-3αのTyr279のリン酸化はGSK-3の酵素活性を向上させ、GSK-3βのSer9またはGSK-3αのSer21のリン酸化は活性部位の利用可能性を大きく低下させる[11]。さらに、GSK-3は通常、基質を最初にリン酸化する「プライミングキナーゼ」を必要とするという点で特殊である。リン酸化の標的部位から4アミノ酸C末端側にリン酸化セリンまたはスレオニン残基が位置することで、アルギニンとリジン残基によって形成される正に帯電したポケットへ基質が結合できるようになる[8][18]。
経路に応じて、GSK-3はさらに細胞内局在化やタンパク質複合体の形成といった調節を受ける。皮質ニューロンでは、GSK-3は細胞質よりも核やミトコンドリアにおいて遥かに高い活性を持つ[19]。また、GSK-3によるβ-カテニンのリン酸化は足場タンパク質であるアキシン (Axin) によって媒介され、双方がアキシンに結合することでβ-カテニンはGSK-3の活性部位にアクセスできるようになる[11]。
疾患との関連[編集]
大多数のシグナル伝達に関与しているため、GSK-3は注目を集める多くの疾患と関連している。現在、アルツハイマー病、2型糖尿病、一部のがん、双極性障害に対してGSK-3阻害剤の治療効果が試験されている[20]。
現在では、双極性障害の治療に用いられているリチウムは、GSK-3を選択的に阻害することで気分安定薬として機能していることが示されている。GSK-3の阻害が気分を安定させる機構は不明であるが、GSK-3の炎症促進能力を阻害することが治療効果をもたらしている可能性が考えられている[11]。また、GSK-3の阻害は、概日時計に大きな役割を果たす転写抑制因子Rev-ErbAαを不安定化する[21]。概日時計の要素は、双極性障害の傾向と関連している可能性がある[22]。
GSK-3の活性は、アルツハイマー病の病理学的特徴の双方、すなわちアミロイドβの蓄積と神経原線維変化 (neurofibrillary tangle) の形成のいずれにも関連している。GSK-3は直接的にアミロイドβの産生を促進し、tangleをもたらすタウタンパク質の過剰なリン酸化の過程にも関わっていると考えられている[3][11]。GSK-3のこのようなアルツハイマー病を促進する役割のため、GSK-3阻害剤はアルツハイマー病患者に治療効果がある可能性があり、現在初期段階の試験が行われている[23]。
同様に、GSK-3の標的阻害は特定のがんに対しても治療効果がある可能性がある。いくつかの場合でGSK-3はアポトーシスを促進することが示されている一方、一部のがんでは腫瘍形成に重要な因子であることが報告されている[24]。この主張を支持するものとして、GSK-3阻害剤は神経膠腫と膵臓がんの細胞にアポトーシスを誘導することが示されている[16][25]。
また、GSK-3阻害剤は2型糖尿病の治療においても有望であることが示されている[8]。糖尿病条件下におけるGSK-3の活性は組織によって完全に異なるが、GSK-3の競合阻害剤によって糖尿病マウスの耐糖能が向上することが研究で示されている[11]。GSK-3阻害剤は急性虚血性脳卒中 (acute ischemic stroke) 後の出血性変化 (hemorrhagic transformation) に対しても治療効果がある可能性がある[26]。
GSK-3の阻害は、T細胞で転写因子T-bet (Tbx21) の転写を増加させ、コリプレッサーであるPD-1の転写を阻害する[27]。GSK-3阻害剤は、免疫療法における抗PD-1抗体と同様に、in vivoでCD8陽性 OT-I CTLの機能と、マウスガンマヘルペスウイルス68株とリンパ球性脈絡髄膜炎ウィルスクローン13株によるウイルス感染のクリアランスを増加させた[27]。
阻害剤[編集]
GSK-3の阻害剤には次のようなものがある[28]。
金属カチオン[編集]
ATP競合型[編集]
海洋生物由来[編集]
- 6-BIO (IC50=1.5 μM)
- ジブロモカンタレリン (dibromocantharelline) (IC50=3 μM)
- ヒメニアルデシン (hymenialdesine) (IC50=10 nM)
- インジルビン (IC50=5-50 nM)
- メリジアニン (meridianin)
アミノピリミジン[編集]
IC50=0.6-7 nM:
- CT98014
- CT98023
- CT99021
- TWS119
アリールインドリルマレイミド[編集]
- SB-216763 (IC50=34 nM)
- SB-41528 (IC50=77 nM)
チアゾール[編集]
- AR-A014418 (IC50=104 nM)
- AZD-1080
パウロン (paullone)[編集]
IC50=4-80 nM:
- Alsterpaullone
- Cazpaullone
- Kenpaullone
アロイシン (aloisine)[編集]
IC50=0.5-1.5 μM:
非ATP競合型[編集]
海洋生物由来[編集]
- マンザミンA (manzamine A) (IC50=1.5 μM)
- パリヌリン (palinurine) (IC50=4.5 μM)
- トリカンチン (tricantine) (IC50=7.5 μM)
チアジアゾリジンジオン (thiadiazolidindione)[編集]
- TDZD-8 (IC50=2 μM)
- NP00111 (IC50=2 μM)
- NP031115 (IC50=4 μM)
- チデグルシブ
ハロメチルケトン[編集]
- HMK-32 (IC50=1.5 μM)
ペプチド[編集]
- L803-mts (IC50=40 μM)
その他: ケタミン
出典[編集]
- ^ PDB: 1J1B; “Structural insight into nucleotide recognition in tau-protein kinase I/glycogen synthase kinase 3 beta”. Acta Crystallographica Section D 60 (Pt 3): 439–46. (March 2004). doi:10.1107/S090744490302938X. PMID 14993667.
- ^ a b “Glycogen synthase kinase-3 from rabbit skeletal muscle. Separation from cyclic-AMP-dependent protein kinase and phosphorylase kinase”. European Journal of Biochemistry 107 (2): 519–27. (June 1980). doi:10.1111/j.1432-1033.1980.tb06059.x. PMID 6249596.
- ^ a b c “The glamour and gloom of glycogen synthase kinase-3”. Trends in Biochemical Sciences 29 (2): 95–102. (February 2004). doi:10.1016/j.tibs.2003.12.004. PMID 15102436.
- ^ “Crystal structure of glycogen synthase kinase 3 beta: structural basis for phosphate-primed substrate specificity and autoinhibition”. Cell 105 (6): 721–32. (June 2001). doi:10.1016/S0092-8674(01)00374-9. PMID 11440715.
- ^ “Regulation and functions of the glycogen synthase kinase-3 subfamily”. Seminars in Cancer Biology 5 (4): 269–75. (August 1994). PMID 7803763.
- ^ “Judging a protein by more than its name: GSK-3”. Science's STKE 2001 (100): re12. (September 2001). doi:10.1126/stke.2001.100.re12. PMID 11579232.
- ^ “Glycogen synthase kinase-3: properties, functions, and regulation”. Chemical Reviews 101 (8): 2527–40. (August 2001). doi:10.1021/cr000110o. PMID 11749387.
- ^ a b c d “Glycogen synthase kinase 3: more than a namesake”. British Journal of Pharmacology 156 (6): 885–98. (March 2009). doi:10.1111/j.1476-5381.2008.00085.x. PMC 2697722. PMID 19366350.
- ^ “Serine 332 phosphorylation of insulin receptor substrate-1 by glycogen synthase kinase-3 attenuates insulin signaling”. The Journal of Biological Chemistry 280 (6): 4422–8. (February 2005). doi:10.1074/jbc.M410610200. PMID 15574412.
- ^ “Inhibition of GSK-3 selectively reduces glucose-6-phosphatase and phosphatase and phosphoenolypyruvate carboxykinase gene expression”. Diabetes 50 (5): 937–46. (May 2001). doi:10.2337/diabetes.50.5.937. PMID 11334436.
- ^ a b c d e f g “Glycogen synthase kinase-3 (GSK3): inflammation, diseases, and therapeutics”. Neurochemical Research 32 (4-5): 577–95. (Apr–May 2007). doi:10.1007/s11064-006-9128-5. PMC 1970866. PMID 16944320.
- ^ a b “Glycogen synthase kinase 3: a point of convergence for the host inflammatory response”. Cytokine 53 (2): 130–40. (February 2011). doi:10.1016/j.cyto.2010.10.009. PMC 3021641. PMID 21095632.
- ^ “Emerging roles of glycogen synthase kinase 3 in the treatment of brain tumors”. Frontiers in Molecular Neuroscience 4: 47. (2011). doi:10.3389/fnmol.2011.00047. PMC 3223722. PMID 22275880.
- ^ “Direct, activating interaction between glycogen synthase kinase-3beta and p53 after DNA damage”. Proceedings of the National Academy of Sciences of the United States of America 99 (12): 7951–5. (June 2002). doi:10.1073/pnas.122062299. PMC 123001. PMID 12048243.
- ^ “CREB DNA binding activity is inhibited by glycogen synthase kinase-3 beta and facilitated by lithium”. Journal of Neurochemistry 78 (6): 1219–32. (September 2001). doi:10.1046/j.1471-4159.2001.00495.x. PMC 1947002. PMID 11579131.
- ^ a b “Glycogen synthase kinase-3 inhibition induces glioma cell death through c-MYC, nuclear factor-kappaB, and glucose regulation”. Cancer Research 68 (16): 6643–51. (August 2008). doi:10.1158/0008-5472.CAN-08-0850. PMC 2585745. PMID 18701488.
- ^ “GSK-3β: A Bifunctional Role in Cell Death Pathways”. International Journal of Cell Biology 2012: 930710. (May 2012). doi:10.1155/2012/930710. PMC 3364548. PMID 22675363.
- ^ “GSK-3: tricks of the trade for a multi-tasking kinase”. Journal of Cell Science 116 (Pt 7): 1175–86. (April 2003). doi:10.1242/jcs.00384. PMC 3006448. PMID 12615961.
- ^ “Glycogen synthase kinase-3 beta is highly activated in nuclei and mitochondria”. NeuroReport 14 (18): 2415–9. (December 2003). doi:10.1097/00001756-200312190-00025. PMID 14663202.
- ^ “Glycogen synthase kinase-3 and its inhibitors: Potential target for various therapeutic conditions”. European Journal of Medicinal Chemistry 144: 843–858. (January 2018). doi:10.1016/j.ejmech.2017.11.103. PMID 29306837.
- ^ “Nuclear receptor Rev-erbalpha is a critical lithium-sensitive component of the circadian clock”. Science 311 (5763): 1002–5. (February 2006). doi:10.1126/science.1121613. PMID 16484495.
- ^ “Polymorphism of circadian clock genes and temperamental dimensions of the TEMPS-A in bipolar disorder”. Journal of Affective Disorders 159: 80–4. (April 2014). doi:10.1016/j.jad.2014.02.024. PMID 24679394.
- ^ “GSK3 inhibitors show benefits in an Alzheimer's disease (AD) model of neurodegeneration but adverse effects in control animals”. Neurobiology of Disease 33 (2): 193–206. (February 2009). doi:10.1016/j.nbd.2008.10.007. PMC 4313761. PMID 19038340.
- ^ “Glycogen synthase kinase 3 in MLL leukaemia maintenance and targeted therapy”. Nature 455 (7217): 1205–9. (October 2008). doi:10.1038/nature07284. PMC 4084721. PMID 18806775.
- ^ “Inhibition of glycogen synthase kinase-3 activity triggers an apoptotic response in pancreatic cancer cells through JNK-dependent mechanisms”. Carcinogenesis 33 (3): 529–37. (March 2012). doi:10.1093/carcin/bgr309. PMID 22201186.
- ^ “GSK-3β inhibitor TWS119 attenuates rtPA-induced hemorrhagic transformation and activates the Wnt/β-catenin signaling pathway after acute ischemic stroke in rats”. Molecular Neurobiology 53 (10): 7028–7036. (December 2016). doi:10.1007/s12035-015-9607-2. PMC 4909586. PMID 26671619.
- ^ a b “Glycogen Synthase Kinase 3 Inactivation Drives T-bet-Mediated Downregulation of Co-receptor PD-1 to Enhance CD8(+) Cytolytic T Cell Responses”. Immunity 44 (2): 274–86. (February 2016). doi:10.1016/j.immuni.2016.01.018. PMC 4760122. PMID 26885856.
- ^ “GSK-3 Inhibitors: Preclinical and Clinical Focus on CNS”. Frontiers in Molecular Neuroscience 4: 32. (2011). doi:10.3389/fnmol.2011.00032. PMC 3204427. PMID 22065134.
関連項目[編集]
外部リンク[編集]
- Glycogen Synthase Kinase 3 - MeSH・アメリカ国立医学図書館・生命科学用語シソーラス(英語)
