主要組織適合遺伝子複合体
主要組織適合遺伝子複合体(しゅようそしきてきごういでんしふくごうたい、major histocompatibility complex; MHC)は、免疫反応に必要な多くのタンパクの遺伝子情報を含む[1][2]、細胞膜表面にある糖タンパク質である。研究の当初、MHCは遺伝子として同定されてきたが、のちに糖タンパク質として意味が置き換わって行った[3]。
(糖タンパクか遺伝子かの)区別のために糖タンパク質であることを明記・強調したい場合には、日本では「MHC抗原」、「MHC分子」、「MHCタンパク質[4][5]」などと表現するのが一般的である。
いっぽう、遺伝子領域においてMHCをコードする遺伝子のこととして明記したい場合には、「MHC領域」[6]、「MHC遺伝子」[7]などと表現する場合もある。
概要
MHC分子は、ほとんどの脊椎動物が細胞に持ち、ヒトのMHCはヒト白血球型抗原 (HLA)、マウスのMHCはH-2 (histocompatibility-2)、ニワトリではB遺伝子座 (B locus) と呼ばれる。
MHCは免疫に関わるが、MHC分子そのものの存在箇所は免疫細胞だけではなく、ほぼすべての有核細胞にもMHC分子は存在する。また、MHC分子は糖タンパク質である。
正確には、MHC分子には主に2種類あり、クラスIとクラスIIという2種類が主要で、このうちMHCクラスIが、核のあるすべての細胞に存在・発現している。(なお、じつはMHC遺伝子には、補体系をコードする遺伝子領域としてMHCクラスIIIがある[8]。) MHCクラスIIは、B細胞・樹状細胞・マクロファージに存在・発現している[9]。
このMHC分子は抗原提示を行うことで細菌やウイルスなどの感染病原体の排除や、がん細胞の拒絶、臓器移植の際の拒絶反応などに関与し、免疫にとって非常に重要な働きをする。その他、ペプチドの輸送に関与するTAP (transporter associated with antigen processing) やプロテアソームに関与するLMP (low-molecular-weight protein) といった、免疫に関するさまざまなタンパク群もこのMHCにコードされている。
なお、あまり正確な言い方ではないかしれないが、T細胞側の、MHCと結合する受容体のことを「T細胞受容体」(TCR)という。つまり、T細胞側の、MHCにとってのリガンド(ある受容体にとっての結合相手側の別の受容体のこと)のことを「T細胞受容体」という。ややこしいことに、T細胞には、MHCと結合する受容体のほかにも多くの受容体があり、それぞれリガンドも異なるのだが、しかし、「T細胞受容体」という呼び方が慣習になっている。
MHC分子
MHC分子は細胞表面に存在する細胞膜貫通型の糖タンパク分子であり、細胞内のさまざまなタンパク質の断片(ペプチド)を細胞表面に提示する働きをもつ。
ペプチドについて、(病原体などの)細胞に感染したウイルスや癌抗原、あるいは樹状細胞などの抗原提示細胞に貪食処理された結果に生成するペプチドのことを「抗原ペプチド」[10]または「ペプチド抗原」[11]と一般にいう。(なお、「抗菌ペプチド」とは異なる。抗菌ペプチドとはディフェンシンなどの事。)
抗原ペプチドがMHC分子に結合して細胞表面に提示されると、それがリンパ球のうちT細胞に抗原として認識され、引き続き免疫反応が惹起されてウイルスや癌などを攻撃排除する方向に働く。
いっぽう、抗原の無い状態でのMHC自身の生成時にもMHCに自己由来のペプチド(いわゆる「自己ペプチド」)が結合して安定化していると考えられており、抗原の侵入・発生時には抗原由来のペプチドに置き換わる仕組みである[12]と、考えられている。
また、用語として、MHC分子に上述のペプチドがついた状態であることを明記したい場合、そのような(MHC分子に上述のペプチドがついた状態の)MHC分子のことを「MHC分子-ペプチド複合体[13]」または「ペプチド-MHC複合体[14]」などと呼ぶことがある。
生物個体それぞれは、似たような構造のMHC分子の遺伝子情報を何種類も持ち、こうして数種類のMHCを同時に発現させている。さらに数種類のMHC全てを、父親由来のMHC1組と母親由来MHC1組の計2組ずつもっている。またMHCは個体によって非常に多様性に富み(多型性 polymorphic )、このため2組のMHCはほとんどの場合異なった種類の組み合わせとなる(ヘテロ接合体)。このようにしてそれぞれの個体は、何種類ものMHC分子の遺伝子情報をもっており(多遺伝子性 polygenic )、このためMHCはさまざまな抗原に対応できる。また多型性のため、MHC分子はT細胞が自己と他者の区別をする目印にもなる。つまり、T細胞は自己のMHC分子を発現する細胞から抗原提示を受けるが、自己と異なるMHC分子を異物と見なし、攻撃排除しようとする。しかし、個体によって持つMHCが異なるということは、MHCによって結合できる抗原が異なるため、MHCの違いにより病気のなりやすさが異なることがある。例えばMHCの違いによってAIDSの進行が違ってくる[15]。逆にいうとこの多様性によって、病原体に対して種の絶滅を防ぐことができるようになっている。
MHC分子には大きく分けてクラスIとクラスIIの2つの種類がある。MHCクラスI分子は細胞内の内因性抗原を結合し、MHCクラスII分子はエンドサイトーシスで細胞内に取り込まれて処理された外来性抗原を結合して提示する[16]。つまり、ウイルスのように感染した細胞内で増殖する病原体に対して、あるいはがん細胞内で産生されるがん抗原に対しては、MHCクラスIを介した抗原提示により免疫反応をおこし、いっぽう、細菌など細胞外で増殖する病原体や毒素に対して、あるいは結核菌のようにマクロファージ等の抗原提示細胞に感染する病原体に対しては、抗原提示細胞のMHCクラスIIを介した抗原提示により免疫反応をおこす。ただしこの2つ経路は絶対的なものではなく、外来抗原もMHCクラスIによる抗原提示経路にも入りうる(クロスプライミング cross-priming またはクロスプレゼンテーション cross-presentation )。
MHCクラスIに結合するペプチドの長さと、MHCクラスIIに結合するペプチドの長さは違っていることが分かっており、MHCクラスIIに結合するペプチドのほうが長い。MHCクラスIに結合するペプチドのアミノ酸の長さは、およそ8〜10塩基である。いっぽう、MHCクラスIIに結合するペプチドのアミノ酸の長さはおよそ10〜30塩基である[17]。
MHCクラスI分子
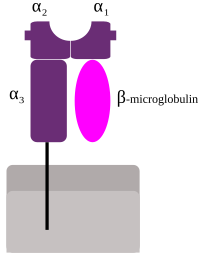
MHCクラスI分子はほとんどすべての有核細胞と血小板の細胞表面に存在する糖タンパクであり、内因性抗原を抗原提示する働きをもつ。MHCクラスI分子はさらに古典的クラスI分子(クラスIa)と非古典的クラスI分子(クラスIb)に分けられる。古典的クラスI分子には、ヒトではHLA-A、HLA-B、HLA-Cの3種類が、マウスではH-2K、H-2D、H-2Lの3種類がある。非古典的クラスI分子にはヒトではHLA-E、HLA-F、HLA-Gが、マウスではH-2Qa、H-2Tlaがある[18]。
構造
MHCクラスI分子は、糖鎖が付加した分子量45 kDaの重鎖(α鎖)と、分子量12 kDaのβ2-ミクログロブリン軽鎖の2つが非共有結合した二量体であり、これにペプチド抗原が結合して三量体として細胞表面に発現する。非古典的クラスI分子の中には、発現にβ2-ミクログロブリンを必要としないものもある。クラスI重鎖はα1〜α3の3つの細胞外領域と、細胞膜貫通領域、細胞内領域からなる。α1領域とα2領域の間に大きな溝状の構造(「ペプチド収容溝」[19])があり、MHCはこのペプチド収容溝に抗原を結合しT細胞に提示する。
局在
MHCクラスI分子はほとんど全ての有核細胞および血小板の細胞表面に発現するが、発現の程度には差異がある[20]。甲状腺、副甲状腺、下垂体の内分泌細胞や膵臓ランゲルハンス島、胃粘膜、心筋、骨格筋、肝細胞では発現が弱く、中枢神経,末梢神経には発現がない[20][21]。また、精子細胞は精巣にある間はMHCクラスI分子を発現しているが、精巣上体(副睾丸)に移動すると発現がなくなる[20]。
悪性腫瘍においても、さまざまな悪性腫瘍で16〜50%程度にMHCクラスI分子の発現の低下・欠失がみられる[22]。さらに、原発巣よりも転移巣において発現低下・欠失の頻度が高く、MHCクラスI発現は腫瘍の予後,免疫治療の効果[23]等と関連することから,MHCクラスI分子の発現低下・欠失により腫瘍細胞は免疫監視機構から逃避していると考えられている[24]。
発現経路
ウイルスのように感染した細胞内で増殖する病原体や、あるいはがん細胞内で産生されるタンパクなど、細胞質内のタンパクはユビキチン化された後、プロテアソームによって5〜15アミノ酸程度のペプチドにまで分解される。分解されたペプチドは、小胞体 (ER) 膜上にあるTAP (transporter associated with antigen processing) というATP駆動型トランスポーターによって小胞体 (ER) 内部に輸送される。なおTAPの構造は、膜貫通型であり、TAP1とTAP2からなるヘテロ二量体である。なお一般にABC輸送体と呼ばれるATP駆動型トランスポーターは膜貫通型である。TAPを、ABC輸送体の一種として分類することもある。
MHCクラスIα鎖とβ2ミクログロブリンは小胞体(ER)内で合成され、小胞体(ER)内でMHCクラスIα鎖、β2ミクログロブリン、そしてペプチドの3つが結合してMHC-ペプチド複合体を作る[25]。その後、MHC-ペプチド複合体は、より小さな小胞体の内部に置かれて、小胞輸送によって細胞膜を目指して運ばれる途中でゴルジ体を通り、糖鎖修飾を受けた後、細胞膜上に到達して発現する。
機能
T細胞には、主にキラーT細胞やヘルパーT細胞という2種類があるが、MHCクラスI分子の抗原と反応するのはキラーT細胞のほうである。
詳細にいうと、CD8陽性T細胞(キラーT細胞)は、細胞膜上に発現したMHCクラスI分子と抗原を認識し、活性化する。そしてその抗原を発現している細胞、例えばウイルス感染細胞やがん細胞を傷害するようになる(細胞傷害性T細胞)。ただしCD8陽性T細胞は、自己と同じMHCクラスI分子に結合した抗原のみ認識し、自己と異なるMHC分子は異物と見なし攻撃する。
MHCクラスI分子は、NK細胞の細胞傷害活性を抑制する働きももつ。NK細胞は細胞表面にKIR(キラー細胞免疫グロブリン様受容体 killer cell immunoglobulin-like receptor )とよばれる受容体を持っており、このKIRが古典的MHCクラスI分子、あるいはヒト非古典的MHCクラスI分子のうちHLA-Gを認識すると、NK細胞はその細胞を傷害しなくなる。またヒト非古典的MHCクラスI分子であるHLA-Eは、NK細胞がもつ受容体のひとつであるNKG2A (natural killer group 2A) を介してNK細胞の傷害活性を抑制する。逆にNK細胞はMHCクラスI分子を持たない細胞を攻撃する(Missing Self説[26])。例えばヒトでは胎児由来の胎盤細胞はHLAクラスI分子の発現がないが、HLA-Gを発現して母親由来のNK細胞から胎児を守っている[27]。
つまり、MHCクラスI分子は自己と他者を区別する標識であり、自己のCD8陽性T細胞に抗原を提示して病原体や癌などを排除しつつ、NK細胞の攻撃から身を守る働きをしている。
MHCクラスII分子

T細胞には、主にキラーT細胞やヘルパーT細胞という2種類があるが、MHCクラスII分子の抗原と反応するのはヘルパーT細胞のほうである。
MHCクラスII分子は、マクロファージや樹状細胞、活性化T細胞、B細胞などの抗原提示細胞を含め、限られた細胞にのみ発現している。クラスII分子はα鎖とβ鎖の2つの重合体であり、それぞれ2つの細胞外領域および膜貫通領域、細胞内領域からなる。MHCクラスII分子はヒトではHLA-DR、HLA-DQ、HLA-DPの3種類があるが、DRのβ鎖は2種類あることが多く、これがDRα鎖と結合するためDR分子は2種類あることになる。つまり、ヒトでは4種類のMHCクラスII分子をもつことが多い。マウスMHCクラスII分子にはH-2A、H-2Eの2種類がある。
エンドサイトーシスにより抗原提示細胞に取り込まれた外来抗原は、抗原提示細胞内のエンドソームでタンパク分解酵素により消化され、ペプチド断片に分解される。MHCクラスII分子に結合するペプチドはクラスI分子に結合するペプチドよりも長く、15〜24アミノ酸程度である。ペプチド断片はその後CPL (compartment for peptide loading) と呼ばれる小胞に移動する。小胞体 (ER) で合成されたMHCクラスIIα鎖とβ鎖はゴルジ体を通ってCPL内に移動し、このCPL内でペプチドとMHCクラスII複合体が生成される。そして細胞表面に発現し、CD4陽性T細胞(ヘルパーT細胞)に抗原を提示して活性化させる。活性化したCD4陽性細胞は細胞傷害性T細胞やB細胞、その他の免疫細胞を活性化して異物を攻撃する。
遺伝子
ヒトMHC (HLA) 遺伝子は6番染色体短腕上に、マウスMHC (H-2) は17番染色体上に存在し、ヒトでは224もの遺伝子(128の機能的遺伝子と96の偽遺伝子)を含む360万塩基対にも及ぶ巨大な複合的遺伝子領域である[28]。1999年にヒトMHC遺伝子の全塩基配列と遺伝子地図が解読された[28]。
ヒトMHC遺伝子の分類は、3つの領域に分けられ、クラスI領域、クラスII領域、クラスIII領域に分けられている。染色体のテロメア側(末端側)からセントロメア側(中心側)に向かって、クラスI領域、クラスIII領域、クラスII領域が存在する。クラスIII領域のうち、腫瘍壊死因子 (TNF) スーパーファミリーなど炎症に関わる遺伝子群の領域はクラスIV領域と分類されることもある[29]。マウスMHCは転座がおこっているためクラスI領域が2つに分断されており、テロメア側からクラスI領域、クラスIII領域、クラスII領域、小さなクラスI領域となっている。
MHCクラスI領域には3種類のクラスI分子α鎖、つまりヒトではHLA-A、B、C、マウスではH-2K、D、Lの3種類のクラスI分子α鎖がコードされている。β2-ミクログロブリン遺伝子はMHCにはなく、ヒトでは15番染色体 (15q21-q22.2) に[30]、マウスでは2番染色体 (2 F1-F3; 2 69.0 cM) に[31]存在する。MHCクラスII領域にはクラスII分子α鎖とβ鎖、つまりヒトではHLA-DQ、DR、DPのα鎖とβ鎖が、マウスではH-2AとEのα鎖とβ鎖がコードされている。その他2つのTAP (TAP1、TAP2) 遺伝子、LMP (low-molecular-weight protein) 遺伝子、タパシン (tapasin) 遺伝子もクラスII領域にある[2]。ヒトMHCクラスIII領域にはC4、C2、B因子などの補体や、TNFなどのサイトカインの遺伝子が存在する。
MHC遺伝子には、免疫と関係のない遺伝子も存在する。たとえば、クラスIB領域にあるHFe 遺伝子は腸管の細胞の鉄代謝に関与しており、クラスII領域の21-水酸化酵素はステロイド合成に関与している。
MHC遺伝子の進化と多様性
MHC遺伝子はほとんどの脊椎動物にみられる遺伝子領域であるが、遺伝子の構成や配置は種によってさまざまである。例えばニワトリは最も小さいMHC遺伝子をもつ種のひとつであり、ヒトMHC遺伝子の約20分の1、全長92,000塩基で19の遺伝子しか持たない[32]が、一方ほとんどのほ乳類はヒトとよく似た構成のMHCをもつ。ニワトリMHC遺伝子の19全ての遺伝子に相当する遺伝子がヒトにも存在し、これは必要最低限のMHCであるといえるかもしれない[32]。 MHC遺伝子の多様性は遺伝子重複によるところが大きい。ヒトMHCには多くの偽遺伝子がちりばめられている。
研究当初の歴史とノーベル賞など
1930年代にPeter Alfred Gorerが、移植片拒絶の研究を本格的に開始した。
そして1940年代にアメリカのジョージ・スネルにより、同系を20代以上かけあわせたマウスをつかった移植の研究によって、1940年代には原因物質としてマウスのH-2抗原が発見された。
1950年代には、フランスのジャン・ドーセにより、頻繁に輸血を受けた人の血液をもとに得られた血清に、他人の白血球を凝集させる抗原があることが発見され、HLAの発見となった。
MHCの研究は当初、ジョージ・スネル、バルフ・ベナセラフ、ジャン・ドーセ、ヒュー・マグデビットなどによって、遺伝子が発見された。ジョージとバルフとジャンの3人は1980年にMHCの研究業績によりノーベル生理学・医学賞を受賞した。
その後、1987年にはハーバード大学で当時は研究員だったPamela J. BjorkmanによってMHCクラスI抗原タンパク質の結晶化に成功し、X線で結晶構造が解析された。
1993年には、ジャック・ストロミンジャーがMHC-ペプチド複合体の溝の仕組みを解明したことなどの業績で、アメリカの医学賞であるラスカー賞をDon Wiley、Emil R. Unanueとともに受賞し、1999年にはストロミンジャーとWileyが日本国際賞を受賞した。また、1978年にスイスのロルフ・ツィンカーナーゲルが、T細胞がウイルスを殺害する際に抗原だけでなくMHCも認識する必要があることを発見し、これらの業績により1996年にノーベル生理学・医学賞を受賞した。
アクセサリー分子
MHCおよびそれと結合するTCRは、抗原提示反応において中心的な特別的な役割をしていると考えられている。しかし、MHC・TCR以外にも抗原提示に関わる分子(ここでいう「分子」とは何らかの細胞表面にある特別なタンパク質の意味)は発見されており、CD40(抗原提示細胞 側)とそれに接着するCD154(T細胞 側)、CD58(抗原提示細胞 側)とそれに接着するCD2(T細胞 側)、などの接着分子も発見されている。
これら、MHCとTCR以外の接着分子のことを「アクセサリー分子」[33]または「アクセサリーたんぱく質」などという。
脚注
- ^ Belov K, Deakin JE, Papenfuss AT, et al. "Reconstructing an ancestral mammalian immune supercomplex from a marsupial major histocompatibility complex", PLoS Biology, Vol.4, No.3, 2006, p.p. 317-318 (e46). PMID 16435885
- ^ a b Janeway CA, Travers P, Walport M, Shlomchik M. "Imunobiology. The immune system in health and desease. 5th edition." Garland Publishing Inc., New York, 2001. Part 2. 5-9. Many proteins involved in antigen processing and presentation are encoded by genes within the major histocompatibility complex.
- ^ 宮坂昌之 ほか編集『標準免疫学』、医学書院、2016年2月1日 第3版 第2刷、128ページ、右段の4~10行目付近
- ^ J.M.Bergほか著『ストライヤー生化学』、入村達郎ほか訳、第7版、936ページ、2013年2月22日発行、第1刷、
- ^ 東京書籍『生物』(高等学校の理科用の検定教科書)、平成24年3月15日検定済み、平成26年2月10日発行、29ページ
- ^ 椎名陸、「MHC領域の比較ゲノム解析」 日本組織適合性学会誌 2006年 13巻 2号 p.139-155, doi:10.12667/mhc.13.139
- ^ 笠原正典、「MHCはどのように進化してきたのか?」 日本組織適合性学会誌 1994年 1巻 2号 p.135-138, doi:10.12667/mhc.1.135
- ^ 小山次郎ほか著、『免疫学の基礎』、東京化学同人、2013年8月1日発行 第4版 第5冊、166ページの第2段落(ページ上側)
- ^ 梶川瑞穂ほか『非古典的MHCクラスI分子の構造と機能』、生化学(雑誌名)第81巻3号、2009年、 2018年に閲覧
- ^ 熊ノ郷淳ほか『免疫学コア講義』、南山堂、2019年3月25日 4版 2刷、28ページ
- ^ 河本宏『もっとよくわかる! 免疫学』、2018年5月30日 第8刷、31ページ
- ^ 宮坂昌之 ほか編集『標準免疫学』、医学書院、2016年2月1日 第3版 第2刷、116ページ、左段の中付近
- ^ 谷口克 ほか著、『標準免疫学』、2016年2月1日 第3版、298ページ、
- ^ Lodish 原著、石浦章一 翻訳『分子細胞生物学』、東京化学同人、2016年4月20日 第7版、946ページ
- ^ Gao X, Nelson GW, Karacki P, et al. "Effect of a single amino acid change in MHC class I molecules on the rate of progression to AIDS." NEJM., Vol.344, No.22, 2001, p.p. 1668-1675. PMID 11386265
- ^ 本間研一 ほか編集『標準生理学』、医学書院、2015年8月1日 第8版 第2刷、536ページ、左段の中付近
- ^ 宮坂昌之 ほか編集『標準免疫学』、医学書院、2016年2月1日 第3版 第2刷、129ページ、左段の中付近
- ^ Bjorkman PJ, Saper MA, Samraoui B, et al. "Structure of the human class I histocompatibility antigen, HLA-A2." Nature, Vol.329, No.6139, 1987, p.p. 506-512. PMID 3309677
- ^ 熊ノ郷淳ほか『免疫学コア講義』、南山堂、2019年3月25日 4版 2刷、29ページ
- ^ a b c Daar AS, Fuggle SV, Fablre JW, et al. "The detailed distribution of HLA-A, B, C antigens in normal human organs." Transplantation, Vol.38, No.3, 1984, p.p. 287-292. PMID 6591601
- ^ Fernandez JE, Concha A, Aranega A, et al. "HLA class I and II expression in rhabdomyosarcomas." Immunobiology, Vol.182, No.5, 1991, p.p. 440-448. PMID 1916885
- ^ Hicklin DJ, Marincola FM, Ferrone S. "HLA class I antigen downregulation in human cancers: T-cell immunotherapy revives an old story." Molecular Medicine Today, Vol.5, No.4, 1999, p.p. 178-186. PMID 10203751
- ^ Kitamura H, Torigoe T, Honma I, et al. "Effect of human leukocyte antigen class I expression of tumor cells on outcome of intracesical instillation of bacillus calmette-guerin immunotherapy for bladder cancer." Clinical Cancer Research, Vol.12, No.15, 2006, p.p. 4641-4644. PMID 16899613
- ^ Khong HT, Restifo NP. "Natural selection of tumor variants in the generation of "tumor escape" phenotypes." Nature Immunology, Vol.3, No.11, 2002, p.p. 999-1005. PMID 12407407
- ^ 『標準免疫学』第3版、123ページの上の図、
- ^ Karre K, Ljunggren HG, Piontek G, Kiessling R. "Selective rejection of H-2-deficient lymphoma variants suggests alternative immune defence strategy." Nature, Vol.319, No.6055, 1986, p.p. 675-678. PMID 3951539
- ^ Janeway CA, Travers P, Walport M, Shlomchik M. "Imunobiology. The immune system in health and desease. 5th edition." Garland Publishing Inc., New York, 2001. Part 2. 5-11. Specialized MHC class I molecules act as ligands for activation and inhibition of NK cells.
- ^ a b The MHC sequencing consortium. "Complete sequence and gene map of a human major histocompatibility complex", Nature, Vol.401, No.6756, 1999, p.p. 921-923. PMID 10553908
- ^ Gruen JR, Weissman SM. "Evolving views of the major histocompatibility complex." Blood, Vol.90, No.11, 1997, p.p. 4252-4265. PMID 9373235
- ^ Entrez Gene: B2M beta-2-microglobulin (Homo sapiens )
- ^ Entrez Gene: B2m beta-2-microglobulin (Mus musculus )
- ^ a b Kaufman J, Milne S, Gobel TW, et al. "The chicken B locus is a minimal essential major histocompatibility complex." Nature, Vol.401, No.6756, 1999, p.p. 923-925. PMID 10553909
- ^ JEFFREY K.ACTOT原著、大沢利昭・今井康之 訳『インテグレーテッドシリーズ免疫学・微生物学』、東京化学同人、2010年3月15日、第1版 第1刷
参考文献
- 宮坂昌之 ほか編集『標準免疫学』、医学書院、2016年2月1日 第3版 第2刷
- Lodish ほか原著、石浦章一 翻訳『分子細胞生物学』、東京化学同人、2016年4月20日 第7版
- J.M.Bergほか著『ストライヤー生化学』、入村達郎ほか訳、936ページ、2013年2月22日発行 第7版 第1刷、
