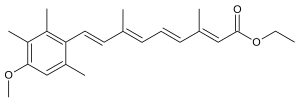
エトレチナート
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| Drugs.com | Micromedex Detailed Consumer Information |
| MedlinePlus | a601010 |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 薬物動態データ | |
| 半減期 | 120 days |
| 識別 | |
| CAS番号 |
54350-48-0 |
| ATCコード | D05BB01 (WHO) |
| PubChem | CID: 5282375 |
| DrugBank |
APRD00966 |
| ChemSpider |
4445538 |
| UNII |
65M2UDR9AG |
| KEGG |
D00316 |
| ChEBI |
CHEBI:4913 |
| ChEMBL |
CHEMBL464 |
| 化学的データ | |
| 化学式 | C23H30O3 |
| 分子量 | 354.483 g/mol |
| |
エトレチナート(英語: Etretinate)とは、ビタミンA誘導体であり乾癬や毛孔性苔癬に有効とされる薬である。ロシュが開発し、FDAは1986年に承認した。欧米ではテジソン (Tegison) の名で発売されていたが、催奇性という強い副作用のために1996年にカナダ、1998年に米国で使用禁止となっている。日本では中外製薬からチガソン (Tigason) の名で発売されており[1]、先進国では唯一発売が続けられている。日本国内でも2例の先天異常症例が報告されており、製造元である中外製薬が定期的に注意喚起を行っている[2]。
効能・効果
[編集]諸治療が無効かつ重症な下記疾患
- 乾癬群(尋常性乾癬、膿疱性乾癬、乾癬性紅皮症、関節症性乾癬)、
- 魚鱗癬群(尋常性魚鱗癬、水疱型先天性魚鱗癬様紅皮症、非水疱型先天性魚鱗癬様紅皮症)、
- 掌蹠角化症、ダリエー病、掌蹠膿疱症、毛孔性紅色粃糠疹および紅斑性角化症、
- 口腔白板症、口腔乳頭腫および口腔扁平苔癬
服用時の注意点
[編集]ビタミンAの薬との併用は不可[1]。ビタミンAの過剰摂取となり肝機能などに悪影響を与える危険性がある。また、骨棘の形成や靱帯の石灰化等の過骨症変化及び長管骨の骨膜肥厚等の造骨性変化を生じる事がある[3][4]。長期の服用の場合定期的に骨X線[4]、肝機能、中性脂肪の検査を行う必要がある。
日本では、レチノイド(ビタミンA)の脂溶性が強く、体内に長期間蓄積されることから、服用中はもちろん、服用後の妊娠につながる性行為(女性は最低2年間・男性は最低6ヶ月間の避妊が必要)と、男女とも最低2年間は献血をしてはならない事となっている[1][2]。処方に当たっては皮膚科医師からの説明の上、同意書を交わす[1][2]。閉経前の女性に対しては、妊娠検査を行い、妊娠していないことを確認される事もある。そして薬剤師の問診・確認を済ませて初めて処方されることとなっている。
禁忌
[編集]妊婦、肝障害または腎障害のある患者、ビタミンA製剤を服用中の患者、過敏症のある患者には禁忌である。
副作用
[編集]滅多に発生することはないが以下の症状が出た場合医療機関に受診を薦める。
- 高熱、ひどい発疹・発赤、唇や口内の爛れ、のどの痛み、水ぶくれ、皮がむける、強い痛み、目の充血(これらの症状は重い皮膚症状である)
- だるい、食欲不振、吐き気、発熱、発疹、かゆみ、皮膚や白目が黄色くなる、尿が褐色(これらの症状は重い肝臓の重い症状である)
なお、副作用の発生率は71.0%であり[1]、
- 皮膚症状:落屑(27.7%)、皮膚菲薄化(13.7%)、そう痒(12.4%)、脱毛(6.6%)、爪囲炎(5.5%)、
- 粘膜異常:口唇炎(51.5%)、口内乾燥(24.8%)、鼻腔乾燥(6.3%)、口角炎(7.9%)
の発生頻度が高い他、重大な副作用として上記の催奇性の他に、中毒性表皮壊死症(Lyell症候群)、多形紅斑、血管炎が記載されている。
出典
[編集]- ^ a b c d e “チガソンカプセル10/チガソンカプセル25 添付文書” (2014年7月). 2016年7月1日閲覧。
- ^ a b c 中外製薬 (2014年2月). “角化症治療剤チガソン適正使用のお願い ― 催奇形性について ―” (PDF). 医薬品医療機器総合機構. 2016年8月4日閲覧。
- ^ 清島真理子、青山裕美、森俊二 ほか、エトレチナート内服中に造骨性変化のみられた乾癬の1例 日本皮膚科学会雑誌 Vol.102 (1992) No.5 p.569-, doi:10.14924/dermatol.102.569
- ^ a b ほか、エトレチナート長期内服に伴う骨,関節変化-16症例の検討- 日本皮膚科学会雑誌 Vol.101 (1991) No.5 p.547-, doi:10.14924/dermatol.101.547
