水酸化バリウム
| 水酸化バリウム | |
|---|---|

| |
水酸化バリウム | |
| 識別情報 | |
| CAS登録番号 | [17194-00-2 (無水物) [22326-55-2] (1水和物) [12230-71-6] (8水和物) [17194-00-2] (無水物) [22326-55-2] (1水和物) [12230-71-6] (8水和物)] |
| 特性 | |
| 化学式 | Ba(OH)2 |
| モル質量 | 171.34 g mol−1 |
| 外観 | 無色結晶または白色粉末 |
| 密度 | 4.495 g cm−3(無水物) 4.495 g cm−3 (1水和物)3.74 g cm−3(8水和物) |
| 融点 |
408 ℃ |
| 沸点 |
780 (分解) |
| 水への溶解度 | 1.68 g / 100 cm3(0℃) 3.89 g / 100 cm3(20℃) 5.6 g / 100 cm3(25℃) 8.23 g / 100 cm3(40℃) 20.95 g / 100 cm3(60℃) 101.4 g / 100 cm3(80℃) |
| 構造 | |
| 結晶構造 | 単斜(無水)、正方(8水和物) |
| 熱化学 | |
| 標準生成熱 ΔfH |
-944.7 kJ mol−1 |
| 危険性 | |
| EU Index | 056-002-00-7 |
| NFPA 704 | |
| Rフレーズ | R20/22 |
| Sフレーズ | (S2), S28 |
| 引火点 | 不燃性 |
| 関連する物質 | |
| 関連物質 | 水酸化ベリリウム 水酸化マグネシウム 水酸化カルシウム 水酸化ストロンチウム |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
水酸化バリウム(すいさんかバリウム、Barium hydroxide)は塩基性の無機化合物で、バリウムの水酸化物であり化学式 Ba(OH)2 で表される。バリウムイオンと水酸化物イオンよりなるイオン結晶であり、粒状または粉末状の外観を持つ。最も一般的な形として1水和物が市販されている。一般の水溶性バリウム化合物と同様に毒性が強く劇物に指定されている。
バリタ (baryta) とも呼ばれ、飽和水溶液(バリタ水)は水酸化カルシウム同様に二酸化炭素を吹き込むと炭酸バリウムが析出し、白く濁ることで知られる。
調製[編集]
酸化バリウム (BaO) を水に溶解させることによって生成する。再結晶すると8水和物が得られ、これを空気中で加熱すると1水和物となる。減圧下で100℃に加熱すると無水物が得られる[1]。 ただしこの水和反応は生石灰の消和よりも激しく危険を伴う。
- ,
化学的性質[編集]
水酸化カルシウムより脱水に対し安定であり無水物は408℃で熔融するが、さらに加熱すると脱水が始まり998℃で水蒸気の解離圧が1気圧に達する。
無水物の水に対する溶解熱はかなり発熱的である[2]。
- ,
しかし、78℃以下において水溶液から析出する固相は八水和物であり、八水和物の溶解熱は著しく吸熱的であるため、溶解度は温度の上昇と伴に著しく増大する。
- ,
0.05mol/dm3(0.1N)の水溶液の電離度は約0.8であり強塩基として分類され、水酸化カルシウムよりも溶解度は高く塩基としての作用も強い。 水酸化バリウムを酸で中和したものであるバリウム塩水溶液の加水分解はほとんど無視し得る。水和バリウムイオンの酸解離定数(pKa)は以下の通りである。
- ,
従って水酸化バリウムの第二段階塩基解離定数は以下のようになる。
- ,
用途[編集]
分析化学において弱酸、特に有機酸の滴定に用いられる。水酸化バリウムの水溶液は透明であれば炭酸塩を含まないことを示すが、これは水酸化ナトリウムや水酸化カリウムには見られない特徴であり、炭酸バリウムが水に不溶なためである。この性質を利用すると、アルカリ性で変色するフェノールフタレインやチモールフタレインを指示薬として使う際に、弱塩基である炭酸イオンが存在しても終点誤差を出すことなく滴定を行うことができる[3]。
有機合成においては強塩基としてエステル[4]やニトリル[5][6][7]の加水分解に用いられる。
酸性の物質をこぼした際に、これを中和して危険性を減らす目的にも使われる。
ウンデカンカルボン酸ジメチルエステルのエステル基のうち片方だけを加水分解する反応に用いられている[8]。
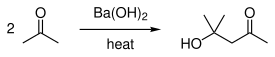
また、シクロペンタノン[9]、ジアセトンアルコール(4-ヒドロキシ-4-メチル-2-ペンタノン)[10]、D-グロン酸-γ-ラクトン[11]の合成にも用いられる。
安全性[編集]
他の強塩基や水溶性のバリウム化合物と同様の注意を要する。腐食性があり、有毒である。
法規制[編集]
日本では毒物及び劇物取締法および毒物及び劇物指定令によりバリウム化合物として劇物に指定されている。 他に、消防法、労働安全衛生法、大気汚染防止法、船舶安全法、航空法、PRTR法にも規定がある。
参考項目
脚注[編集]
- ^ (1960). Gmelins Handbuch der anorganischen Chemie, 8. Aufl.; Verlag Chemie: Weinheim, p. 289.
- ^ D.D. Wagman, W.H. Evans, V.B. Parker, R.H. Schumm, I. Halow, S.M. Bailey, K.L. Churney, R.I. Nuttal, K.L. Churney and R.I. Nuttal, The NBS tables of chemical thermodynamics properties, J. Phys. Chem. Ref. Data 11 Suppl. 2 (1982).
- ^ Mendham, J.; Denney, R. C.; Barnes, J. D.; Thomas, M. J. K.; Denney, R. C.; Thomas, M. J. K. Vogel's Quantitative Chemical Analysis, 6th ed.; Prentice Hall: New York. ISBN 0-582-22628-7.
- ^ Meyer, K.; Bloch, H. S. (1945). "Naphthoresorcinol". Organic Syntheses (英語). 25: 73.; Collective Volume, vol. 3, p. 637
- ^ Brown, G. B. (1946). "Methylsuccinic acid". Organic Syntheses (英語). 26: 54.; Collective Volume, vol. 3, p. 615
- ^ Ford, J. H. (1947). "β-Alanine". Organic Syntheses (英語). 27: 1.; Collective Volume, vol. 3, p. 34
- ^ Anslow, W. K.; King, H.; Orten, J. M.; Hill, R. M. (1925). "Glycine". Organic Syntheses (英語). 4: 31.; Collective Volume, vol. 1, p. 298
- ^ Durham, L. J.; McLeod, D. J.; Cason, J. (1958). "Methyl hydrogen hendecanedioate". Organic Syntheses (英語). 38: 55.; Collective Volume, vol. 4, p. 635
- ^ Thorpe, J. F.; Kon, G. A. R. (1925). "Cyclopentanone". Organic Syntheses (英語). 5: 37.; Collective Volume, vol. 1, p. 192
- ^ Conant, J. B.; Tuttle, N. (1921). "Diacetone alcohol". Organic Syntheses (英語). 1: 45.; Collective Volume, vol. 1, p. 199
- ^ Karabinos, J. V. (1956). "D-Gulonic γ-lactone". Organic Syntheses (英語). 36: 38.; Collective Volume, vol. 4, p. 506
関連項目[編集]
参考項目
- 水酸化バリウム水溶液 理科ねっとわーく(一般公開版) - 文部科学省 国立教育政策研究所




![{\displaystyle {\ce {Ba(OH)2 \ ->[\Delta] \ {BaO}+ H2O}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/5047c829bb9892b2c1e332d593cdad3789928426)