グリニャール試薬
グリニャール試薬(グリニャールしやく、英: Grignard reagent)はヴィクトル・グリニャールが発見した有機マグネシウムハロゲン化物で、一般式が R−MgX と表される有機金属試薬である(R は有機基、X はハロゲンを示す)。多彩な用途を持ち、有機金属化学の黎明期を支えた試薬であり、今もなお有機合成には欠かせない有機反応試薬として、近代有機化学史を通して非常に重要な位置を占めている[1][2]。
その調製は比較的容易であり、ハロゲン化アルキルにエーテル溶媒中で金属マグネシウムを作用させると、炭素-ハロゲン結合が炭素-マグネシウム結合に置き換わりグリニャール試薬が生成する。生成する炭素-マグネシウム結合では炭素が陰性、マグネシウムが陽性に強く分極しているため、グリニャール試薬の有機基は強い求核試薬 (形式的には R−)としての性質を示す。
また、強力な塩基性を示すため、酸性プロトンが存在すると、酸塩基反応によりグリニャール試薬は炭化水素になってしまう。そのため、水の存在下では取り扱うことができず、グリニャール試薬を合成する際には原料や器具を十分に乾燥させておく必要がある。これらの反応性や取り扱いはアルキルリチウムと類似している。
調整済のグリニヤール試薬が市販されており、工業的スケールで使用することができる[3]。
発見
[編集]
グリニャール試薬の発見までは1849年にエドワード・フランクランドによって発見されたジアルキル亜鉛がアルキル化剤として使用されていた。しかしジアルキル亜鉛には空気と触れると容易に発火する、調製できるアルキル基が限られている、反応性があまり高くないといった問題点があった。
ヴィクトル・グリニャールの師匠であったフィリップ・バルビエールはカルボニル化合物とハロゲン化アルキルの混合物をマグネシウムに作用させると、ハロゲン化アルキルのアルキル基がカルボニル化合物に付加したアルコールが得られることを発見していた。しかし反応の再現性が悪かったため、グリニャールにより詳しい検討を行なうように勧めた。
フランクランドはジアルキル亜鉛をエーテル中で調製する方法を試みていた。しかしこの方法ではジアルキル亜鉛にエーテルが配位した化合物が沈殿してしまい利用が困難であった。1900年にグリニャールはこの方法をマグネシウムに適用し、亜鉛の場合とは異なり均一な有機金属化合物の溶液が得られてくること、この有機金属化合物が多くのカルボニル化合物と反応することを発見した[4]。
この有機金属化合物は R−MgX の組成を持つと考えられ、この化合物はグリニャール試薬と呼ばれるようになった。1912年にグリニャールはこの業績によりノーベル化学賞を受賞した。
調製
[編集]グリニャール試薬の調製法は
- ハロゲン化アルキルとマグネシウムの反応
- 酸性度の高い炭化水素に他のグリニャール試薬を作用させる
- ハロゲン化アルキルと他のグリニャール試薬の金属-ハロゲン交換反応
- 他の有機金属化合物とハロゲン化マグネシウムとのトランスメタル化反応
などが知られている。
ハロゲン化アルキルとマグネシウムの反応
[編集]一般的なグリニャール試薬はハロゲン化アルキルとマグネシウムの反応で調製される。これは以下のように行なう。
- 良く乾燥し不活性ガス(窒素、アルゴン)で置換した反応容器にマグネシウムを入れる。ここで撹拌してマグネシウムを少し破砕しておくとグリニャール試薬の生成がスムーズになる[5]。
- ここにマグネシウムが浸る程度のエーテル系溶媒を加える。多くの場合ジエチルエーテルかテトラヒドロフランが使用される。
- ヨウ素や1,2-ジブロモエタンといった活性化剤を少量添加して加熱、撹拌する。これらの活性化剤はマグネシウム表面の酸化物の皮膜を溶解させて活性化する。
- 少量のハロゲン化アルキルのエーテル溶液を添加し撹拌する。多くの場合、反応溶液は一旦濁った後、グリニャール試薬の生成に伴う急激な温度の上昇を伴って黒色から褐色の透明な溶液になる。グリニャール試薬の生成は自触媒反応であるとされており急激な反応となる。そのためグリニャール試薬の生成に伴う発熱が起こる前に、ハロゲン化アルキルを多く加えすぎているとグリニャール試薬の生成が起こった際の発熱が大きすぎて反応が暴走し、あたりに反応溶液が撒き散らされる結果となってしまう。
- 残りのハロゲン化アルキルのエーテル溶液を適切な反応温度を保つスピードで滴下していく。
-
マグネシウム片をフラスコに入れる。白いものは攪拌子。
-
溶媒を入れ、活性化のためヨウ素の小片を加える。
-
アルキルハライドの溶液を滴下する。
-
滴下終了後、しばらく加熱を続ける。
-
グリニャール試薬の生成が完了。少量のマグネシウムが未反応のまま残っている。
-
次の反応に備え、溶液を冷却する。グリニャール試薬が白色固体として析出している。
-
カルボニル化合物の溶液を滴下する。
-
滴下終了後、溶液を室温まで温める。付加反応は完了しており、このあと加水分解を行う。
ハライドの反応性
[編集]グリニャール試薬生成の際の反応性はヨウ化アルキル > 臭化アルキル > 塩化アルキルの順でフッ化物は普通の調製法ではグリニャール試薬を生成しない。また同じハロゲン原子においては反応性は第1級ハライド > 第2級ハライド > 第3級ハライドの順である。
逆にグリニャール試薬自身の求核性は塩化物 > 臭化物 > ヨウ化物であるので、適切なハロゲン化物の選択が重要となる場合もある。
マグネシウム
[編集]グリニャール試薬の調製には削り屑状マグネシウム (magnesium turning) を使用することが多い。粉末状のマグネシウムでは反応速度が速くなりすぎて局所的な加熱によるウルツカップリングが起こりやすくなり、収率が低下するためである。
マグネシウムの活性化には、機械的撹拌や、あるいはヨウ素や1,2-ジブロモエタンの添加が行われる。ヨウ素はマグネシウムの酸化膜を切削する。1,2-ジブロモエタンがマグネシウムと反応すると臭化マグネシウムとエチレンを生成する。また、グリニャール試薬の生成が自触媒反応であることを利用して、以前に調製したグリニャール試薬を開始剤として添加する場合もある。
溶媒
[編集]用いるエーテル系溶媒の選択も重要である。マグネシウムへの配位力の高い溶媒ほどグリニャール試薬生成の際の反応性を高める。そのためジエチルエーテルよりテトラヒドロフランや1,2-ジメトキシエタンの方がグリニャール試薬生成の反応性は高い。このためアルケニルハライドやアリールハライドのような反応性の低いハライドからのグリニャール試薬の調製は普通テトラヒドロフラン中で行われる。しかし逆に、テトラヒドロフランはウルツカップリングを促進するので、反応性の高いヨウ化アルキルやハロゲン化アリル、ハロゲン化ベンジルからグリニャール試薬を調製する場合には収率が大きく低下する場合がある。これらのテトラヒドロフラン溶液が必要な場合には、一旦ジエチルエーテル中でグリニャール試薬の調製を行ってから溶媒置換を行う方がよい。
ジオキサンはエーテル系溶媒であるものの、マグネシウムハライドと不溶性の錯体を作るため、後述するシュレンク平衡によりグリニャール試薬が反応性の低いジアルキルマグネシウムへと変化してしまう。そのため、グリニャール試薬の調製には用いない。
グリニャール試薬自体はトルエンなどの芳香族系の溶媒にも溶解し、反応に用いることができるが、芳香族系の溶媒中ではグリニャール試薬の生成は極めて遅く調製が困難である。そのため芳香族系の溶媒が必要な場合にはエーテル系溶媒でグリニャール試薬の調製を行った後、溶媒置換を行うのが普通である。
トリエチルアミンなどの第3級アミン中でもグリニャール試薬の調製は可能であるが、生成したグリニャール試薬の反応性が低いため、あまり使用されることはない。
溶媒の使用量は、一般的なグリニャール試薬では 1 mol/L 程度の濃度になるようにすることが多い。濃すぎるとグリニャール試薬が析出してしまい、後述する逆滴下法が不可能になる場合もある。ウルツカップリングが起こりやすい反応性の高いハライドからの調製ではもっと希釈した濃度で調製が行われる。
反応温度
[編集]反応温度は多くの場合、−20 ℃ 程度からテトラヒドロフラン還流程度の温度で行なわれる。反応しにくいハライドほど高い温度が必要となる。反応温度が高いほどウルツカップリングが促進されるので、ウルツカップリングを起こしやすいハライドではなるべく低温で反応させる。一方、反応性の低いハライドでは反応温度が低すぎるとグリニャール試薬の生成が停止してしまい、温度を上げた途端に反応が再開して暴走することがあるので注意が必要である。
反応機構
[編集]ハロゲン化アルキルと金属マグネシウムは一電子移動によって発生するラジカル中間体を経由して反応するとされる[6]。機構を以下に示す。式中で が付された分子はラジカル種であることを示す。
まずハロゲン化アルキル R−X が金属マグネシウムから電子を1個奪い、ラジカルアニオン R−X•− となる。発生したラジカル R−X•− からハロゲンアニオンが脱離し、アルキルラジカル R• となる。脱離したハロゲンアニオンと先に発生した1価のマグネシウムカチオンは XMg• を形成し、これと R• が結合することによって RMgX が生成する。以上の反応は金属マグネシウムの表面上で起こるとされている。
酸性度の高い炭化水素からの調製
[編集]この方法がとられるのは主に末端アルキニルのグリニャール試薬である。末端アルキンにアルキルグリニャール試薬(エチルグリニャール試薬が使用されることが多い)を反応させると、グリニャール試薬が塩基として働き、末端アルキンからプロトンが引き抜かれてアルキニルグリニャール試薬が生成する[7]。
金属-ハロゲン交換反応による調製
[編集]この方法は室温ではグリニャール試薬と反応してしまうエステルやニトリルなどの官能基を持つ芳香族化合物のグリニャール試薬を調製するために利用される。−40 ℃ 以下の低温で、芳香族ハロゲン化物にイソプロピルグリニャール試薬のようなかさ高いグリニャール試薬を反応させると金属-ハロゲン交換反応によりアリールグリニャール試薬が生成する[8]。
トランスメタル化による調製
[編集]他の有機金属化合物にマグネシウムハライドを作用させるとトランスメタル化によりグリニャール試薬が生成する。この方法も室温ではグリニャール試薬と反応してしまうエステルやニトリルなどの官能基を持つグリニャール試薬を調製するのに使用されることがある。
組成
[編集]グリニャール試薬は通常 R−MgX の形式で書かれるが、実際には複雑な組成を持っているとされている。このことを最初に指摘したのはヴィルヘルム・シュレンクであり、溶液中でジアルキルマグネシウムとの平衡が存在することを指摘した[9]。
この平衡はシュレンク平衡と呼ばれる。
さらにマグネシウムは通常4配位をとるため、グリニャール試薬のマグネシウムには溶媒であるエーテル分子の酸素が配位している。また、グリニャール試薬の濃度や溶媒の種類によっては、溶媒やハロゲン原子を介して複数のマグネシウムが架橋した複核錯体を形成している。配位力の強いテトラヒドロフランや1,2-ジメトキシエタンでは単核錯体であるが、ジエチルエーテル中では濃度が高い場合には二核錯体、濃度が低い場合には単核錯体となっているとされている。
反応
[編集]強い求核性と強塩基性により反応性に富むため、様々な化合物を合成するのに有用である。
反応を行なう方法には主に3つの方式がある。これらを総称してグリニャール反応という。
- グリニャール試薬の溶液に反応させる基質を滴下する。
- グリニャール試薬を調製する際に、ハロゲン化アルキルとともに基質を滴下する(バルビエール法)。
- グリニャール試薬の溶液を反応させる基質の溶液に滴下する(逆滴下法)。
バルビエール法はウルツカップリングを起こしやすいアリルやベンジルのグリニャール試薬を反応させる場合に使用される。逆滴下法は2当量以上のグリニャール試薬の反応が可能な基質に対して、1当量だけグリニャール試薬を作用させたい場合などに使用される。例えばカルボン酸クロリドからケトンを合成したい場合などである。
以下に反応の例を示す。
求核剤としての反応
[編集]カルボニル化合物との反応
[編集]- ホルムアルデヒド (HCHO) と反応させ酸で処理すると第一級アルコール (R−CH2OH) が生成する。
- アルデヒド (R'−CHO) と反応させ酸で処理すると第二級アルコール (R−CR'(OH)H) が生成する[10][11]。
- ケトン (R'−C(=O)−R'') と反応させ酸で処理すると第三級アルコール (R−CR'(R'')OH) が生成する[12]。
- エステル (R'−C(=O)O−R'') とグリニャール試薬2当量を反応させ酸で処理すると第三級アルコール (R'−CR2OH) が生成する。この時アルコール (R''−OH) も得られる[13][14]。
- ハロゲン化アシル (R'−C(=O)−X)、カルボン酸無水物、カルボン酸チオエステルと −78 ℃でグリニャール試薬を反応させるとケトン (R−C(=O)−R') が生成する。温度が高い場合にはさらに生成したケトンへの付加が進む[15]。
- 一般的な第三級カルボン酸アミドとの反応は反応性が低いためあまり用いられないが、ホルムアミドとの反応はアルデヒドの合成法として知られる。また、ワインレブアミドとの反応はケトンを合成する良い方法として知られている。
- 二酸化炭素と反応させ、酸で処理するとカルボン酸 (R−C(=O)OH) を生成する[16][17][18]。
- α,β-不飽和カルボニル化合物との反応では、通常 1,2-付加が優先するが、カルボニル基が立体的に障害されている場合には 1,4-付加も起こる。1,2-付加を選択的に行いたい場合にはセリウム塩の添加が、1,4-付加を選択的に行ないたい場合には銅塩の添加が有効である。

カルボニル化合物との反応
反応機構
[編集]既に述べたようにグリニャール試薬は反応溶液中でシュレンク平衡を起こしているため、反応の機構を速度論に基づいて検討することは難しく、完全には理解されていない。一般的には (A) 4員環状の遷移状態を経る協奏的なもの、(B) ラジカルを経由する段階的なものの2つが提案されており、用いる基質によってこれらのうちいずれかの機構がとられると考えられている。

アルキル基など電子求引性の弱い置換基をもつケトンとの反応の場合はAを、あるいは立体障害の大きいカルボニル化合物やグリニャール試薬を用いた場合はBを経由することが知られている[19]。
その他の付加・置換反応
[編集]- アリルハライドやベンジルハライドとはSN2反応によりカップリング反応を起こす[20]。その他のハロゲン化アルキルとはそのままでは反応しにくいが、銅塩を添加すると反応が進行する。
- エポキシドとSN2反応してアルコールを生成する。付加は立体的に空いている側の炭素上で進行する[21]。
- 酸素と反応してヒドロペルオキシドを経てアルコールを生成する。
- N-アルキルイミンとグリニャール試薬の反応ではアミンが生成する[22]。
- ニトリル (R'−CN) とグリニャール試薬 (RMgX) を反応させ酸で処理するとケトン (R−C(=O)−R') が生成する。ニトリルの場合には付加で生成するイミダート (R−C(=NMgX)−R') への2段階目の付加が極めて遅いため、そのまま酸加水分解でケトンが生成する[23]。
- 単体硫黄との反応ではチオールを生成する[24]。
- ジスルフィドとの反応では S−S 結合を開裂させて、チオールとスルフィドを生成する。
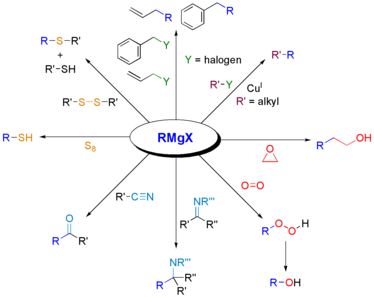
その他の付加・置換反応
塩基としての反応
[編集]グリニャール試薬は強い塩基であるため、水、アルコール、アミンといったブレンステッド酸からプロトンを引き抜いて、アルコキシドやアミドを生成する。末端アルキンに対してアルキルグリニャール試薬を作用させると、塩基として作用してアルキニルグリニャール試薬が生成する[25]。
かさ高いケトンに対して、イソプロピルや tert-ブチルといったかさ高いグリニャール試薬を作用させると、一部塩基として作用してエノラートが生成する。またα-水素を持つニトリルでも一部同じように反応する。これらの生成したアニオンは求核付加を受けず、反応終了時の酸による加水分解で原料に戻る。
還元剤としての反応
[編集]かさ高いケトンに対してグリニャール試薬を作用させると、多くの場合求核付加を起こさずにケトンが還元されてアルコールになった生成物が得られる。
この反応はグリニャール試薬のβ-水素がカルボニル基に転位して起こる。グリニャール試薬のマグネシウムにケトンが配位した後、メーヤワイン・ポンドルフ・バーレイ還元と類似した6員環遷移状態を経由して起こっている反応機構が考えられている。ゆえに、β-水素を持たないメチルグリニャールではこの反応は起こらない。
そのほかの反応
[編集]他の金属化合物とトランスメタル化を起こすため、任意のアルキル金属錯体を調製する原料として重要である。
また、ニッケル触媒の存在下でアルケニルハライドやアリールハライドとクロスカップリング反応のひとつである熊田・玉尾反応を起こす。
アルキルグリニャール試薬に当モル量のアルキルリチウムを作用させると R3MgLi の形のアート錯体が発生する。これは求核性の高い試薬として、低温での選択的なハロゲン-メタル交換反応に利用される[26]。
参考文献
[編集]- ^ Smith, M. B.; March, J. Advanced Organic Chemistry, 5th ed.; John-Wiley & Sons: New York, 2001. ISBN 0-471-58589-0 - グリニャール試薬を用いた反応を網羅している。
- ^ Kürti, L.; Czakó, B. Storategic Applications of Named Reactions in Organic Chemistry; Elsevier: Amsterdam, 2005; pp 188–189. ISBN 0-12-429785-4 - グリニャール反応に関する論文など38の参考文献が記載されている。
- ^ 一哉, 岡野「グリニャール試薬,ターボ·グリニャール試薬」『有機合成化学協会誌』第72巻第7号、2014年、836–839頁、doi:10.5059/yukigoseikyokaishi.72.836。
- ^ Grignard, V. "Some new organometaric combinations of magnesium and their application to the synthesis of alcohols and hydrocarbons". C. R. Acad. Sci. 1900, 1322–1324.
- ^ Baker, Karen V and Brown, John M and Hughes, Nigel and Skarnulis, A Jerome and Sexton, Ann (1991). “Mechanical activation of magnesium turnings for the preparation of reactive Grignard reagents”. The Journal of Organic Chemistry (ACS Publications) 56 (2): 698-703. doi:10.1021/jo00002a039. 撹拌後のマグネシウムの表面写真あり。
- ^ Garst, J. F.; Ungvary, F. "Mechanism of Grignard reagent formation". In Grignard Reagents; Richey, R. S., Ed.; John Wiley & Sons: New York, 2000; pp 185–275. ISBN 0-471-99908-3.
- ^ Wender, P. A.; Holt, D. A.; Sieburth, S. Mc N. "2-Alkenyl carbinols from 2-halo ketones: 2-E-propenylcyclohexanol". Org. Synth., Coll. Vol. 7, p. 456 (1990); Vol. 64, p. 10 (1986). オンライン版
- ^ Jensen, Anne Eeg and Dohle, Wolfgang and Sapountzis, Ioannis and Lindsay, David M and Vu, Viet Anh and Knochel, Paul (2002). “Preparation and reactions of functionalized arylmagnesium reagents”. Synthesis (Georg Thieme Verlag Stuttgart New York) 2002 (04): 0565-0569. doi:10.1055/s-2002-20955.
- ^ Schlenk, W.; Schlenk, W., Jr. Chem. Ber. 1929, 62B, 920.
- ^ Overberger, C. G.; Saunders, J. H.; Allen, R. E.; Gander, R. "m-Chlorophenylmethylcarbinol". Org. Synth., Coll. Vol. 3, p. 200 (1955); Vol. 28, p. 28 (1948). オンライン版
- ^ Drake, N. L.; Cooke, G. B. "Methyl isopropyl carbinol". Org. Synth., Coll. Vol. 2, p. 406 (1943); Vol. 12, p. 48 (1932). オンライン版
- ^ Adkins, H.; Zartman, W. "Triphenylethylene". Org. Synth., Coll. Vol. 2, p. 606 (1943); Vol. 17, p. 89 (1937). オンライン版
- ^ Allen, C. F. H.; Converse, S. "1,1-Diphenylethylene". Org. Synth., Coll. Vol. 1, p. 226 (1941); Vol. 6, p. 32 (1926). オンライン版
- ^ Riegel, B.; Moffett, R. B.; McIntosh, A. V. "3,12-Diacetoxy-bisnor-cholanyldiphenylethylene". Org. Synth., Coll. Vol. 3, p. 237 (1955); Vol. 24, p. 41 (1944). オンライン版
- ^ Ciabattoni, J.; Nathan, E. C.; Feiring, A. E.; Kocienski, P. J. "Tri-tert-butylcyclopropenyl tetrafluoroborate". Org. Synth., Coll. Vol. 6, p. 991 (1988); Vol. 54, p. 97 (1974). オンライン版
- ^ Gilman, H.; Kirby, R. H. "DL-Methylethylacetic acid". Org. Synth., Coll. Vol. 1, p.361 (1941); Vol. 5, p. 75 (1925). オンライン版
- ^ Puntambeker, S. V.; Zoellner, E. A. "Trimethylacetic acid". Org. Synth., Coll. Vol. 1, p. 524 (1941); Vol. 8, p. 104 (1928). オンライン版
- ^ Gilman, H.; St. John, N. B.; Schulze, F. "α-Naphthoic acid". Org. Synth., Coll. Vol. 2, p. 425 (1943); Vol. 11, p. 80 (1931). オンライン版
- ^ Holm, T.; Crossland, I. "Mechanistic features of the reaction of organomagnesium compounds". In Grignard Reagents; Richey, R. S., Ed.; John Wiley & Sons: New York, 2000; pp 1–26. ISBN 0-471-99908-3.
- ^ Lespieau, R.; Bourguel, M. "3-Cyclohexyl-2-bromopropene". Org. Synth., Coll. Vol. 1, p. 186 (1941); Vol. 6, p. 20 (1926). オンライン版
- ^ Dreger, E. E. "n-Hexyl alcohol". Org. Synth., Coll. Vol. 1, p. 306 (1941); Vol. 6, p. 54 (1926). オンライン版
- ^ Stork, G.; Dowd, S. R." Alkylations of aldehydes via reaction of the magnesioenamine salt of an aldehyde: 2,2-dimethyl-3-phenylpropionaldehyde". Org. Synth., Coll. Vol. 6, p. 526 (1988); Vol. 54, p. 46 (1974). オンライン版
- ^ Callen, J. E.; Dornfeld, C. A.; Coleman, G. H. "9-Acetylphenanthrene". Org. Synth., Coll. Vol. 3, p. 26 (1955); Vol. 28, p. 6 (1948). オンライン版
- ^ Cymerman-Craig, J.; Loder, J. W. "Methyl 2-thienyl sulfide". Org. Synth., Coll. Vol. 4, p. 667 (1963); Vol. 35, p. 85 (1955). オンライン版
- ^ Holmes, A. B.; Sporikou, C. N. "Trimethylsilylacetylene". Org. Synth., Coll. Vol. 8, p. 606 (1993); Vol. 65, p. 61 (1987). オンライン版
- ^ Inoue, Atsushi and Kitagawa, Kazuya and Shinokubo, Hiroshi and Oshima, Koichiro (2001). “Selective Halogen- Magnesium Exchange Reaction via Organomagnesium Ate Complex”. The Journal of Organic Chemistry (ACS Publications) 66 (12): 4333-4339. doi:10.1021/jo015597v.
関連文献
[編集]- 萩原秀樹、江口久雄「グリニャール試薬とクロスカップリング反応 —反応開発の歴史と産業利用について—」『化学と教育』第67巻第3号、日本化学会、2019年、126-129頁、doi:10.20665/kakyoshi.67.3_126。
関連項目
[編集]外部リンク
[編集]- オーガニック・シンセゼス オンライン版 - グリニャール反応および関連反応のカテゴリ。
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
















