エンザルタミド
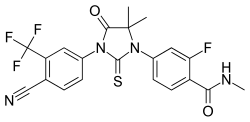 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | イクスタンジ, Xtandi |
| Drugs.com | entry |
| ライセンス | US FDA:リンク |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 識別 | |
| CAS番号 | 915087-33-1 |
| ATCコード | None |
| PubChem | CID: 15951529 |
| ChemSpider | 13093347 |
| UNII | 93T0T9GKNU |
| KEGG | D10218 |
| ChEBI |
CHEBI:68534 |
| 化学的データ | |
| 化学式 | C21H16F4N4O2S |
| 分子量 | 464.44 g/mol |
| |
| |
エンザルタミド(英語: Enzalutamide)は米国Medivation社が創薬したアンドロゲン受容体拮抗薬であり、去勢抵抗性前立腺癌(CRPC)に適応を持つ[1]。商品名イクスタンジ。血清PSAを1ヶ月で最大89%低下させる[2]。また、in vitroでは乳癌細胞の成長阻害も報告されている[3][4]。開発コードMDV3100。
米国では2012年8月にFDAによりCRPCの治療薬として承認された[5][6]。日本ではアステラス製薬が2014年3月に同効能・効果について承認を取得した[7]。欧州では「化学療法施行歴のない成人男性における無症候性または軽度の症候性の転移性去勢抵抗性前立腺癌」について2014年12月に承認された[8]。
前臨床試験
[編集]エンザルタミドはアンドロゲン受容体(AR)に対してビカルタミドより約5倍強く結合する[9]。アンドロゲンの効果発現にはARの細胞核内への移動が必要であるが、ビカルタミドとは逆に、エンザルタミドはARの細胞核への移動を促進しない。加えて、ARとDNA、ならびにARとコアクチベーターの結合を阻害する[9]。
また、AR発現を亢進させたLNCaP細胞(前立腺癌細胞株)にエンザルタミドを添加すると、ビカルタミドとは対照的にPSAとTMPRSS2の濃度が低下し、アンドロゲン依存性の遺伝子発現が抑制されることが確認された[9]。AR発現が亢進したVCaP細胞(前立腺癌細胞株)では、エンザルタミドはアポトーシスを誘導する[9]。(ビカルタミドは誘導しない。)さらにW741C変異ARに対しては、ビカルタミドはアゴニストとして作用するが、エンザルタミドはアンタゴニストとして作用する[9]。
エンザルタミドは in vitro において乳癌のエストロゲン受容体に対してタモキシフェンと同様に作用し、さらにアンドロゲン受容体を阻害することが明らかにされている[10]。
臨床試験
[編集]エンザルタミドは転移のある去勢抵抗性前立腺癌(mCRPC)に対して臨床的に有効である[11]。PSA濃度は50%以上の患者で低下(化学療法未治療患者:65例中40例、化学療法既治療患者:75例中38例)した[11]。読影に拠る病勢進行までの期間は中央値で56週間(化学療法未治療患者)と25週間(化学療法既治療患者)であった[12]。
既治療のmCRPCに対する第III相臨床試験(AFFIRM)の結果、全生存期間の中央値はエンザルタミド群(n=800例)で18.4ヶ月、プラセボ群(n=399例)で13.6ヶ月であった[13][14]。 そのほか、PSA濃度が半分以下に減少した患者の比率はエンザルタミド群54%対プラセボ群2%、PSAに拠る病勢進行までの期間(中央値)はエンザルタミド群8.3ヶ月対プラセボ群3.0ヶ月、読影に拠る病勢進行までの期間(中央値)はエンザルタミド群8.3ヶ月対プラセボ群2.9ヶ月等の結果が得られた。
未治療のmCRPCに対する第III相臨床試験(PREVAIL)の中間解析結果では、全生存期間のハザード比はプラセボ群に対してエンザルタミド群で0.70(95%信頼区間:0.59-0.83)で、生存期間の中央値はエンザルタミド群32.4ヶ月対プラセボ群30.2ヶ月、読影(ならびに死亡イベント)に拠る病勢進行までの期間(中央値)はエンザルタミド群NYR(95%信頼区間:13.8–上限値)対プラセボ群3.9ヶ月(95%信頼区間:3.7-5.4)(ハザード比:0.19)であった[15]。 独立データモニタリング委員会がエンザルタミドのベネフィットを認め、試験が中止された。
副作用
[編集]日本の添付文書に拠れば[16]、
- 国内第I/II相臨床試験での主な副作用は高血圧(14.9%)、便秘(14.9%)、疲労(12.8%)、食欲減退(12.8%)、体重減少(10.6%)および心電図QT延長(10.6%)等であった。
- 海外第III相試験での主な副作用は疲労(21.5%)、悪心(20.1%)、ほてり(15.0%)、食欲減退(12.6%)および無力症(10.0%)等であった。
また重大な副作用として痙攣発作(0.2%)と血小板減少(頻度不明)が記載されている。
出典
[編集]- ^ “Medivation's MDV3100 Shown to Be Effective in a Preclinical Model of Hormone-Refractory Prostate Cancer”. Press release. Medivation, Inc. (2007年2月26日). 2009年5月10日閲覧。
- ^ “Medivation's MDV3100 Demonstrates Substantial PSA Reductions In First Patient Groups Treated In Phase 1-2 Hormone Refractory Prostate Cancer Trial”. Medical News Today (2007年11月6日). 2009年5月10日閲覧。
- ^ “Preclinical Evaluation of Enzalutamide in Breast Cancer Models”. 2014年9月8日閲覧。
- ^ “Medivation and Astellas Announce New Preclinical Study Results Showing MDV3100 Blocks Breast Cancer Cell Growth”. Press Release. MarketWatch (2011年8月4日). 2011年9月25日閲覧。
- ^ “FDA approves new treatment for a type of late stage prostate cancer”. press release. United States Food and Drug Administration (2012年8月31日). 2014年9月8日閲覧。
- ^ Anna Azvolinsky (September 4, 2012). “FDA Approves Enzalutamide (Xtandi) for Late-Stage Prostate Cancer”. CancerNetwork. 2014年9月8日閲覧。
- ^ “前立腺癌治療剤 「イクスタンジカプセル」 製造販売承認取得のお知らせ”. press release. アステラス製薬 (2014年3月24日). 2014年9月8日閲覧。
- ^ “経口アンドロゲン受容体阻害剤XTANDI(エンザルタミド) 化学療法施行歴のない転移性去勢抵抗性前立腺がんの追加適応症 欧州での承認取得のお知らせ” (2014年12月2日). 2014年12月6日閲覧。
- ^ a b c d e Tran C, Ouk S, Clegg NJ, Chen Y, Watson PA, Arora V, Wongvipat J, Smith-Jones PM, Yoo D, Kwon A, Wasielewska T, Welsbie D, Chen CD, Higano CS, Beer TM, Hung DT, Scher HI, Jung ME, Sawyers CL (May 2009). “Development of a second-generation antiandrogen for treatment of advanced prostate cancer”. Science 324 (5928): 787–90. doi:10.1126/science.1168175. PMC 2981508. PMID 19359544.
- ^ “Role of the androgen receptor in breast cancer and preclinical analysis of enzalutamide”. Breast Cancer Res. 16 (1): R7. (January 2014). doi:10.1186/bcr3599. PMC 3978822. PMID 24451109.
- ^ a b Scher HI, Beer TM, Higano CS, Taplin M, Efstathiou E, Anand A, Hung D, Hirmand M, Fleisher M (2009). “Antitumor activity of MDV3100 in a phase I/II study of castration-resistant prostate cancer (CRPC)”. J Clin Oncol 27 (15s): abstr 5011.
- ^ Medivation, Inc. (2011年2月15日). “Medivation and Astellas Announce Positive New, Long-Term Follow-Up Data From Phase 1-2 Trial of MDV3100 in Advanced Prostate Cancer Patients”. Acquire Media. 2011年3月24日閲覧。
- ^ Increased Survival with Enzalutamide in Prostate Cancer after Chemotherapy. New England Journal of Medicine. (2012-09-27) 2014年9月7日閲覧。.
- ^ Fred Saad (2013年8月). “Evidence for the efficacy of enzalutamide in postchemotherapy metastatic castrate-resistant prostate cancer”. 2014年9月7日閲覧。
- ^ “NCT01212991”. ClinicalTrials.gov, United States National Institutes of Health. 2014年9月8日閲覧。 “A Safety and Efficacy Study of Oral MDV3100 in Chemotherapy-Naive Patients With Progressive Metastatic Prostate Cancer (PREVAIL)”
- ^ “イクスタンジカプセル40mg 添付文書” (2015年11月). 2016年6月28日閲覧。
