硫化ナトリウム
| 硫化ナトリウム | |
|---|---|
| |
別称 硫化二ナトリウム | |
| 識別情報 | |
| CAS登録番号 | 1313-82-2 1313-84-4(9水和物) |
| PubChem | 237873 |
| EC番号 | 215-211-5 |
| 国連/北米番号 | 1385(無水物) 1849(水和物) |
| RTECS番号 | WE1905000 |
| 特性 | |
| 化学式 | Na2S |
| モル質量 | 78.0452 g/mol(無水物) 240.18 g/mol(9水和物) |
| 外観 | 無色の潮解性固体 |
| 密度 | 1.856 g/cm3(無水物) 1.58 g/cm3(5水和物) 1.43 g/cm3(9水和物) |
| 融点 |
1176 ℃(無水物) |
| 水への溶解度 | 18.6 g/100 mL (20 ℃) 39 g/100 mL (50 ℃) |
| 溶解度 | エーテルに不溶 アルコールに微溶 |
| 構造 | |
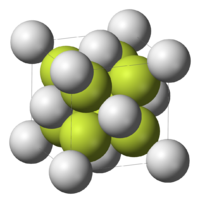
| 結晶構造 | 逆蛍石型(立方晶), cF12 |
| 空間群 | Fm3m, No. 225 |
| 配位構造 | 四面体形 (Na+); 立方晶 (S2–) |
| 危険性 | |
| 安全データシート(外部リンク) | ICSC 1047 |
| EU分類 | 毒性 (T) 腐食性 (C) 環境への危険性 (N) |
| EU Index | 016-009-00-8 |
| NFPA 704 | |
| Rフレーズ | R22, R24, R31, R34, R50 |
| Sフレーズ | (S1/2), S26, S36/37/39, S45, S61 |
| 発火点 | > 480 ℃ |
| 関連する物質 | |
| その他の陰イオン | 酸化ナトリウム セレン化ナトリウム テルル化ナトリウム |
| その他の陽イオン | 硫化リチウム 硫化カリウム |
| 関連物質 | 硫化水素ナトリウム |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
硫化ナトリウム(りゅうかナトリウム、sodium sulfide)は化学式 Na2S で表されるナトリウムの硫化物である。普通は9水和物の形で存在し、これは無色の結晶である。硫化ソーダともいう。
無水物は立方晶系の逆蛍石型構造、格子定数は a = 652.6 pm である。
硫化染料の製造・染色用・ニトロ化合物の還元・脱毛剤に用いられるアルカリ性物質で、非常に強い腐卵臭と腐食性、吸湿性を有する。
製法[編集]
水酸化ナトリウム溶液を硫化水素で飽和した硫化水素ナトリウムの溶液に、同量の水酸化ナトリウムを加え、濃縮することによって9水和物が析出する。
9水和物を硫酸デシケーター中で乾燥した後、水素気流中で加熱すると無水物が得られる。また計算量のナトリウムと硫黄の直接反応でも無水物が得られる。
工業的には無水硫酸ナトリウムで空気を遮断して、反射炉で約 1000 ℃ でコークスで還元させることにより製造される。
特徴[編集]
- 潮解性があり、水やアルコールに可溶。
- 空気中での酸化、あるいは無水物を水に溶解する際には発熱する。
- 空気中の酸素によって酸化するとチオ硫酸ナトリウム・亜硫酸ナトリウムを生じ、炭酸ガスを吸収すると炭酸ナトリウムに変質する。
- 水溶液は硫黄を溶解して黄色のポリ硫化ナトリウムを生成する。
- 廃液中の硫化ナトリウムと酸、酸性塩などが反応して硫化水素を発生した事例があるため、取扱いには留意が必要である。
脚注[編集]






