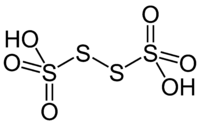
四チオン酸
| 四チオン酸 | |
|---|---|
| |
1,6-dihydrido-2,2,5,5-tetraoxido-1,6-dioxy-2,3,4,5-tetrasulfy-[6]catena | |
別称 2-(dithioperoxy)disulfuric acid | |
| 識別情報 | |
| CAS登録番号 | 13760-29-7 |
| PubChem | 26259 |
| UNII | 8V1L8R19JH |
| KEGG | C02084 |
| ChEBI | |
| ChEMBL | CHEMBL3306828 |
| |
| |
| 特性 | |
| 化学式 | H2O6S4 |
| モル質量 | 226.27 g mol−1 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
| 四チオン酸イオン | |
|---|---|

| |
2,2,5,5-tetraoxido-1,6-dioxy-2,3,4,5-tetrasulfy-[6]catenate(2-) | |
別称 2-(dithioperoxy)disulfate | |
| 識別情報 | |
| CAS登録番号 | 15536-54-6 |
| PubChem | 4657547 |
| ChEBI | |
| 特性 | |
| 化学式 | S4O2− 6 |
| モル質量 | 224.3 g mol−1 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
四チオン酸(しチオンさん)またはテトラチオン酸(Tetrathionic acid)は、4つの硫黄原子が連なるポリチオン酸である[1]。硫黄原子のうち2つは酸化状態0、2つは酸化状態+5である。S2−
2がSO3に結合して生じた付加物と見る事もできる。四チオン酸に由来するオキソアニオンは四チオン酸アニオン (S4O2−
6) である。
生成[編集]
- 2S2O2−
3 + I2 → S4O2−
6 + 2I−
構造[編集]
図はBaS4O6·2H2OとNa2S4O6·2H2OにおけるS4O2−
6の配置を示したものであるが、このように立方体の4つの頂点に硫黄原子が位置した構造をしている。多硫化物では、S-S-S-S の二面角が 90°に近づくのが普通である。
化合物[編集]
四チオン酸アニオンを含む化合物としては、四チオン酸ナトリウム:Na2S4O6、四チオン酸カリウム:K2S4O6、四チオン酸バリウム二水和物:BaS4O6·2H2Oが挙げられる。
性質[編集]
中間の酸化状態にあるチオ硫酸のような硫黄化合物同様、炭素鋼やステンレス鋼の孔食の原因となる事がある。
哺乳類の小腸に存在するチオ硫酸は、炎症反応において免疫系が放出する活性酸素(主にNADPHオキシダーゼが生成するスーパーオキシド)により酸化され四チオン酸に変化する。一方で、この四チオン酸は細菌 Salmonella Enterica serotype Typhimurium において終末電子受容体となる事が分かっている。このため、炎症反応によって細菌の増殖が促進されることがある[2]。
関連項目[編集]
出典[編集]
- ^ グリーンウッド, ノーマン; アーンショウ, アラン (1997). Chemistry of the Elements (英語) (2nd ed.). バターワース=ハイネマン. ISBN 978-0-08-037941-8。
- ^ Winter, Sebastian E. "Gut Inflammation Provides a Respiratory Electron Acceptor for Salmonella." Nature, 23 Sept. 2010. Web. 28 Mar. 2013.


