ブレオマイシン
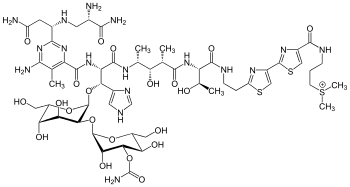 | |
 Bleomycin A2 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Blenoxane |
| Drugs.com | monograph |
| MedlinePlus | a682125 |
| 胎児危険度分類 |
|
| 法的規制 |
|
| 薬物動態データ | |
| 生物学的利用能 | well absorbed |
| 代謝 | ? |
| 半減期 | 2 hours |
| 排泄 | renal (60-70%) |
| データベースID | |
| CAS番号 |
11056-06-7 |
| ATCコード | L01DC01 (WHO) |
| PubChem | CID: 456190 |
| DrugBank |
DB00290 |
| ChemSpider |
401687 |
| UNII |
40S1VHN69B |
| KEGG |
D07535 |
| ChEBI |
CHEBI:22907 |
| ChEMBL |
CHEMBL403664 |
| 化学的データ | |
| 化学式 | C55H84N17O21S3 |
| 分子量 | 1415.551 |
| |
| |
ブレオマイシン(Bleomycin)はがん治療に用いられる薬剤であり[1]、ホジキンリンパ腫、 非ホジキンリンパ腫、 精巣癌、 卵巣癌、子宮頸癌などのがんに使用される。 通常は他のがん薬剤と併用され、静脈内投与のほか、筋肉注射、皮下注射、腹腔内投与、動脈注射により投与される[1][2]。皮膚がんの治療薬として軟膏も製剤化されている[3]。また、がんによる胸水の再発防止のために直接胸部に投与されることもあるが、胸水治療にはタルクの使用が妥当である[4][1]。
一般的な副作用は発熱、体重減少、嘔吐、発疹である。重症なアナフィラキシーが発生することもある。また、肺の炎症を惹き起こす原因となる場合もあり、結果的に肺腺維症となることもある。数週間に一度の胸部X線写真による診察が勧められる。ブレオマイシンの妊娠中の使用は胎児に悪影響を及ぼすことがあり、DNA合成が妨げられると考えられている[1]。
ブレオマイシンは1965年、梅澤濱夫によって発見された[5]。真正細菌の Streptomyces verticillusが産生する[1]。世界保健機関の必須医薬品リストの一つであり、最も効果的で安全な医療制度で必要とされる医薬品である[6]。ジェネリック医薬品として入手でき、開発途上国では1投与$14~$78米ドルで売られている[7]。
効能・効果
[編集]- 注射[2]
- 皮膚癌、頭頸部癌 (上顎癌、舌癌、口唇癌、咽頭癌、喉頭癌、口腔癌など)、肺癌 (特に原発性及び転移性扁平上皮癌)、食道癌、悪性リンパ腫、子宮頸癌、神経膠腫、甲状腺癌、胚細胞腫瘍 (精巣腫瘍、卵巣腫瘍、性腺外腫瘍)
- 軟膏[3]
- 皮膚悪性腫瘍
禁忌
[編集]重篤な肺機能障害や肺線維化病変、重篤な腎機能障害、重篤な心疾患を有する患者などには禁忌である。これは軟膏剤でも変わらない。
また、ブレオマイシン投与中は胸部への放射線照射が禁忌となる。
副作用
[編集]重大な副作用は、
- 間質性肺炎・肺線維症(注射薬:10%、軟膏:0.1%未満)
- ショック(注射薬:0.1%未満)
- 出血(注射薬:2%)
間質性肺炎・肺線維症の出現は警告欄にも記載されている[2][3]。
薬物動態
[編集]血管内への注射では直ちに、また筋肉内投与では投与後1時間で最高血中濃度に達する[8]:15。その後の減少は二相性で、半減期はα相:24分、β相:242分である。
ブレオマイシンは皮膚に多く分布し[8]:19、皮膚、肺、腎、膀胱では活性型であるが、肝、脾などの他の臓器では不活化される[2]。
ブレオマイシンのほとんどは代謝されずに尿に排泄されるが、残りはアミノぺプチダーゼにより加水分解され、不活性型のデアミドブレオマイシンとなる[8]:19。
軟膏を塗布した場合には、健常皮膚からはほとんど吸収されない[3]。
作用機序
[編集]
非ヘム鉄タンパク質の一種であるブレオマイシンは、DNA鎖の切断を誘発することで作用する[9]。 一部の研究では、ブレオマイシンはDNA鎖へのチミジンの取り込みも阻害することが示唆されている。ブレオマイシンによるDNA切断は、少なくともin vitro では酸素と金属イオンに依存している。DNA鎖切断の正確なメカニズムは解明されていないが、ブレオマイシンが金属イオン(主に鉄)をキレートし、酸素と反応してDNAを切断するスーパーオキシドおよびヒドロキシルラジカルを生成する疑似酵素を形成することが示唆されている。また別の仮説では、ブレオマイシンがDNA鎖の特定の部位に結合し、塩基から水素原子を奪うことで切断を誘発し、その結果、塩基がクリーギー転位を起こすか、アルカリに不安定な損傷部位を形成することで鎖が切断されるとされている[10]。さらに、これらの複合体は、脂質の過酸化や他の細胞分子の酸化も触媒する。そのため、ホジキンリンパ腫ではブレオマイシンとドキソルビシンを併用する。これは、ドキソルビシンがDNA鎖間にインターカレーションを起こすとともに、トポイソメラーゼII酵素に作用してトポイソメラーゼ複合体を解体することで、DNAに対して相加的・相補的な作用を及ぼすためである。
化学的特徴
[編集]ブレオマイシンは混合物であり、側鎖の異なるA1~A6、B1~B6、デメチルA2、A2′-a、A2′-b、B1′ の16種類から成る[8]:2-3。主な成分はA2とB2であり、A2:55~70%、B2:25~32%を含有する。
| 異性体 | 側鎖 |
|---|---|
| A2 | -NH-C3H6-S+(CH3)2 |
| B2 | -NH-C4H8-NH-C(=NH)NH2 |
出典
[編集]- ^ a b c d e “Bleomycin Sulfate”. The American Society of Health-System Pharmacists. Aug 1, 2015閲覧。
- ^ a b c d e “ブレオ注射用5mg/ブレオ注射用15mg 添付文書”. www.info.pmda.go.jp. PMDA. 2021年5月11日閲覧。
- ^ a b c d e “ブレオS軟膏5mg/g 添付文書”. www.info.pmda.go.jp. PMDA. 2021年5月11日閲覧。
- ^ Shaw, P (2004). “Pleurodesis for malignant pleural effusions.”. The Cochrane database of systematic reviews (1): CD002916. doi:10.1002/14651858.CD002916.pub2. PMID 14973997.
- ^ Sneader, Walter (2005). Drug discovery : a history (Rev. and updated ed.). Chichester: Wiley. p. 312. ISBN 9780471899792
- ^ “WHO Model List of Essential Medicines (19th List)”. World Health Organization (April 2015). 8 December 2016閲覧。
- ^ “Bleomycin”. 26 August 2015閲覧。[リンク切れ]
- ^ a b c d “ブレオ注射用5mg/ブレオ注射用15mg インタビューフォーム”. PMDA. 2021年5月12日閲覧。
- ^ Takimoto CH, Calvo E. "Principles of Oncologic Pharmacotherapy" Archived 2009-05-15 at the Wayback Machine. in Pazdur R, Wagman LD, Camphausen KA, Hoskins WJ (Eds) Cancer Management: A Multidisciplinary Approach Archived 2013-10-04 at the Wayback Machine.. 11 ed. 2008.
- ^ Hecht, SM (2000). “Bleomycin: new perspectives on the mechanism of action”. J. Nat. Prod. 63 (1): 158–168. doi:10.1021/np990549f. PMID 10650103.
