ファーマコフォア

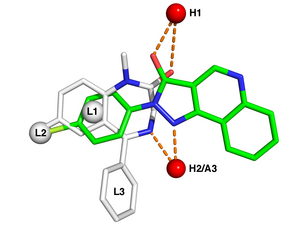
ファーマコフォア(英: pharmacophore)は、生体高分子によるリガンドの分子認識に必要な分子の特徴(官能基群とそれらの相対的な立体配置)の(抽象的な)概念である[2]。IUPACにおけるファーマコフォアの定義は「特定の生物学的標的との最適な超分子相互作用を確実にし、生物学的反応を引き起こす(もしくは遮断する)ために必要な、立体的、電子的特徴の集合体」とされている[3]。ファーマコフォアモデルは、構造的に多様なリガンドがどのようにして共通の受容体部位に結合するかを説明する。さらに、ファーマコフォアモデルを使用して、同じ受容体に結合する新規リガンドを、デ・ノボデザインやバーチャルスクリーニングで同定でき、創薬を支援する[4]。
要素[編集]
典型的なファーマコフォア要素には、疎水性重心、芳香環、水素結合アクセプターあるいはドナー、カチオン、アニオンがある。これらのファーマコフォア点はリガンドそれ自身上に位置してもよいし、受容体中に位置すると推定される投影点でもよい。
新規なリガンドを同定するためには、これらの要素を同様の性質を持つ異なる官能基群と合わせる必要がある。リガンド-受容体相互作用は通常「極性陽性」、「極性陰性」、「疎水性」である。詳細なファーマコフォアモデルには疎水性体積や水素結合ベクトルなども含まれる。
モデル開発[編集]
ファーマコフォアモデルを開発するためのプロセスには、通常、次のステップが含まれる。
- リガンドのトレーニングセットを選択する - ファーマコフォアモデルの開発に使用される構造的に多様な分子の集合体を選択する。ファーマコフォアモデルは、生理活性を持つ分子と持たない分子を区別できるようにする必要があるため、分子セットには活性化合物と不活性化合物の両方を含める必要がある。
- コンホメーション解析 - 選択した各分子のそれぞれについて、生物活性配座を含む可能性の高い、低エネルギー配座の集合体を生成する。
- 分子の重ね合わせ - 分子の低エネルギー配座のすべての組み合わせを重ね合わせる (「適合」させる)。集合体内のすべての分子に共通の類似した (生物学的等価性の) 官能基が適合している可能性がある (例えば、フェニル環やカルボン酸基)。最適な適合となる配座の集合体 (各活性分子から1つの配座) は、活性配座であると推定される。
- 抽象化 - 重ね合わせた分子を抽象的な表現に変換する。たとえば、重畳されたフェニル環は、より概念的には「芳香環」ファーマコフォア要素と呼ばれる。同様にヒドロキシ基は「水素結合供与体/受容体」ファーマコフォア要素として指定することができる。
- 検証 - ファーマコフォアモデルは、共通の生物学的標的に結合する一連の分子の観察された生物学的活性を説明する「仮説」である。このモデルは、一連の分子の生物学的活性の違いを説明できる場合にのみ有効である。
新しい分子の生物学的活性が利用できるようになると、ファーマコフォアモデルを更新してさらに洗練させることができる。
応用[編集]
現代の計算化学では、ファーマコフォアの概念を用いて、同様の生物学的活性を持つ複数の分子から本質的な特徴を決定できる。次に、化合物データベースを検索して、同じ特徴を共有し、同じ相対配向に配置された分子を探すことができる。
ファーマコフォアは、3D-QSARモデルを開発するための出発点としても利用される。このようなツールと「特権構造」と呼ばれる関連概念は「巧みな構造変更によって、複数の種類の受容体や酵素標的に対して有用なリガンドを提供できる分子フレームワーク」と定義される[5]。
歴史[編集]
歴史的に、ファーマコフォアの概念はレモント・キール (英語版) によって確立された。キールは1967年にこの概念に初めて言及し[6]、1971年の論文でこの用語を使用した[7]。
この概念の作成は、しばしば誤ってパウル・エールリヒに帰される。しかしながら、そう主張されている文献[8]やエールリヒのいかなる著作においても、「ファーマコフォア」という用語に言及したものやこの概念を使ったものはない[9]。
1977年に、ピーター・グンドは「分子において受容体に認識され生物学的活性の原因となる一まとまりの構造的特徴」とファーマコフォアを定義した[10]。
脚注[編集]
- ^ Madsen U, Bräuner-Osborne H, Greenwood JR, Johansen TN, Krogsgaard-Larsen P, Liljefors T, Nielsen M, Frølund B (2005). “GABA and Glutamate receptor ligands and their therapeutic potential in CNS disorders”. In Gad SC. Drug Discovery Handbook. Hoboken, N.J: Wiley-Interscience/J. Wiley. pp. 797–907. ISBN 0-471-21384-5
- ^ 日本薬学会 (2014年1月). “ファーマコフォア”. 薬学用語解説. 2015年3月17日閲覧。
- ^ Wermuth CG, Ganellin CR, Lindberg P, Mitscher LA (1998). “Glossary of terms used in medicinal chemistry (IUPAC Recommendations 1998)”. Pure and Applied Chemistry 70 (5): 1129–1143. doi:10.1351/pac199870051129.
- ^ Jangampalli Adi, Pradeepkiran (February 2019). “Pharmacophore-based models for therapeutic drugs against phosphorylated tau in Alzheimer's disease”. Drug Discovery Today 24 (2): 616–623. doi:10.1016/j.drudis.2018.11.005. PMC 6397090. PMID 30453058.
- ^ Duarte, CD (2007), “Privileged structures: a useful concept for the rational design of new lead drug candidates”, Mini Rev Med Chem 7 (11): 1108–1119, doi:10.2174/138955707782331722, PMID 18045214.
- ^ Kier LB (September 1967). “Molecular orbital calculation of preferred conformations of acetylcholine, muscarine, and muscarone”. Mol. Pharmacol. 3 (5): 487–94. PMID 6052710.
- ^ Kier LB (1971). Molecular orbital theory in drug research. Boston: Academic Press. pp. 164–169. ISBN 0-12-406550-3
- ^ Ehrlich P (1909). “Über den jetzigen Stand der Chemotherapie”. Ber. Dtsch. Chem. Ges. 42: 17–47. doi:10.1002/cber.19090420105.
- ^ J.H. van Drie (2007). “Monty Kier and the Origin of the Pharmacophore Concept”. Internet Electronic Journal of Molecular Design 6: 271–279.
- ^ Gund, P. (1977). Prog. Mol. Subcell. Biol. 5: 117-143.
参考文献[編集]
- Osman F. Güner (2000) Pharmacophore Perception, Development, and use in Drug Design ISBN 0-9636817-6-1 Table of contents and preface
- Thierry Langer and Rémy D. Hoffmann (2006) Pharmacophores and Pharmacophore Searches ISBN 3-527-31250-1
関連項目[編集]
- ケモインフォマティクス
- 分子マイニング
- 製薬
- 定量的構造活性相関 (QSAR)
- in silico
外部リンク[編集]
以下のソフトウェアパッケージによって様々な計算化学的手法を用いたファーマコフォアモデルの作成が可能である。
