メタンスルホン酸エチル
| メタンスルホン酸エチル | |
|---|---|

| |
| |
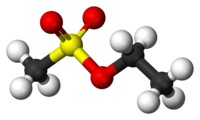
Ethyl methanesulfonate | |
別称 Ethyl mesylate Ethyl methanesulphonate | |
| 識別情報 | |
| CAS登録番号 | 62-50-0 |
| PubChem | 6113 |
| ChemSpider | 5887 |
| |
| 特性 | |
| 化学式 | CH3SO3C2H5 |
| モル質量 | 124.16 g/mol |
| 外観 | 無色液体 |
| 密度 | 1.1452 g/cm3 (22 °C) |
| 沸点 |
85 - 86 °C /10 mmHg |
| 危険性 | |
| NFPA 704 | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
メタンスルホン酸エチル (メタンスルホンさんエチル、Ethyl methanesulfonate = EMS) は、変異原性、催奇性、発癌性を持ち、化学式 C3H8SO3 で表される有機化合物である。特にグアニン アルキル化によって誘発されるG:CからA:T への遷移 (遺伝学)を介して遺伝物質にランダムな突然変異を生成する[1]。EMSは通常、点突然変異のみを生成する。その効力とよく理解されている突然変異スペクトルのために、EMSは実験遺伝学で最も一般的に使用される化学的突然変異誘発物質である[2]。EMS曝露によって誘発された突然変異は、遺伝学的スクリーニングまたは他のアッセイで研究することができる。
生物学研究での使用[編集]
EMSは、実質的な死滅なしに、遺伝子あたり5x10-4から5x10-2の割合で突然変異を誘発することができる。モデル生物 C. elegans (カエノラブディティス・エレガンス) の典型的なEMS突然変異誘発実験で観察された遺伝子あたり5x10-4の突然変異率は、G/C塩基対あたり約7x10-6の突然変異、または最初に突然変異した配偶子内の約250の突然変異の生の突然変異率に対応する(〜100 Mbp, 36%一倍体ゲノムを含む)[3]。そのような突然変異誘発された配偶子は、遺伝子に約9つの異なるloss-of-function (機能喪失型)突然変異を持ち、これらの突然変異の1から2は必須遺伝子内にあり、したがって致命的である。ただし、同じ必須遺伝子が独立した配偶子で変異している可能性は低く、必須遺伝子の喪失によって配偶子自体が死滅しなかった場合、下流の配偶子融合により、結果として生じる接合子と生物の生存が可能になることがよくある。機能しない変異対立遺伝子は、他の配偶子によって提供される野生型遺伝子によって救出される可能性がある[3]。
突然変異誘発のメカニズム[編集]
EMSのエチル基はDNAのグアニンと反応し、異常な塩基 O6-エチルグアニンを形成する。このプロセスを触媒するDNAポリメラーゼは、シトシンの代わりに O'6-エチルグアニンの反対側にチミンをしばしば配置する。後続の複製ラウンドに続いて、元のG:C 塩基対はA:Tペア (遷移 (遺伝学)突然変異) になる可能性がある。これは遺伝情報を変化させ、しばしば細胞に有害であり、病気を引き起こす可能性がある。RNAポリメラーゼは、ウリジン (チミンのRNA類似体) を O6-エチルグアニン病変の反対側に配置することもできる[4]。
変異原性病変の修復[編集]
O6-エチルグアニンは、O6-メチルグアニン-DNAメチルトランスフェラーゼ修復タンパク質の活性部位のシステインとin vivoで化学量論的に反応することにより修復できる[5]。O6-エチルグアニンの in vivo半減期は、マウスの脳では約9日であるのに対し、マウスの肝臓では約1日であると報告されている[6]。
安定性[編集]
一般的に、EMSは水中で不安定であり、エタノールとメタンスルホン酸に加水分解されるが、室温で中性から酸性のpHでは、1日以上のかなり長い半減期を持つ[7][8]。したがって、EMSは廃棄する前に特に劣化させる必要がある。その手順は、等量の0.1M NaOH および20%w/v チオ硫酸ナトリウム "不活性化溶液" で、少なくとも半減期の6倍 (24時間以上)でEMSを分解する必要がある[8]。
脚注[編集]
- ^ Sega, Gary A. (1984). “A review of the genetic effects of ethyl methanesulfonate”. Mutation Research/Reviews in Genetic Toxicology (Elsevier BV) 134 (2–3): 113–142. doi:10.1016/0165-1110(84)90007-1. ISSN 0165-1110. PMID 6390190.
- ^ Kutscher, Lena M.; Shaham, Shai (2014). “Forward and reverse mutagenesis in C. elegans”. Wormbook : The Online Review of C. Elegans Biology (WormBook): 1–26. doi:10.1895/wormbook.1.167.1. PMC 4078664. PMID 24449699 2021年6月18日閲覧。.
- ^ a b Anderson, Philip (1995). “Chapter 2 Mutagenesis”. Caenorhabditis elegans: Modern Biological Analysis of an Organism. Methods in Cell Biology. 48. Elsevier. pp. 31–58. doi:10.1016/s0091-679x(08)61382-5. ISBN 978-0-12-564149-4. ISSN 0091-679X
- ^ Gerchman, Lois L.; Ludlum, David B. (1973). “The properties of in templates for RNA polymerase”. Biochimica et Biophysica Acta (BBA) - Nucleic Acids and Protein Synthesis (Elsevier BV) 308 (2): 310–316. doi:10.1016/0005-2787(73)90160-3. ISSN 0005-2787. PMID 4706005.
- ^ Pegg, Anthony E (2000). “Repair of O6-alkylguanine by alkyltransferases”. Mutation Research/Reviews in Mutation Research (Elsevier BV) 462 (2–3): 83–100. doi:10.1016/s1383-5742(00)00017-x. ISSN 1383-5742. PMID 10767620.
- ^ Goth, R.; Rajewsky, M. F. (1974-03-01). “Persistence of O6-Ethylguanine in Rat-Brain DNA: Correlation with Nervous System-Specific Carcinogenesis by Ethylnitrosourea”. Proceedings of the National Academy of Sciences 71 (3): 639–643. Bibcode: 1974PNAS...71..639G. doi:10.1073/pnas.71.3.639. ISSN 0027-8424. PMC 388067. PMID 4522778.
- ^ FROESE-GERTZEN, EDITH E.; KONZAK, C. F.; FOSTER, R.; NILAN, R. A. (1963). “Correlation between Some Chemical and Biological Reactions of Ethyl Methanesulphonate”. Nature (Springer Science and Business Media LLC) 198 (4879): 447–448. Bibcode: 1963Natur.198..447F. doi:10.1038/198447a0. ISSN 0028-0836.
- ^ a b Kodym, Andrea; Afza, Rownak (2003). “Chapter 12 Physical and Chemical Mutagenesis”. Plant functional genomics. Totowa, N.J: Humana Press. p. 189-203. ISBN 978-1-58829-145-5. OCLC 51445955

