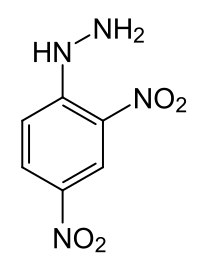
2,4-ジニトロフェニルヒドラジン
| 2,4-ジニトロフェニルヒドラジン | |
|---|---|
| |

| |
(2,4-dinitropheny)lhydrazine | |
| 識別情報 | |
| CAS登録番号 | 119-26-6 |
| PubChem | 3772977 |
| |
| 特性 | |
| 化学式 | C6H6N4O4 |
| モル質量 | 198.14 g mol−1 |
| 外観 | 赤またはオレンジ色の粉末 |
| 融点 |
198 - 202 °C (分解) |
| 危険性 | |
| 安全データシート(外部リンク) | MSDS |
| 主な危険性 | 可燃性、発がんの可能性 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
2,4-ジニトロフェニルヒドラジン (2,4-Dinitrophenylhydrazine = DNPH) は化学式 C6H3(NO2)2NHNH2 で表される化合物である。赤からオレンジ色の固体で、ヒドラジンの置換体である。この固体は衝撃と摩擦に対して比較的鋭敏である。そのため、湿った粉末として取り扱う。医薬品のSivifene の前駆体である。
合成[編集]
2,4-ジニトロフェニルヒドラジンは、硫酸ヒドラジンと2,4-ジニトロクロロベンゼンの反応によって合成される[1]。
DNP テスト[編集]
DNPH は学生実験室で有機定性分析に用いられる試薬である。ブラディ試薬 (Brady's reagent) または ボーチ試薬 (Borch's reagent) は濃硫酸を含むメタノールに2,4-ジニトロフェニルヒドラジンを溶かした溶液である。この溶液はケトンとアルデヒドの検出に用いられる。黄色、オレンジ色または赤色の沈殿が生じればテストが陽性である。芳香族カルボニル化合物では沈殿は赤色、脂肪族なら黄色である[2]。2,4-ジニトロフェニルヒドラジンと一般的なケトンの反応で、以下に示すようなジニトロフェニルヒドラゾンが生成される。
- RR'C=O + C6H3(NO2)2NHNH2 → C6H3(NO2)2NHN=CRR' + H2O
この反応は、全体として、2つの分子が結合して水分が失われる縮合反応である。機構的には、これは付加脱離反応の例である。C=O カルボニル基への -NH2基の求核付加と、それに続く H2O分子の脱離である[3] 。

DNP由来のヒドラゾンは特徴的な融点を持っており、カルボニル化合物の同定を容易にする。 特に、2,4-ジニトロフェニルヒドラジンの使用は Bradyと Elsmie によって開発された[5]。現代の分光分析法がこれらの技術に取って代わった。
2,4-ジニトロフェニルヒドラジンは、カルボン酸、アミド、エステルなどの他のカルボニルを含む官能基とは反応しない。これは孤立電子対がカルボニル炭素のp軌道と相互作用して非局在化が増加するため、共鳴により安定化するためである。この安定性は、カルボニル基に試薬を添加すると失われる。 したがって、これらの化合物は付加反応に対してより耐性がある。 また、カルボン酸の場合、塩基として作用する化合物の効果があり、結果として生じるカルボン酸塩は負に帯電したままになるため、求核攻撃に対して脆弱ではなくなる。
悪臭物質の分析[編集]
悪臭防止法で特定悪臭物質として定められている化合物のうち、アセトアルデヒド、プロピオンアルデヒド、ノルマルブチルアルデヒド、イソブチルアルデヒド、ノルマルバレルアルデヒド、イソバレルアルデヒドは、2,4-ジニトロフェニルヒドラジンをコーティングしたシリカゲルを詰めた補集管に被検空気を通じてヒドラゾンとして捕集し、ガスクロマトグラフで分析する方法が規定されている[6]。
安全性[編集]
DNPH の使用で爆発が生じた[7]。
関連項目[編集]
脚注[編集]
- ^ Allen, C. F. H. (1933). "2,4-Dinitrophenylhydrazine". Organic Syntheses (英語). 13: 36. doi:10.15227/orgsyn.013.0036。
- ^ http://wiki.colby.edu/download/attachments/110920618/Experiment+%232.pdf?version=1&modificationDate=1265312071267
- ^ Adapted from Chemistry in Context, 4th Edition, 2000, Graham Hill and John Holman
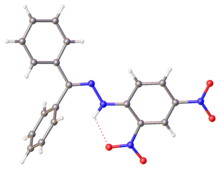
- ^ Tameem, Abdassalam Abdelhafiz; Salhin, Abdussalam; Saad, Bahruddin; Rahman, Ismail Ab.; Saleh, Muhammad Idiris; Ng, Shea-Lin; Fun, Hoong-Kun (2006). “Benzophenone 2,4-dinitrophenylhydrazone”. Acta Crystallographica Section E 62 (12): o5686–o5688. doi:10.1107/S1600536806048112.
- ^ Brady, Oscar L.; Elsmie, Gladys V. (1926). “The use of 2:4-dinitrophenylhydrazine as a reagent for aldehydes and ketones”. Analyst 51 (599): 77–78. Bibcode: 1926Ana....51...77B. doi:10.1039/AN9265100077.
- ^ 昭和47年環境庁告示第9号別表第4の第1
- ^ “Bomb disposal squads detonate chemical stocks in British schools”. The Guardian. (2016年11月2日) 2018年3月19日閲覧。