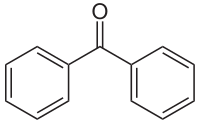
ベンゾフェノン
| ベンゾフェノン | |
|---|---|
| |

|

|

|

|
ジフェニルメタノン | |
別称 ジフェニルケトン | |
| 識別情報 | |
| CAS登録番号 | 119-61-9 |
| PubChem | 3102 |
| ChemSpider | 2991 |
| UNII | 701M4TTV9O |
| KEGG | C06354 |
| ChEMBL | CHEMBL90039 |
| |
| |
| 特性 | |
| 化学式 | C13H10O |
| モル質量 | 182.217 |
| 示性式 | (C6H5)2CO |
| 外観 | 白色固体 |
| 密度 | 1.11 g/cm3、固体 |
| 融点 |
47.9 ℃ |
| 沸点 |
305.4 ℃ |
| 水への溶解度 | 不溶 |
| 危険性 | |
| 安全データシート(外部リンク) | MSDS |
| NFPA 704 | |
| Rフレーズ | R36/37/38 R50/53 |
| Sフレーズ | S26 S29 S37/39 S61 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ベンゾフェノン(benzophenone)は、有機化合物であり、代表的な芳香族ケトンの1つである。紫外線を吸収する性質がある。
用途[編集]
脱水溶媒の調製[編集]
実験室レベルでの有機合成において、金属ナトリウムとベンゾフェノンを用いた蒸留により、溶媒の脱水と脱酸素を行う(脱水と還元自体は金属ナトリウムによって行われる)。ベンゾフェノンの1電子還元によって生じたベンゾフェノン–ケチルは青色であるが、水分や酸素と速やかに反応し消色する。このため脱水と脱酸素が完了したときのみ溶液が青く保たれ、目視で脱水の完了が分かる。THFやジエチルエーテルなどのエーテル系溶媒に対して汎用される方法である。
光アフィニティプローブ[編集]
またケミカルバイオロジーの分野では、光アフィニティープローブに用いられる。低分子化合物にベンゾフェノンを結合させ、タンパク質などの生体分子内で紫外線を照射すると、低分子と相互作用するタンパク質に対してベンゾフェノン部位が共有結合を形成し標識化する。これを何らかの手段により検出することで、低分子と相互作用しているタンパク質を決定することができる。
紫外線吸収剤[編集]
工業的には、紫外線を吸収し光増感作用を示すことを利用して光重合開始剤にも用いられる。紫外線吸収剤としてプラスチックパッケージにベンゾフェノンを利用できる。黒色、不透明なパッケージでは不都合な場合に有用である。また、樹脂モノマーとの混和性や反応速度を向上させることを目的として種々のベンゾフェノン誘導体が開発され、市販されている。
日焼け止め[編集]
ベンゾフェノン誘導体であるオキシベンゾン類は、日焼け止めの成分として用いられている。
合成[編集]
2分子のベンゼンと四塩化炭素からルイス酸触媒下で合成されるジクロロジフェニルメタンの加水分解によって合成できる[1]。また同じくルイス酸存在下で、塩化ベンゾイルとベンゼンによるフリーデル・クラフツ反応によっても合成可能である[2]。
光反応[編集]
ベンゾフェノンのイソプロピルアルコール溶液に微量の酸を加えて紫外光を照射すると、一重項励起状態から三重項状態への項間交差が起こり、ラジカル反応を経て最終的にはベンゾピナコールが得られる[3]。
その他の反応[編集]
ベンゾフェノンを還元すると、フルオレンが生成することが知られている[4]。
関連項目[編集]
出典[編集]
- ^ Marvel, C. S.; Sperry, W. M. "Benzophenone" Org. Synth. 1941, Coll. vol. 1, 95.
- ^ Hardo Siegel, Manfred Eggersdorfer "Ketones" in Ullmann's Encyclopedia of Industrial Chemistry Wiley-VCH, 2002 by Wiley-VCH, Wienheim. DOI: 10.1002/14356007.a15_077
- ^ Bachmann, W. E. "benzopinacol" Org. Synth. 1943, Coll. vol. 2, 71.
- ^ 化学大辞典編集委員会『化学大辞典 (縮刷版) 8』 p.31 (右下) 共立出版 1964年2月15日発行 ISBN 4-320-04022-8

