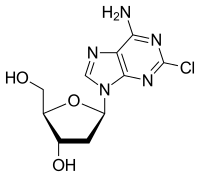
クラドリビン
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Leustatin, Mavenclad, others[1] |
| Drugs.com | monograph |
| MedlinePlus | a693015 |
| ライセンス | EMA:リンク、US Daily Med:リンク |
| 胎児危険度分類 | |
| 法的規制 | |
| 投与経路 | Intravenous, subcutaneous (liquid), by mouth (tablet) |
| 薬物動態データ | |
| 生物学的利用能 | 100% (i.v.); 37 to 51% (orally)[2] |
| 血漿タンパク結合 | 25% (range 5-50%)[3] |
| 代謝 | Mostly via intracellular kinases; 15-18% is excreted unchanged[3] |
| 半減期 | Terminal elimination half-life: Approximately 10 hours after both intravenous infusion and subcutaneous bolus injection[3] |
| 排泄 | Urinary[3] |
| 識別 | |
| CAS番号 |
4291-63-8 |
| ATCコード |
L01BB04 (WHO) (parenteral) L04AA40 (WHO) (oral for MS) |
| PubChem | CID: 20279 |
| IUPHAR/BPS | 4799 |
| DrugBank |
DB00242 |
| ChemSpider |
19105 |
| UNII |
47M74X9YT5 |
| KEGG |
D01370 |
| ChEBI |
CHEBI:567361 |
| ChEMBL |
CHEMBL1619 |
| 化学的データ | |
| 化学式 | C10H12ClN5O3 |
| 分子量 | 285.69 g·mol−1 |
| |
クラドリビン(Cladribine)は、有毛細胞白血病(HCL、白血病性網状内皮症)、B細胞性慢性リンパ性白血病、再発寛解型多発性硬化症(RRMS)の治療に用いられる医薬品である[4][5]。白血病治療には点滴静注剤が、多発性硬化症には経口剤が用いられる。日本では経口剤は承認されていない。
化学名は2-クロロ-2'-デオキシアデノシン(2CdA)で、プリン類縁物質である。リンパ球を標的とし、免疫系を選択的に抑制する合成化学療法剤に分類される。化学的にはヌクレオシドであるアデノシンを模倣している。しかしアデノシンとは異なり、アデノシンデアミナーゼで分解されにくいため、細胞内に蓄積され、細胞がDNAを処理する能力を阻害する。クラドリビンはトランスポーターを介して細胞に取り込まれる。細胞内に取り込まれたクラドリビンは主にリンパ球で活性化され、デオキシアデノシンキナーゼ(dCK)によって三リン酸化される。さまざまなホスファターゼがクラドリビンを脱リン酸化する。活性化された三リン酸化クラドリビンは、ミトコンドリアや核のDNAに取り込まれ、アポトーシスを誘発する。活性化されていないクラドリビンは、他のすべての細胞から速やかに除去される。すなわち、非標的細胞が細胞死する可能性は非常に小さい[4][6]。
効能・効果[編集]
日本[編集]
- ヘアリーセル白血病
- 再発・再燃または治療抵抗性の下記疾患
- 悪性度または濾胞性B細胞性非ホジキンリンパ腫
- マントル細胞リンパ腫
2002年1月に「ヘアリーセル白血病」治療薬として輸入承認を取得した[7]。
2002年12月に「再発・再燃または治療抵抗性の低悪性度またはろ胞性B細胞性非ホジキンリンパ腫、マントル細胞リンパ腫」への適応を取得した[8]。
米国[編集]
- 臨床的に有意な貧血、好中球減少、血小板減少、または疾患関連の症状で定義される活動性有毛細胞白血病の治療[9]
- 【経口剤】成人の再発性多発性硬化症(再発寛解型および活動性二次進行型を含む)の治療[10]
再発寛解型多発性硬化症(RRMS)ならびに二次性進行型多発性硬化症(SPMS)の治療薬としての販売承認を取得したのは2019年3月である[11]。
英国[編集]
- 有毛細胞白血病(HCL)患者の一次治療または二次治療
- B細胞性慢性リンパ性白血病(CLL)で、少なくとも1種類のアルキル化剤を含む標準的な治療法に反応しなかった、または治療中もしくは治療後に疾患が進行した患者の治療
1995年2月に承認された[5]。
その他[編集]
2017年より、欧州、UAE、アルゼンチン、チリ、カナダ、オーストラリアにおいて、RRMSの治療薬として経口剤(10mg錠)が承認されている。
一部の研究者は、HCL患者の治療目的に非経口製剤を経口的に使用している。経口では生物学的に利用可能であるクラドリビンは約40%である旨に留意することが重要である。クラドリビンは、エルドハイム・チェスター病[12]やランゲルハンス細胞組織球症[13]などのさまざまな組織球症の治療に、他の細胞障害性薬剤との併用で使用される。
副作用[編集]
点滴静注剤[編集]
重大な副作用とされているものは
- 骨髄抑制〔汎血球減少、リンパ球減少(87.0%)、好中球減少(79.8%)、白血球減少(77.9%)、血小板減少(53.8%)、貧血[赤血球減少(48.1%)、ヘマトクリット値減少(45.7%)、ヘモグロビン減少(45.2%)]〕
- 重症日和見感染(敗血症、肺炎など)
- 進行性多巣性白質脳症(PML)
- 消化管出血(1.0%)
- 重篤な神経毒性(不全対麻痺、四肢不全麻痺、ギラン・バレー症候群、ブラウン・セカール症候群など)
- 腫瘍崩壊症候群
- 間質性肺炎(1.0%)
- 重篤な皮膚障害(皮膚粘膜眼症候群、中毒性表皮壊死症など)
- 急性腎障害
である[14](%未記載は頻度不明)。
その他、10%以上の患者に発疹、頭痛、悪心、AST(GOT)上昇、ALT(GPT)上昇、CD4陽性リンパ球減少、好酸球増多、IgA減少、IgG減少、IgM減少、蛋白尿、体重減少、発熱、総蛋白減少、各種感染症が発生する。
経口剤[編集]
重篤(正常値の50%以下)リンパ球減少症(6%)。
その他の一般的な副作用としては、頭痛(75%)、喉の痛み(56%)、感冒様疾患(42%)、吐き気(39%)などが挙げられる[15]。
作用機序[編集]
プリン類似体として、リンパ球などの急速に増殖する細胞に取り込まれ、DNA合成に組み込まれる。アデノシンとは異なりクラドリビンは2位に塩素分子を持っているため、アデノシンデアミナーゼ(ADA)による分解に部分的に抵抗性がある。細胞内ではデオキシシチジンキナーゼ(DCK)によってリン酸化され、毒性のあるデオキシアデノシン三リン酸となる。その後、この分子はDNA合成経路に組み込まれ、鎖の切断を引き起こす。その後、転写因子p53が活性化され、ミトコンドリアからシトクロムcが放出され、最終的にはプログラムされた細胞死(アポトーシス)が起こることになる[16]。このプロセスは約2ヵ月間に亘って行われ、治療後4 - 8週目に細胞減少のピークを迎える[17]。
リンパ球プールの中で、クラドリビンはT細胞よりもB細胞を標的とする。有毛細胞白血病とB細胞性慢性リンパ性白血病は、いずれもB細胞性の血液がんである。MSにおいて、クラドリビンの効果は、B細胞、特にメモリーB細胞[18]を効果的に枯渇させる能力によるものと考えられる。MSにおける経口クラドリビンの主要な第3相臨床試験であるCLARITYにおいて、クラドリビンは末梢のB細胞の80%を選択的に枯渇させたのに対し、T細胞は全体の40〜50%しか枯渇しなかった[19]。更に最近では、クラドリビンは特定のB細胞、特にメモリーB細胞を長期的かつ選択的に抑制することが示されている[20]。
別の酵素群である5´ヌクレオチダーゼ(5NCT)群もまた、クラドリビンを脱リン酸化して不活性化する能力がある。このグループの中で最も重要なサブタイプは5NCT1Aであると思われる。5NCT1Aは細胞質で活性を持ち、プリン類縁体に特異的である。DCK遺伝子の発現を5NCT1Aとの比率で表すと、最も高い比率の細胞はB細胞、特に胚中心とナイーブB細胞である[20]。このことは、どのB細胞がクラドリビンによるアポトーシスに対してより脆弱であるかを説明している。
クラドリビンはB細胞に選択的に作用するが、MSにおけるクラドリビンの効果に寄与していると思われるメモリーB細胞の長期的な抑制は、遺伝子やタンパク質の発現では説明できない。むしろ、クラドリビンはB細胞群全体を枯渇させるように見える。しかし、ナイーブB細胞はリンパ系臓器から速やかに移動するが、メモリーB細胞プールは骨髄から非常にゆっくりと再増殖する。
多発性硬化症(MS)[編集]
有効性[編集]
クラドリビンは、再発性寛解型MSに対して有効な治療法であり、年間の再発率を54.5%減少させた[15]。この効果は、初回投与から4年後まで、その後の投与がなくても持続する可能性がある[21]。このように、クラドリビンはMSの免疫再構築療法として非常に有効であると考えられる。クラドリビンは、アレムツズマブと同様に、約1年の間隔をおいて2つのコースに分けて投与される。各コースは、体重に応じた用量を最初の月に5日間かけて投与し、翌月にさらに4 - 5錠を2回目に投与する[22]。この間および最終投与後、患者の副作用や再発の兆候を観察する。
安全性[編集]
アレムツズマブと比較して、クラドリビンは重度のリンパ球減少の割合が低いとされている。また、一般的な有害事象、特に軽度から中等度の感染症の発生率も低いと思われる[15][21]。 クラドリビンは遺伝子組み換え生物学的製剤ではないため、薬剤に対する抗体の発生とは無縁であり、将来の投与で有効性が低下することはないと思われる。また、アレムツズマブとは異なり、クラドリビンは二次的な自己免疫とは無縁である[23]。
これは、クラドリビンがより選択的にB細胞を標的としていることによると思われる。アレムツズマブとは異なり、クラドリビンは末梢血B細胞プールの急速な再増殖を伴わず、元の数を最大30%オーバーシュートさせる[24]。むしろB細胞の再増殖は緩やかで、1年後にはほぼ正常な総B細胞数に達する。この現象と、他の自己免疫反応に対するシステムの調整に重要な役割を果たすと思われるT細胞が比較的少ないことが、二次的な自己免疫の欠如の説明になると考えられている。
臨床応用[編集]
MSにおいてクラドリビンを開始するかどうかは、疾患活動性の程度(過去1年間の再発回数およびMRIのT1ガドリニウム強調病変で測定)、過去の疾患修飾療法の失敗、潜在的なリスクとベネフィット、および患者の選択によって決定される。
英国では、英国国立医療技術評価機構(NICE)が、成人の高活動性RRMSの治療にクラドリビンを推奨している。「急速に進行する重症の再発性多発性硬化症(過去1年間に少なくとも2回の再発があり、ベースラインのMRIで少なくとも1つのT1ガドリニウム増強病変がある)」、または「疾患修飾療法による治療効果が不十分な再発性多発性硬化症(過去1年間に1回の再発があり、MRIで疾患活動性の証拠があるもの)」[25]。
MS患者は、再発および疾患進行のリスクを低減するクラドリビンの効果と、頭痛、吐き気、軽度から中等度の感染症などの副作用のリスクを比較して、カウンセリングを受ける必要がある。また、妊娠可能な年齢の女性は、胎児に悪影響を及ぼす可能性があるため、クラドリビン服用中は妊娠しないようにカウンセリングを受ける必要がある。
クラドリビンは、10mgの経口製剤として、約1年の間隔をおいて2コース投与される。各コースは、1か月目に4 - 5回の治療日を設け、2か月目にさらに4 - 5回の治療日を設ける。推奨用量は、1.75mg/kg/年を2コースとして、2年間で3.5mg/kgを投与する。そのため、治療日毎の投与錠数は患者の体重によって異なる。
治療後は、定期的に血液検査を行い、特に白血球数と肝機能を調べて、MSの患者をモニターする。患者は、効果を評価するために、治療を担当する神経科医による定期的なフォローアップを受ける必要があり、副作用や再発があった場合には、MSサービスに連絡できるようにしておく必要がある。クラドリビンは治療後少なくとも4年間は有効であることが示されているため、最初の2年間の積極的な治療の後は、それ以上の治療を行う必要はない。しかし、患者に効果が見られない場合は、アレムツズマブ、フィンゴリモド、ナタリズマブなど、効果の高い他の疾患修飾療法に切り替えることも可能である。
研究の方向性[編集]
Cladribineは、薬剤耐性T細胞性前リンパ球性白血病に対する多剤併用化学療法の一剤として研究されている[26]。
参考資料[編集]
- ^ “Cladribine”. Drugs.com (2020年2月28日). 2020年3月4日閲覧。
- ^ Liliemark, Jan (1997). “The Clinical Pharmacokinetics of Cladribine”. Clinical Pharmacokinetics 32 (2): 120–131. doi:10.2165/00003088-199732020-00003. PMID 9068927.
- ^ a b c d “PRODUCT INFORMATION LITAK© 2 mg/mL solution for injection” (PDF). TGA eBusiness Services. St Leonards, Australia: Orphan Australia Pty. Ltd (2010年5月10日). 2014年11月27日閲覧。
- ^ a b European Medicines Agency - - Litak.
- ^ a b Leustat Injection. - Summary of Product Characteristics (SPC) - (eMC).
- ^ Leist, TP; Weissert, R (2010). “Cladribine: mode of action and implications for treatment of multiple sclerosis.”. Clinical Neuropharmacology 34 (1): 28–35. doi:10.1097/wnf.0b013e318204cd90. PMID 21242742.
- ^ “ヤンセン ファーマ 抗悪性腫瘍剤「ロイスタチン注」の輸入承認を取得”. 株式会社じほう. 2021年3月26日閲覧。
- ^ “ヤンセン ファーマ ロイスタチンの適応追加 | ニュース | ミクスOnline”. www.mixonline.jp. 2021年3月26日閲覧。
- ^ “Cladribine- cladribine injection”. DailyMed (2019年12月31日). 2020年3月4日閲覧。
- ^ “Mavenclad- cladribine tablet”. DailyMed (2019年4月10日). 2020年3月4日閲覧。
- ^ “FDA approves new oral treatment for multiple sclerosis”. U.S. Food and Drug Administration (FDA) (2019年3月29日). 2020年3月4日閲覧。
- ^ Histiocytosis Association Erdheim-Chester Disease Archived 2019-06-06 at the Wayback Machine. Page accessed Aug 20, 2016
- ^ Aricò M (2016). “Langerhans cell histiocytosis in children: from the bench to bedside for an updated therapy”. Br J Haematol 173 (5): 663–70. doi:10.1111/bjh.13955. PMID 26913480. "The combination of cytarabine and cladribine is the current standard for second-line therapy of refractory cases with vital organ dysfunction."
- ^ “ロイスタチン注8mg 添付文書”. www.info.pmda.go.jp. PMDA. 2021年3月26日閲覧。
- ^ a b c Giovannoni, G; Comi, G; Cook, S; Rammohan, K; Rieckmann, P; Soelberg Sørensen, P; Vermersch, P; Chang, P et al. (4 February 2010). “A placebo-controlled trial of oral cladribine for relapsing multiple sclerosis.”. The New England Journal of Medicine 362 (5): 416–26. doi:10.1056/NEJMoa0902533. PMID 20089960.
- ^ Johnston, JB (June 2011). “Mechanism of action of pentostatin and cladribine in hairy cell leukemia.”. Leukemia & Lymphoma 52 Suppl 2: 43–5. doi:10.3109/10428194.2011.570394. PMID 21463108.
- ^ Beutler, E; Piro, LD; Saven, A; Kay, AC; McMillan, R; Longmire, R; Carrera, CJ; Morin, P et al. (1991). “2-Chlorodeoxyadenosine (2-CdA): A Potent Chemotherapeutic and Immunosuppressive Nucleoside.”. Leukemia & Lymphoma 5 (1): 1–8. doi:10.3109/10428199109068099. PMID 27463204.
- ^ Baker, D; Marta, M; Pryce, G; Giovannoni, G; Schmierer, K (February 2017). “Memory B Cells are Major Targets for Effective Immunotherapy in Relapsing Multiple Sclerosis.”. EBioMedicine 16: 41–50. doi:10.1016/j.ebiom.2017.01.042. PMC 5474520. PMID 28161400.
- ^ Baker, D; Herrod, SS; Alvarez-Gonzalez, C; Zalewski, L; Albor, C; Schmierer, K (July 2017). “Both cladribine and alemtuzumab may effect MS via B-cell depletion.”. Neurology: Neuroimmunology & Neuroinflammation 4 (4): e360. doi:10.1212/NXI.0000000000000360. PMC 5459792. PMID 28626781.
- ^ a b Ceronie, B; Jacobs, BM; Baker, D; Dubuisson, N; Mao, Z; Ammoscato, F; Lock, H; Longhurst, HJ et al. (May 2018). “Cladribine treatment of multiple sclerosis is associated with depletion of memory B cells.”. Journal of Neurology 265 (5): 1199–1209. doi:10.1007/s00415-018-8830-y. PMC 5937883. PMID 29550884.
- ^ a b Giovannoni, G; Soelberg Sorensen, P; Cook, S; Rammohan, K; Rieckmann, P; Comi, G; Dangond, F; Adeniji, AK et al. (1 August 2017). “Safety and efficacy of cladribine tablets in patients with relapsing-remitting multiple sclerosis: Results from the randomized extension trial of the CLARITY study.”. Multiple Sclerosis (Houndmills, Basingstoke, England) 24 (12): 1594–1604. doi:10.1177/1352458517727603. PMID 28870107. オリジナルの10 March 2020時点におけるアーカイブ。.
- ^ “Sustained Efficacy - Merck Neurology”. Merck Neurology. 2018年9月28日閲覧。
- ^ Guarnera, C; Bramanti, P; Mazzon, E (2017). “Alemtuzumab: a review of efficacy and risks in the treatment of relapsing remitting multiple sclerosis.”. Therapeutics and Clinical Risk Management 13: 871–879. doi:10.2147/TCRM.S134398. PMC 5522829. PMID 28761351.
- ^ Baker, D; Herrod, SS; Alvarez-Gonzalez, C; Giovannoni, G; Schmierer, K (1 August 2017). “Interpreting Lymphocyte Reconstitution Data From the Pivotal Phase 3 Trials of Alemtuzumab.”. JAMA Neurology 74 (8): 961–969. doi:10.1001/jamaneurol.2017.0676. PMC 5710323. PMID 28604916.
- ^ “Cladribine tablets for treating relapsing–remitting multiple sclerosis”. National Institute for Clinical Excellence. 2018年9月23日閲覧。
- ^ Hasanali, Zainul S.; Saroya, Bikramajit Singh; Stuart, August; Shimko, Sara; Evans, Juanita; Shah, Mithun Vinod; Sharma, Kamal; Leshchenko, Violetta V. et al. (24 June 2015). “Epigenetic therapy overcomes treatment resistance in T cell prolymphocytic leukemia”. Science Translational Medicine 7 (293): 293ra102. doi:10.1126/scitranslmed.aaa5079. ISSN 1946-6234. PMC 4807901. PMID 26109102.
外部リンク[編集]
- “Cladribine”. Drug Information Portal. U.S. National Library of Medicine. 2021年3月26日閲覧。
